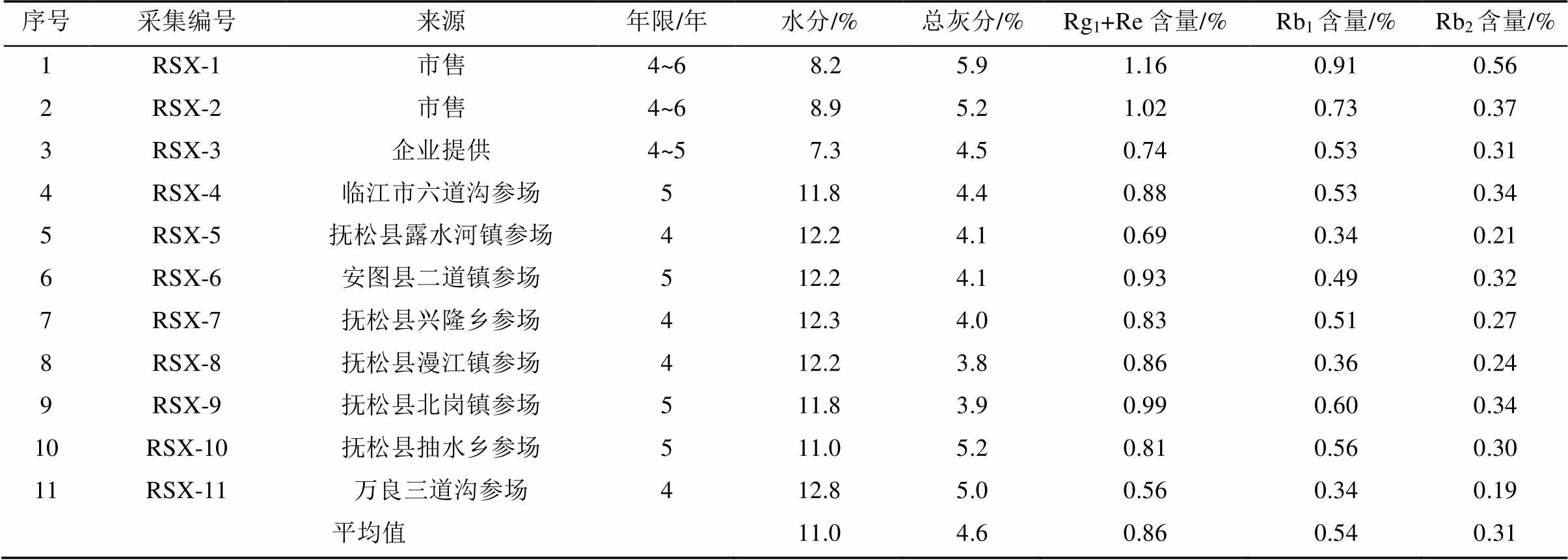
表1 样品信息及人参皂苷含量结果
Tab. 1 The specific information and ginsenoside constituent ofGinseng Leptoradix
崔业波,马晓静
(四平市食品药品检验所,吉林 四平 136000)
摘要:目的建立人参须药材质量标准。方法采用经验、显微鉴别法对该药材性状、显微特征进行描述;按照中国药典2015年版四部通则相关方法,对药材水分、总灰分进行了测定;采用薄层色谱法,分别以人参对照药材和人参皂苷(Rb1、Re、Rf和 Rg1)对照品为对照,对该药材的脂溶性成分及皂苷类成分进行定性鉴别;采用HPLC,以人参皂苷Re、Rg1、Rb1和Rb2为对照,采用Sepax BR-C18色谱柱(4.6 mm×250 mm,5 μm),乙腈-水为流动相,进行梯度洗脱,在203 nm波长下对各皂苷成分进行定量分析,建立该药材中皂苷类成分的含量测定方法。结果该药材性状、显微、薄层鉴别方法具有较强的专属性,水分平均值为11.0%,总灰分平均值为4.6%,人参皂苷Re与Rg1总含量平均值为0.86%,Rb1含量平均值为0.54%,Rb2含量平均值为0.31%。结论本研究依据实验结果和传统经验,同时结合了吉林省人参须药材的生产现状及药用企业的应用情况,可以作为人参须药材的质量标准。
关键词:人参须;质量标准;人参皂苷;薄层色谱法;高效液相色谱法
人参须为五加科植物人参Panax ginsengC.A.Mey.栽培品(俗称园参),于秋季采挖时,取下的支根或须根,加工成白直须、白弯须、红直须、红弯须等药材规格。参须始载于《本经逢源》:益气,生津,止渴,主治咳嗽吐血,口渴,胃虚呕逆。其后吴仪洛的《本草从新》及张山雷的《本草正义》中,均对参须与人参、人参条功效的区别进行了论述。人参皂苷为人参须主要的药效成分[1-3],研究表明人参须具有抗肿瘤、调节老年人免疫功能、治疗慢性咽炎等临床疗效[4-8]。
人参须在吉林省民间多用于咳嗽吐血、口渴、胃虚呕逆等症,目前被广泛应用于食品、药品和保健食品中,如心可宁胶囊、益气生津降糖胶囊。但历版中国药典均未收载本品药材质量标准。因此,人参须药材质量标准的研究及确定势在必行。通过市场调研,走访参场,可知整个吉林省长白山区的种植加工现状,被广泛应用的人参须,均为园参须,习称“白混须”,而红参须另以独立的药材规格被应用。本实验以应用为源头,以典型的应用产品心可宁胶囊为基础,建立人参须药材质量标准。
岛津LC-2010AHT高效液相色谱仪,二极管阵列检测器SPD-M20A(日本岛津公司);Agilent 1260型高效液相色谱仪(美国Agilent公司);BP211D型电子天平(赛多利斯公司);SY5200-T型超声清洗器(上海声源超声波仪器设备有限公司);linnomat5型半自动点样仪(瑞士卡玛公司);SRJX-4-9型箱式电阻炉(上海实验电炉厂);DHG-9036A型电热鼓风干燥箱(上海精宏实验设备有限公司)。
乙腈[色谱纯,赛默飞世科技(中国)有限公司],水为超纯水,其他试剂均为分析纯。硅胶G预制薄层板(青岛海洋化工有限公司,批号:20160403);人参对照药材及人参皂苷Re(批号:110754- 201525;纯度:92.3%)、Rg1(批号:110703-201530;纯度:91.7%)、Rb1(批号:110704-201424;纯度:93.7%)、Rb2(批号:111715-201203;纯度:93.8%)和Rf(批号:111719-201104)对照品均购自中国食品药品检定研究院;11批人参须药材均为市售或产地收集,由吉林农业大学韩忠明教授鉴定,见表1。
表1 样品信息及人参皂苷含量结果
Tab. 1 The specific information and ginsenoside constituent ofGinseng Leptoradix

本品较粗的支根,习称“白直须”,呈圆柱形或长圆锥形,较直或略弯曲,下部有偶有分枝,长3~15 cm,直径0.1~1.0 cm。表面灰黄色,其上偶见不明显的细小疣状突起。质脆,易折断,断面平坦,黄白色,木质部、韧皮部和形成层清晰可见。较纤细的须根,习称“白弯须”,常成团状,表面灰黄色,有细小疣状突起,质脆易折断。气微香而特异,味微苦、微甘。二者常混成团状,习称“白混须”,见图1。

图1 人参须药材
Fig. 1 Crude drug material ofGinseng Leptoradix
本品粉末呈淡黄白色。树脂道碎片易见,含黄色块状分泌物。草酸钙簇晶较小,棱角锐尖。木栓细胞表面观类方形或多角形,壁薄,略波状弯曲。网纹及梯纹导管清晰可见。淀粉粒甚多,单粒类球形,脐点点状、裂隙状或三叉状;复粒由2~6分粒组成。见图2。
2.3.1 供试品和对照品溶液的制备 取RSX-1、RSX-2、RSX-3批人参须(白直须、白弯须)药材粉末各l g,加乙醚40 ml,加热回流1 h,回收乙醚溶液备用,药渣挥干溶剂,加水0.5 ml搅拌湿润,加水饱和正丁醇10 ml,超声处理30 min,吸取上清液加3倍量氨试液,摇匀,放置分层,取上层液蒸干,残渣加甲醇l ml使溶解,作为供试品溶液。另取人参对照药材l g,同法制成对照药材溶液,并回收乙醚溶液备用。再取人参皂苷(Rb1、Re、Rf和Rg1)对照品,加甲醇制成每l ml各含2 mg的混合溶液,作为对照品溶液。

图2 人参须粉末显微图
A-白弯须显微图;B-白直须显微图;1-淀粉粒;2-草酸钙簇晶;3-树脂道碎片;4-木栓细胞;5-导管。
Fig. 2 Micrograph ofGinseng Leptoradixpowder
A-micrograph of the thinner fibrous roots of Ginseng; B-micrograph of the thicker fibrous roots of Ginseng; 1-strarch granules; 2-cluster of calcium oxalate; 3-fragments of resin cannal; 4-cork cells; 5-vesels.
2.3.2 TLC条件及结果 吸取供试品溶液、对照药材溶液及对照品溶液各1~2 μL,分别点于同一硅胶G 薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15∶40∶22∶10)10 ℃以下放置的下层溶液为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,105 ℃加热至斑点显色淸晰,分别置日光和紫外光灯(365 nm)下检视,结果见图3。
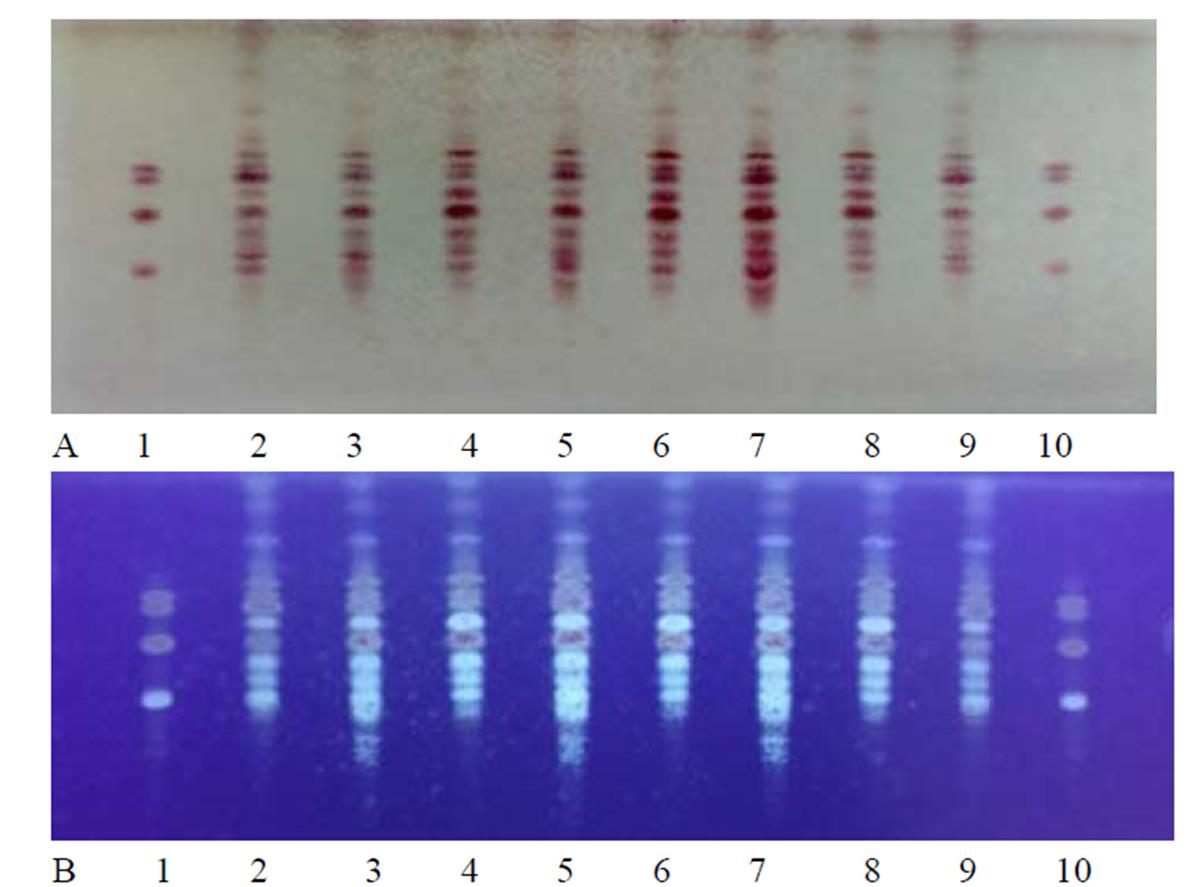
图3 人参须药材、人参对照药材及人参皂苷TLC图谱
A-日光;B-紫外光灯(365 nm);1,10-人参皂苷对照品(从上而下依次为人参皂苷Rf,Rg1,Re,Rb1);9-人参对照药材;3,5,7-RSX-1,RSX-2,RSX-3白弯须;4,6,8-RSX-1,RSX-2,RSX-3白直须。
Fig. 3 TLC ofGinseng Leptoradix,Ginseng Radixandginsenoside constituent
A-sunlight; B-UV(365 nm); 1, 10-ginsenoside constituent (from top to bottom was Rf, Rg, Re, Rb1); 2, 9-reference drug of Ginseng; 3, 5, 7-RSX-1, RSX-2, RSX-3 sample (thinner fibrous roots of Ginseng); 4, 6, 8-RSX-1, RSX-2, RSX-3 sample (thicker fibrous roots of Ginseng).
2.4.1 供试品和对照药材溶液的制备 取“2.3.1”项下的供试品溶液和人参对照药材溶液制备过程中回收的乙醚溶液,蒸干,加入1 ml的乙酸乙酯使溶解,分别作为供试品溶液和人参对照药材溶液。
2.4.2 TLC条件及结果 吸取供试品溶液与对照药材溶液各4 μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-石油醚(60~90 ℃)(1∶5)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105 ℃加热至斑点显色清晰,分别置日光和紫外光灯(365 nm)下检视,结果见图4。
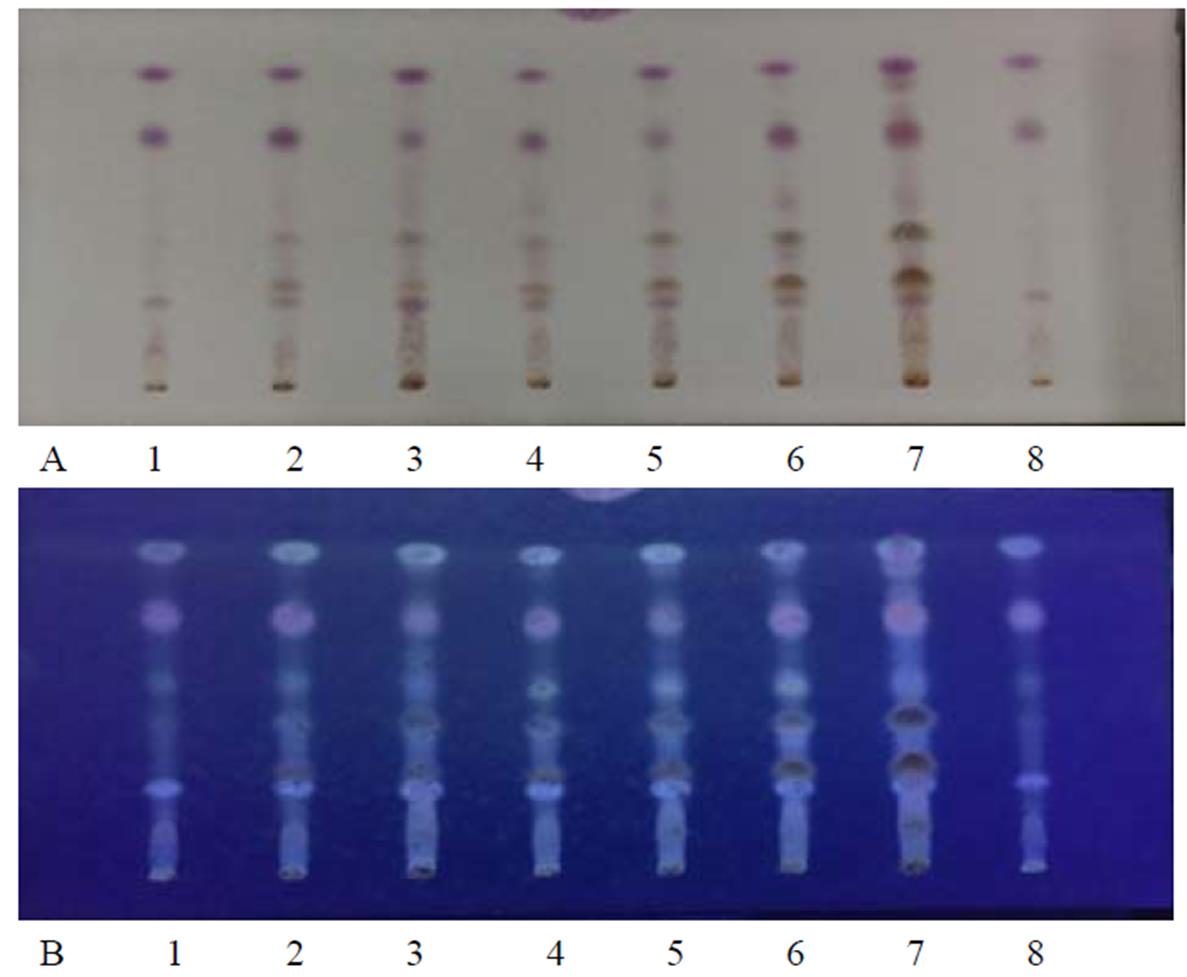
图4 人参须药材与人参对照药材TLC图谱
A-日光;B-紫外光灯(365 nm);1,8-人参对照药材;2,4,6-RSX-1,RSX-2,RSX-3白直须;3,5,7-RSX-1,RSX-2,RSX-3白弯须。
Fig. 4 TLC ofGinseng LeptoradixandGinseng Radix
A-sunlight; B-UV(365 nm); 1, 8-reference drug of Ginseng; 2, 4, 6-RSX-1, RSX-2, RSX-3 sample (thicker fibrous roots of Ginseng); 3, 5, 7-RSX-1, RSX-2, RSX-3 sample (thinner fibrous roots of Ginseng).
按照中国药典2015年版四部通则0832和通则2302进行水分测定及总灰分测定,结果见表1。
2.6.1 色谱条件及系统适用性 采用Sepax BR-C18(4.6 mm×250 mm,5 μm)色谱柱,流动相:乙腈(A)-水(B),梯度洗脱(0~35 min,17%A;35~ 55 min,17%→26%A;55~70 min,26%A;70~ 100 min,26%→40%A);流速:1.0 ml·min-1,柱温20 ℃,检测波长203 nm,进样量20 μl,理论板数按人参皂苷Rg1峰计算应≥6 000。空白溶剂、对照品及供试溶液的HPLC图见图5。
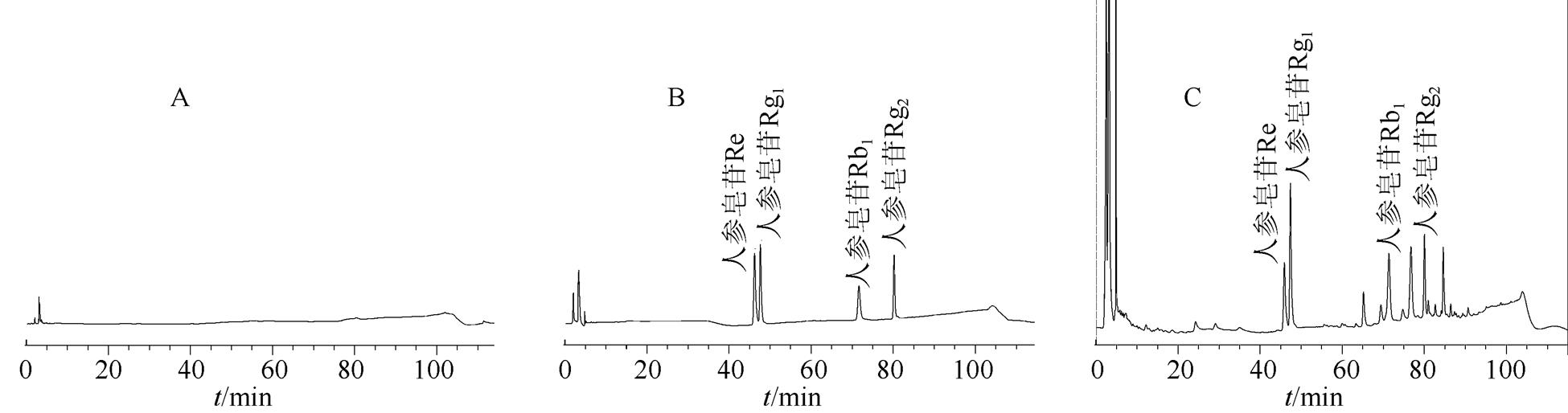
图5 高效液相色谱图
A-空白溶剂;B-混合对照品;C-人参须供试品。
Fig. 5 HPLC chromatograms
A-blank solvent; B-reference substance; C-sample solution.
2.6.2 供试品溶液的制备 取本品粉末(过四号筛)约l g,精密称定,置索氏提取器中,加乙醚加热回流3 h,弃去乙醚液,药渣挥干溶剂,连同滤纸筒移入100 ml锥形瓶中,精密加水饱和正丁醇50 ml,密塞,放置过夜,超声处理(功率250 W,频率50 kHz)30 min,滤过,弃去初滤液,精密量取续滤液25 ml,置蒸发皿中蒸干,残渣加甲醇溶解并转移至10 ml量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
2.6.3 对照品溶液的制备 精密称取人参皂苷Rg1对照品、人参皂苷Re对照品、人参皂苷Rb1对照品及Rb2对照品,加甲醇制成每l ml依次含0.1,0.2,0.2,0.1 mg的混合溶液,摇匀,即得。
2.6.4 仪器精密度试验 取“2.6.3”项下对照品溶液,重复进样6次,人参皂苷Rg1、Re、Rb1和Rb2峰面积RSD均<2%,表明仪器精密度良好。
2.6.5 线性关系的考察 精密称取人参皂苷Rg1、Re、Rb1和Rb2对照品适量,用甲醇溶解并稀释,制成依次含量为0.094,0.196,0.205,0.096 mg·mL-1的混合溶液。分别精密吸取对照品溶液5,10,15,20,25 μl,依次注入液相色谱仪中,记录色谱图,以峰面积为纵坐标,各对照品质量数为横坐标,进行线性回归,得线性方程:Y(Rg1)=626.36X+ 19.49,R2=1.00;Y(Re)=301.98X+54.87,R2=0.999;Y(Rb1)=283.62X-7.26,R2=1.00;Y(Rb2)=304.37X-3.42,R2=1.00。人参皂苷Rg1的线性范围为0.47~ 2.35 μg、Re为0.98~3.92 μg、Rb1为1.03~4.12 μg,Rb2为0.48~1.92 μg。
2.6.6 重复性试验 取同一批药材6份,按“2.6.2”项下方法制备供试品溶液和“2.6.1”项下色谱条件进行分析,结果表明人参皂苷Rg1+Re、Rb1和Rb2平均含量为0.86%,0.38%和0.25%。
2.6.7 稳定性试验 取同一供试品溶液按照“2.6.1”项下色谱条件分别于0,2,4,6,8,12,14,26 h精密量取20 μl注入液相色谱仪,记录色谱图,以人参皂苷Rg1、Re、Rb1和Rb2峰面积考察溶液稳定性,结果显示人参皂苷Rg1、Re、Rb1和Rb2峰面积的RSD依次为0.3%,0.4%,1.0%,1.0%。
2.6.8 回收率试验 精密称取已知含量的同一批药材6份各1 g,精密称定,对照品的加入量按照1∶1加入,按“2.6.2”项下方法处理,按“2.6.1”项下色谱条件进行测定,结果人参皂苷Rg1+Re、Rb1和Rb2加样平均回收率依次93.%(RSD= 0.6%),94%(RSD=2.8%),104%(RSD=3.0%)。
2.6.9 色谱柱耐用性 取同一批药材,按“2.6.2”项下方法制备2份供试品溶液;按上述色谱条件分别用不同色谱柱Sepax BR-C18(4.6 mm×250mm,5 μm)、WondaSil C18-WR(4.6 mm×250 mm,5 μm)、Inertsil ODS-3(4.6 mm×250 mm,5 μm)进样分析,人参皂苷Rg1+Re、Rb1和Rb2的RSD依次为1.8%,3.4%,4.0%。
2.6.10 样品测定 取上述11批次药材,按“2.6.2”项下方法处理,按“2.6.1”项下色谱条件进行含量测定,样品中人参皂苷Rg1+Re、Rb1和Rb2的含量依次为0.56%~1.16%,0.34%~0.91%,0.19%~ 0.56%,结果见表1。
本实验参考文献及中国药典2015年版一部人参药材的质量标准中含量分析方法[10-15]。对比氯仿与乙醚脱脂对人参皂苷含量测定的影响,结果表明,二者无差异,考虑绿色环保因素,因此在供试样品制备过程改为乙醚脱脂;通过研究,不同来源及产地的人参须中皂苷含量差异较大,白弯须中人参皂苷含量明显最高,其次为白混须,再次为白直须;经过对比,人参须中Rg1和Rb1明显高于人参药材。孙光芝等[16]报道人参皂苷Rb2具有脂肪代谢、肝脏糖代谢等方面的药理学作用。鉴于其药理学作用与人参须功能主治及目前临床应用的相关性,本实验对人参须中的人参皂苷Rb2含量进行定量分析,为以后人参须药材的开发利用提供实验依据。
本实验比较了白弯须和白直须的粉末显微特征,二者无明显的区别,只是在数量及观察难度上有区别,例如草酸钙簇晶在白弯须中较难观察。白直须粗端的横切面显微特征包括:木质部、形成层、韧皮部、木射线、导管、树脂道、木栓层及草酸钙簇晶清晰可见,与人参药材横切面一致;其中段及末端横切面十分难以操作,未对其进行研究与对比。
薄层鉴别沿用了人参药材质量标准的鉴别,将氯仿改为乙醚,并通过验证,二者对皂苷类成分的鉴别均无差异,从而使标准更环保。通过图2可知,白弯须皂苷的种类明显多于人参对照药材,并且斑点颜色更深;而白直须确与人参药材相似。本实验就其展开剂[石油醚(30~60 ℃/60~90 ℃)-乙酸乙酯(5∶1)、丙酮-二氯甲烷(1∶6)和甲酸乙酯-环己烷(3∶7)]、吸附剂(硅胶GF254、硅胶H)及显色剂(10%硫酸乙醇和5%三氯化氯)、点样量及温湿度的影响进行了考察。结果表明,点样量为4 μL,吸附剂为硅胶G,以乙酸乙酯-石油醚(60~90 ℃)(1∶5)为展开剂,显色方式以喷10%硫酸乙醇溶液,在105 ℃加热至斑点显色清晰,分别置日光和紫外光灯(365 nm)下检视为最佳。由图4可知,白弯须及白直须的斑点个数明显有别于人参对照药材,为人参须进一步研究提供实验依据。
由表1可知,白混须水分平均值11.0%,由于人参须为加工人参过程中获得,已经经过了工厂或参厂的处理,又由于在东北春季测定,气候比较干燥,因此,拟定水分限度≤13.0%。11批白混须总灰分的平均值为4.6%,参考人参药材质量标准,结合人参须生产加工条件,拟定总灰分限度≤5.5%。鉴于人参须总灰分量较小,完全可控制药材质量,因此不再进行酸不溶性灰分测定。含量测定指标成分较多,因此不再就其药材的浸出物进行研究。
REFERENCES
[1] XU J, JIA L, ZHAO Y Q. Constituents of Ginseng and quality evaluation of Ginseng products [J]. Drug Eval Res(药物评价研究), 2011, 34(3): 199-203.
[2] 孟繁荣. 人参的化学成分与人参产品的质量评价[J]. 食品安全导刊, 2016(27): 102.
[3] LIANG H, LI B, LIU Y F, et al. Determination of notoginsenoside R1, ginsenoside Rg1,Re, Rb1and Rd in Notoginsenoside-ginseng Amino Acid capsules by HPLC [J]. Pharm Today(今日药学), 2017, 27(8): 528-531.
[4] ZHANG D R, FENG D. Rsearch advances on application of ginsenosides in liver diseases [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2016, 33(5): 671-675.
[5] 梁仲培, 谢美恩, 古英明, 等. 人参须糖浆对二甲基奶油黄诱发大白鼠肝癌的影响[J]. 广州医学院学报. 1986, 14(2): 8.
[6] 张绍景, 朱科伦, 马佩球, 等. 人参须对老年人免疫功能调节作用的探讨[J]. 广州医学院学报, 1987, 15(4): 32.
[7] YIN D F.Treating 52 cases of chronic pharyngitis by Runyantang [J]. Hunan Guid J TCM(湖南中医药导报), 2002, 8(9): 531-532.
[8] TAN S Q, XU Y H, WANG L Z, et al. New progress on anti-tumor effect of ginsenoside Rg3[J]. Ginseng Res(人参研究), 2016, 28(3): 46-48.
[9] 中国药典. 一部[S]. 2015: 8-9.
[10] CHEN L, LI C Y, WANG Z, et al.Quantitation of nine ginsenosides inPanax ginsenghairy roots and other Panax ginseng plant components by HPLC [J]. J Pharm Pract(药学实践杂志), 2016, 4(34): 313-317.
[11] CAI Y, SONG J, WANG G J, et al. Determination of 7 kinds of ginsenosides inPanax ginsengin the extract of Ginseng radix by UPLC [J]. Northwest Pharm J(西北药学杂志), 2016, 5(31): 441-445.
[12] 杨秀伟, 王洪平, 徐嵬, 等. 不同产地人参根和根茎中人参皂苷的含量分析 [J]. 药物分析杂志, 2017, 37(1): 30-36.
[13] ZHANG Y, WANG Y H, XUE X L.Contents determination of ginsenoside inPanax ginsengfrom different regions in Jilin province [J]. Northern Horticult(北方园艺), 2016(1): 137-139.
[14] PANG S F, LI Y L, XU S Q, et al. Investigation of ginsenosides in different parts ofPanax ginseng[J]. Ginseng Res(人参研究), 2015, 27(1): 5-8.
[15] Nolte j, Nigge w, Hohaus e, et al. Comparative study of extraction techniques with ammonia or methanol/water for the isolation of ginsenosides using HPLC/MS [J]. Zeitschrift für Naturforschung B, 2015, 60(2): 205-210.
[16] SUN G Z, WANG J Y, LIU Z, et al. General view on pharmacological research of ginsenoside-Rb2[J]. J Jilin Agric Univ(吉林农业大学学报), 2005, 27(3): 299-305.
CUI Yebo, Ma Xiaojing
(Siping City Institute for Food and Drug Control, Siping 136000, China)
Abstract:OBJECTIVETo establish quality standards ofGinseng Leptoradix.METHODSEmpircal and microscopic identification methods were adopted to observe morphological and histological characters. The contents of water and total ash were analyzed according to the methods of Chinese Pharmacopoeia(2015). Ginsenoside constituent(Rb1, Re, Rf, Rg1) and reference herbs were used to identify materia medica ofGinseng Leptoradix.The ginsenoside constituent were analyzed by HPLC, Ginsenoside constituent (Re, Rg1, Rb1, Rb2) was used as reference substances. The determination method was performed on a Sepax BR-C18column(4.6 mm×250 mm, 5 μm) with acetonitrile-water as the mobile phase, which was a multi-step acetonitrile-water gradient run. The detection wavelength was 203 nm.RESULTSThe macroscopical identification, microscopic features and TLC methods were proper. The average congtents of water, total ash and ginsenoside constituent(Re and Rg1, Rb1, Rb2) were 11.0%, 4.6%, 0.86%, 0.54% and 0.31%, respectively.CONCLUSIONThe quality standards established based on the research results, traditional experience and the production status ofGinseng Leptoradixin Jilin Province, which is suitable for the quality evaluation ofGinseng Leptoradix.
KEY WORDS:Ginseng Leptoradix; quality standards; ginsenoside constituent; TLC; HPLC
中图分类号:R284.1
文献标志码:B
文章编号:1007-7693(2018)09-1360-05
DOI:10.13748/j.cnki.issn1007-7693.2018.09.020
引用本文:崔业波, 马晓静. 人参须药材质量标准的研究[J]. 中国现代应用药学, 2018, 35(9): 1360-1364.
收稿日期:2017-12-12
基金项目:吉林省中药材标准制修订项目(计划文号2015〔304〕)
作者简介:崔业波,男,硕士,主管药师 Tel: (0434)3256832 E-mail: cuiyebo@163.com
(本文责编:曹粤锋)