 表示,检验水准α=0.05。
表示,检验水准α=0.05。业康1,叶兴法2,黄晶晶1,韩鹏2,金捷1,毛培江1*
(1.浙江省中药研究所,杭州 310023;2.浙江景岳堂药业有限公司,浙江 绍兴 312025)
摘要:目的比较制草乌、姜半夏配方颗粒与饮片煎剂的急性毒性差异。方法参照国家药品监督管理局2014年发布的《药物单次给药毒性研究技术指导原则》,对制草乌、姜半夏配方颗粒与其饮片煎剂进行小鼠急性毒性实验,根据毒性实验结果的不同,分别以最小致死量(minimum lethal dose,MLD)或最大给药量(maximum administration dosage,MAD)来反映制草乌、姜半夏配方颗粒与其各自饮片煎剂的毒性差异。结果制草乌饮片煎剂的MLD值在生药25.6~32 g·kg-1之间,而制草乌配方颗粒的MLD值在生药40~50 g·kg-1之间;姜半夏饮片煎剂与姜半夏配方颗粒小鼠灌胃的MAD均为生药238.872 g·kg-1,以姜半夏在中国药典2015年版中的上限用量9 g·d-1计算,相当于人用剂量的1 592.48倍。结论制草乌颗粒的毒性明显低于制草乌饮片煎剂;姜半夏配方颗粒与饮片煎剂均未见毒性表现。
关键词:制草乌;姜半夏;配方颗粒;饮片煎剂;毒性
中药配方颗粒也称“单味中药浓缩颗粒”“中药新型颗粒饮片”“免煎饮片”等,是以符合炮制规范的中药饮片为原料,经现代制药技术提取、浓缩、分离、干燥、制粒、包装精制而成的供中医临床配方用的颗粒,是对传统饮片的补充[1-2]。目前关于中药配方颗粒的研究报道,以制备工艺、化学成分、质量标准等居多,药效学研究较少,毒性及安全性研究更少[3-4]。本研究拟通过对有毒药材草乌和半夏配方颗粒的急性毒性实验,研究中药配方颗粒与相应的饮片煎剂间的毒性差异,为中药配方颗粒临床应用的安全性,提供实验依据。
ICR小鼠,SPF级,160只,♀♂各半,由浙江省实验动物中心提供。实验动物生产许可证号:SCXK(浙)2014-0001。质量合格证号:1709300010 (110只用于制草乌实验)、1707200022(50只用于姜半夏实验)。饲养于清洁级动物房内,温度18~ 26 ℃,相对湿度50%~60%,光照明暗交替各12 h,通风每小时22次。实验动物使用许可证号:SYXK(浙)2013-0188。
制草乌配方颗粒[批号:K1604074,规格:每袋100 g(每克颗粒相当于饮片6 g)]、制草乌饮片(批号:16031401;规格:每袋2 kg)、姜半夏配方颗粒[批号:K1704059;规格:每袋100 g(每克颗粒相当于饮片12 g)]、姜半夏饮片(批号:17042106;规格:每袋1 kg)均由浙江景岳堂药业有限公司提供,配方颗粒均由相应同一批次中药饮片制得,饮片质量均符合中国药典2015年版的要求[5]。
制草乌饮片煎剂的制备:取适量中药饮片于清洁煎药罐,加入8倍量的去离子纯净水,浸泡1 h后开始煎煮,待充分煮沸后再煎煮40 min,煎煮过程中用玻璃棒搅拌2~3次,保证充分煎透,无糊块状,无白心,无硬心。趁热用80目药筛过滤,药渣同法再煎煮1次,合并2次滤液,浓缩至1.56 g生药·mL-1。
姜半夏饮片煎剂的制备:预试验结果显示需要进行最大给药量(maximum administration dosage,MAD)实验,由于姜半夏药液含固量比较高,故采用冷冻干燥技术处理。500 g生药饮片同法(参考制草乌)煎煮后,滤液经冷冻干燥得124.8 g粉末,得率与含量分别为24.96%与生药4.01 g·g-1,临用时用蒸馏水溶解配制成适合抽取灌胃的最大浓度(生药1.99 g·mL-1)。
AWH-3-SA型电子天平(上海英展机电企业有限公司);HX103T型电子天平(慈溪市天东衡器厂);Scien-100F冷冻干燥机(宁波新芝生物科技股份有限公司)。
ICR小鼠110只,体质量18~22 g,♀♂各半,按体质量随机分为11个组别,10个给药组与1个对照组,每组♀♂各5只,按表1剂量给药,给药前禁食不禁水24 h,按0.4 mL·(10 g)-1灌胃给药,对照组灌胃给予等容的生理盐水(NS)。给药结束即刻观察小鼠的反应情况,包括动物饮食、外观、行为、分泌物、排泄物、死亡情况及中毒反应(参照CFDA 2014年发布的《药物单次给药毒性研究技术指导原则》)等,连续观察2 h,之后分别在给药后4,8,24 h各观察1次。以后每天观察1次,连续观察14 d,每3天称体质量1次。如有动物死亡,则对死亡动物及时进行大体解剖,若肉眼发现有器官出现体积、颜色、质地等改变时,则对改变的器官进行组织病理学检查。存活动物在试验观察结束后,脱颈椎处死并剖检,对脏器组织进行大体检查。
体质量18~22 g的ICR小鼠50只,♀♂各半,按体质量随机分为3组,分别为姜半夏饮片组(♀♂各10只)、姜半夏配方颗粒组(♀♂各10只)和NS对照组(♀♂各5只)。给药前禁食不禁水过夜后,按0.4 mL·(10 g)-1灌胃给药,每日给药3次,间隔时间为4 h,姜半夏饮片组和配方颗粒组每次给药剂量为生药79.6 g·kg-1,24 h内3次给药总剂量为生药238.872 g·kg-1。对照组灌胃给予等容的NS。给药后观察方法同“2.1”项。
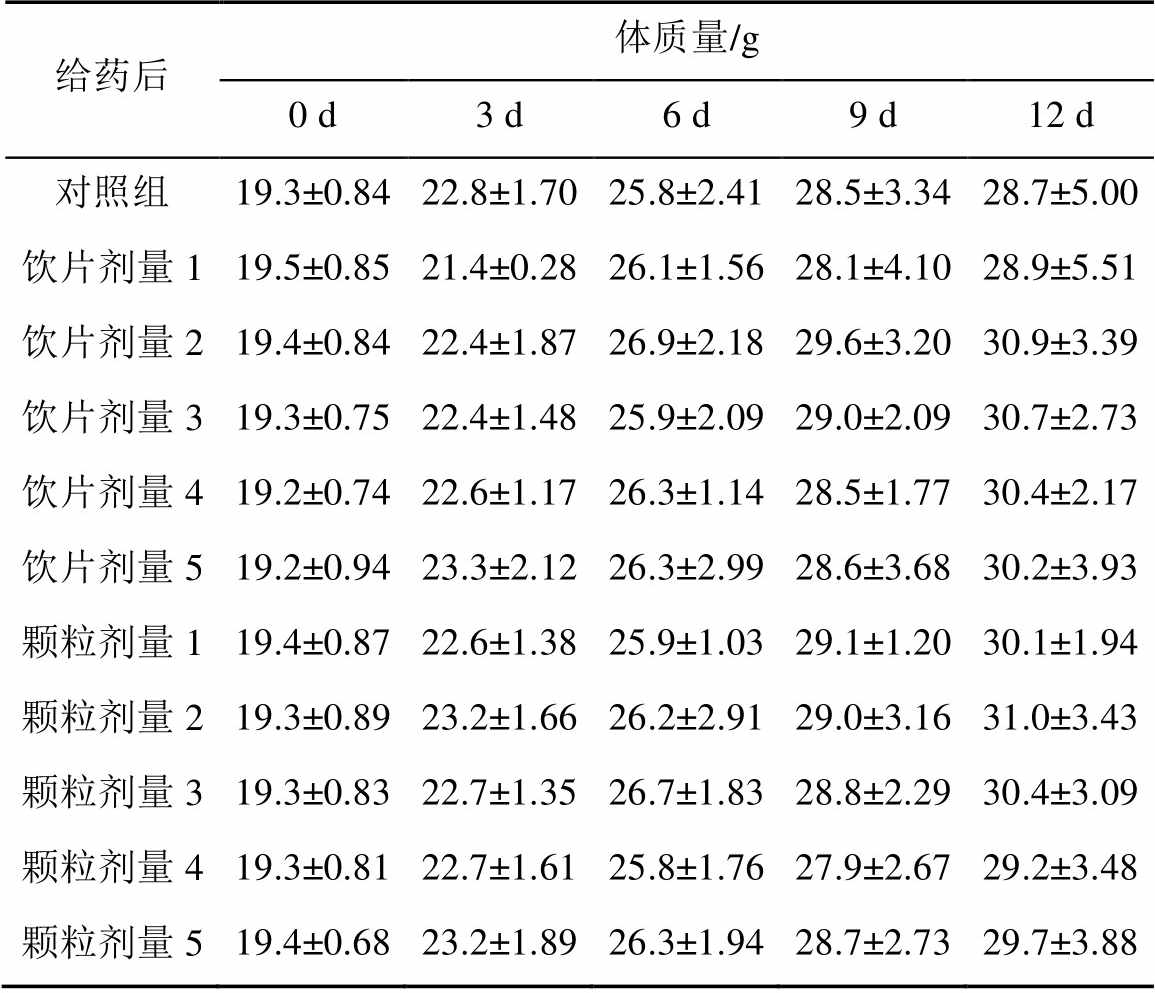
利用IBM SPSS Statistics 20统计软件对实验数据进行单因素方差(one-way ANOVA)分析,结果用 表示,检验水准α=0.05。
表示,检验水准α=0.05。
3.1.1 动物存活情况 制草乌饮片煎剂与配方颗粒组小鼠给药后约20 min开始出现中毒症状,活动减少,俯卧,呼吸困难,口吐白沫,上下睑下垂,尿失禁。动物死亡均出现在给药后2 h内,小鼠死亡前有震颤、散瞳、角弓反张等症状,见表1。动物中毒症状于2 h后逐渐缓解,未死亡小鼠在4 h后逐渐恢复正常。
不同时间点的各组动物平均体质量数据均符合方差齐性要求,与对照组比较,经Dunnett-t检验,制草乌饮片组、制草乌配方颗粒组与对照组比较均无显著差异。见表2。
表1 动物死亡情况
Tab. 1 The death situation of the mice
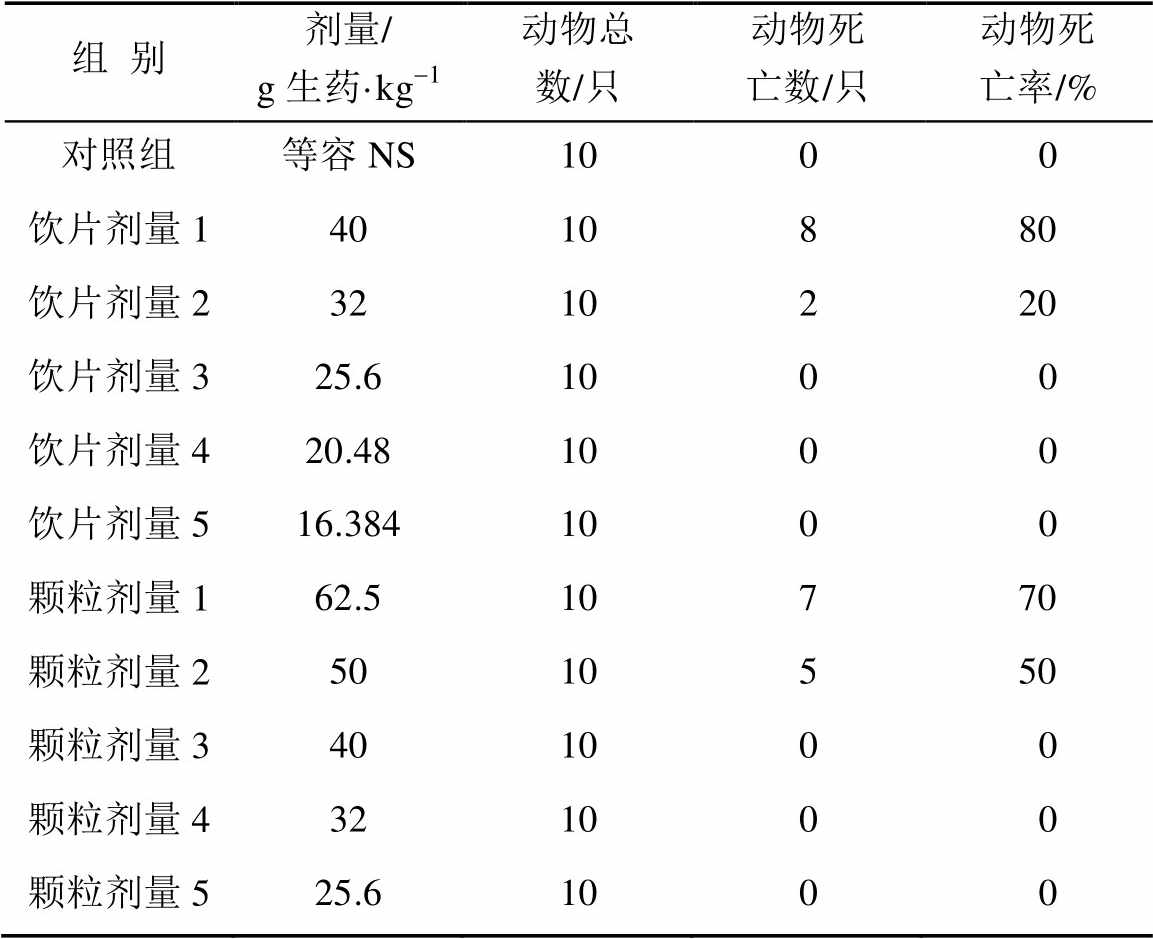
表2 动物体质量变化(n=10,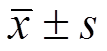 )
)
Tab. 2 The body weight change of the mice(n=10,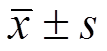 )
)
注:给药前各组动物数为10只,给药后由于部分动物死亡,该数据为存活动物平均体质量。
Note: The number of animals in each group was 10 before the administration, because some animals died after the administration, the data were the average weight of the living animals.
3.1.2 动物主要器官观察结果 死亡小鼠解剖观察其心脏、肝脏、脾脏、肺与肾脏等器官,给药组小鼠肺部均有出血、萎缩等病变,肾脏、肝脏、心脏颜色加深,脾脏未见明显异常。实验结束后颈椎脱臼处死存活小鼠,观察其心脏、肝脏、脾脏、肺与肾脏等器官,与对照组比较,未见异常。
3.1.3 结论 制草乌饮片煎剂的最小致死量(minimum lethal dose,MLD)在生药25.6~32 g·kg-1之间,而制草乌配方颗粒的MLD值在生药40~50 g·kg-1之间,制草乌颗粒的毒性明显低于制草乌饮片煎剂。
3.2.1 动物存活情况 经14 d的观察周期后实验小鼠均存活,实验期间小鼠精神状态、进食、饮水及粪便均无异常。实验期间各组小鼠平均体质量均未见显著性差异,见表3。
表3 动物体质量变化(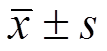 )
)
Tab. 3 The body weight change of the mice(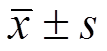 )
)

注:实验期间无小鼠死亡, 各组小鼠平均体质量均未见显著性差异。
Note: No mice died during the experiment. There was no significant difference in the average weight of the mice in each group.
3.2.2 动物主要器官观察结果 实验结束后,颈椎脱臼处死小鼠,解剖观察心脏、肝脏、脾脏、肺与肾脏等器官,与对照组比较,肉眼观察无异常病理变化。
3.2.3 结论 姜半夏饮片煎剂与姜半夏配方颗粒小鼠灌胃的MAD均为生药238.872 g·kg-1,以姜半夏在中国药典2015年版上限用量9 g计算,相当于人用剂量的1 592.48倍,两者在该剂量下均无毒性表现。
中药配方颗粒是传统中药饮片的改良剂型,具有质量可控、方便携带、调配灵活等优点。中药饮片制成配方颗粒后的药效差异得到了众多学者的关注,如杨蓉[6]系统分析评价了大承气汤配方颗粒与汤剂的化学成分、大肠杆菌生物热活性以及便秘型小鼠的药效作用,研究结果表明大承气汤配方颗粒与汤剂对大肠杆菌生物热活性以及便秘型小鼠均有阳性作用且二者之间无显著性差异;吴昊等[7]通过研究人参饮片与配方颗粒对小鼠抗疲劳能力、常压耐缺氧能力以及胸腺、脾脏等免疫器官质量的影响,发现人参饮片与配方颗粒均可提高小鼠的免疫与抗应激能力,但二者对比药效无显著性差异。全智慧等[8]以二甲苯致小鼠耳肿胀模型评价制川乌配方颗粒与标准煎剂的抗炎作用,发现在抗炎方面制川乌配方颗粒和制川乌标准煎剂的等剂量效应不具有等效性,制川乌配方颗粒等剂量效应较制川乌标准煎剂大;以上研究说明中药饮片在制成配方颗粒后并没有降低其药效。有毒中药材如草乌、半夏等制成配方颗粒后的毒性也受到关注,但目前实验研究报道较少。任艳青等[9]探索性地利用体外正常肝细胞LO2为研究载体,通过MTT法与Hoechst 33258荧光染色法评价栀子、连翘、大黄等10种中药配方颗粒的细胞毒性,但该研究未进行中药饮片的汤剂与配方颗粒的毒性对比。本研究以有毒药材制草乌、姜半夏为研究对象,通过小鼠急性毒性实验,评价中药饮片制成配方颗粒后毒性的变化。实验结果中制草乌配方颗粒的毒性低于其水煎剂,可能是由于草乌中剧毒成分双酯型二萜类生物碱发生了分解(如乌头碱、中乌头碱、次乌头碱等,含量一般不足1%,其对心脏及神经系统具有较大的毒性)。此类成分化学性质不稳定,遇水加热易水解成毒性较小的单酯型生物碱,继续水解可生成毒性更小的乌头原碱,制草乌配方颗粒制药工艺中提取温度、提取时间对双酯型二萜类生物碱分解起关键作用。笔者将进一步研究有毒中药配方颗粒制药工艺中成分的变化以及体外药效评价体系的建立。
REFERENCES
[1] ZHOU J L. Historic review and future prospect of TCM formula granules [J]. Mod Chin Med(中国现代中药), 2016, 18(9): 1093-1096.
[2] GUO M X, WU C, TONG W H. Research progress in equivalence study of TCM dispensing granule and traditional herbal decoction [J]. Mod Chin Med(中国现代中药), 2016, 18(9): 1107-1110.
[3] ZHUANG J R, XU D S, LIU L, et al. Analysis of superiorities and inferiorities of Chinese medicine dispensing granule [J]. Chin J Inf Tradit Chin Med(中国中医药信息杂志), 2014, 21(7): 8-10.
[4] 王永和. 中药配方颗粒的现状及最新研究进展[J]. 中国卫生产业, 2014, 11(8): 188-189.
[5] 中国药典. 一部[S]. 2015: 236-237, 119-120.
[6] 杨蓉. 大承气汤配方颗粒与汤剂的比较研究[D]. 北京: 北京中医药大学, 2014.
[7] 吴昊, 刘同彥, 刘佳, 等. 人参饮片与配方颗粒药效的比较研究[J]. 人参研究, 2017, 29(1): 8-10.
[8] QUAN Z H, ZHAO Z M, HUANG X J, et al. Comparison on inhibition between Aconiti Radix Cocta formula granule and standard decoction on ear swelling of mice induced by dimethyl benzene [J]. Drug Eva Res(药物评价研究), 2014, 37(4): 309-316.
[9] 任艳青, 李葆林, 田宇柔, 等. 栀子、连翘等中药配方颗粒体外肝细胞毒性研究[J]. 河北中医药学报, 2017, 32(1): 43-46.
Comparative Study on Acute Toxicity of Aconiti Kusnezoffii Radix Cocta, Pinelliae Rhizoma Praeparatumcum Zingibere Et Alumine Formula Granule and Decoction
YE Kang1, YE Xingfa2, HUANG Jingjing1, HAN Peng2, JIN Jie1, MAO Peijiang1*
(1.Zhejiang Research Institute of Traditional Chinese Medicine, Hangzhou 310023, China; 2.Zhejiang Jingyuetang Pharmaceutical Limited Company, Shaoxing 312025, China)
ABSTRACT:OBJECTIVETo compare the acute toxicity between formula granule and decoction of Aconiti Kusnezoffii Radix Cocta and Pinelliae Rhizoma Praeparatumcum Zingibere Et Alumine.METHODSReferring toTechnical Guidelines for the Study of Single Dose AdministrationDrug Toxicitypublished by CFDA in 2014, the acute toxicity test of formula granule and decoction of Aconiti Kusnezoffii Radix Cocta and Pinelliae Rhizoma Praeparatumcum Zingibere et Alumine was performed. According to the experimental results, the toxicity differences were studied with minimum lethal dose method(MLD) and maximum administration dose method(MAD) respectively.RESULTSThe MLD value of the decoction was between 25.6-32 g·kg-1, and the MLD value of the formula granule was between 40-50 g·kg-1of Aconiti Kusnezoffii Radix Cocta. The MAD value of formula granule and decoction of Pinelliae Rhizoma Praeparatumcum Zingibere et Alumine were both 238.872 g·kg-1. It was equivalent to 1 592.48 times of the upper limit (9 g·d-1) dose of the 2015 Edition of Pharmacopoeia.CONCLUSIONThe toxicity of formula granule is significantly lower than the decoction of Aconiti Kusnezoffii Radix Cocta. Formula granule and decoction of Pinelliae Rhizoma Praeparatum Cum Zingibere et Alumine are both non-toxic.
KEY WORDS:Aconiti Kusnezoffii Radix Cocta; Pinelliae Rhizoma Praeparatumcum Zingibere et Alumine; formula granule; decoction; toxicity
中图分类号:R285.5
文献标志码:A
文章编号:1007-7693(2018)09-1347-04
DOI:10.13748/j.cnki.issn1007-7693.2018.09.017
引用本文:业康, 叶兴法, 黄晶晶, 等.制草乌、姜半夏中药配方颗粒与饮片煎剂的急性毒性比较研究[J]. 中国现代应用药学, 2018, 35(9):1347-1350.
收稿日期:2017-12-07
基金项目:浙江省科技计划项目(2018F10079)
作者简介:业康,男,硕士,助理工程师 Tel: (0571)85241073 E-mail: yksimon1988@163.com
*通信作者:毛培江,男,硕士,高级工程师 Tel: (0571)85241073 E-mail: maopeijiang@163.com
(本文责编:李艳芳)