表1 市售4种中药注射剂
Tab. 1 Four Chinese medicine injections in drug store

桑晶,陈舒怀,蒙宏,谢珍,匡荣*
(浙江省食品药品检验研究院,杭州 310004)
摘要:目的研究体外人源细胞激活试验法(human cell line activation test,h-CLAT)用于中药注射剂过敏反应检查的可行性,探讨中药注射剂的Ⅳ型变态反应体外检测的可行性。方法参考OECD指导原则442E的h-CLAT法,应用流式细胞仪在类树突样的人源白血病细胞系THP-1上对4种中药注射剂进行体外过敏反应检查,根据THP-1细胞表面抗原CD86和CD54的相对荧光强度评价4种中药注射剂体外过敏反应;同时采用体内过敏反应对4种注射剂进行评价。结果体外皮肤过敏试验表明,树突状细胞表面特异抗原CD86相对荧光强度值<150,CD54的相对荧光强度值<200,根据判定标准结果为阴性,与体内法结果一致。结论h-CLAT法具有检验周期短、测试方法简便、评价客观等优点,是一种较好的检查中药注射剂过敏反应的替代方法。
关键词:人源细胞激活试验;皮肤变态反应;替代方法
中药注射剂是我国特有的剂型,随着中药注射剂在临床中的广泛应用,临床过敏和类过敏反应报道逐年增加,中药注射剂的安全性受到越来越多的关注。目前,中国药典2015年版对中药注射剂的过敏反应试验以及药物临床前安全性评价仍以传统的豚鼠主动全身过敏法和/或PCA反应法为主。但这2种方法都存在动物使用量大、试验周期长、动物与人反应差异大、结果判定主观等缺点,同时这2种方法也很难实现临床前的高通量快速筛选[1-2]。近年来随着3R理念的深入,越来越多的研究致力于开发新的体外过敏反应检查方法[3-4]。
体外人源细胞激活试验2016年被收录到OECD指南中,作为一种对化学品的潜在致敏性评价的体外测试方法,其主要原理是通过检测DC样细胞系接触化学物后的激活状态,以致敏过程中树突状细胞特异性表达的表面分子CD86、CD54的表达增强作为判断标准[2,4-5]。本研究评价体外人源细胞激活试验法用于评价中药注射剂过敏反应检查的可行性,以推动中药注射剂的过敏反应检查体外方法的开发。
HERAcell150i型号二氧化碳培养箱 (Thermo Scientific公司);DMI3000B型显微镜(美国Leica公司);FACSVerseTM System 型流式细胞仪(美国BD);Sorvall ST8型水平式离心机(Thermo公司);ACS-20-TE型号的电子天平(Mettler Toledo公司)。
4种中药注射剂样品见表1。
表1 市售4种中药注射剂
Tab. 1 Four Chinese medicine injections in drug store

人源白血病细胞系THP-1 (上海中科院细胞资源中心);RPMI-1640培养液 (GIBCO公司,批号:1864173);胎牛血清(浙江天杭生物科技有限公司,批号141013);磷酸盐缓冲液(DPBS,含钙镁离子,批号:1740576);流式上样缓冲液临用时用水配成2%溶液;CD86同型对照FITC标记小鼠源IgG1抗体(BD公司,批号:7313762);FITC标记鼠源单克隆抗人CD54抗体(DAKO公司,批号:20038138);FITC标记鼠单克隆抗人CD86抗体(BD公司,批号:6036848);CD54同型对照FITC标记小鼠源IgG1(DAKO公司,批号:20027873);阳性对照:2,4-二硝基氯苯(2,4-dinitrochlorobenzene,SIGMA公司,规格:10 g·ml-1);阴性对照:乳酸(SIGMA公司,批号:WXBC2377V,规格:每瓶500 g)。
健康豚鼠,每批6只,共计30只。动物来源:余姚市泗门镇建飞实验兔养殖场,生产许可证号:SCXK(浙)2017-0002。
2.1.1 样品浓度的确定 用RPMI-1640作为溶剂,从原液起依次向下稀释8个剂量:原液、原液1/2体积、原液1/4体积、原液1/8体积、原液1/16体积、原液1/32体积、原液1/64体积、原液1/128体积。再用RPMI-1640作为溶剂,将每个剂量进行1∶50倍稀释,制成工作液。采用流式细胞仪检测PI染色阴性的活细胞数计算细胞成活率,计算公式如下:细胞成活率=活细胞数/总收获的细胞数×100%。
根据细胞成活率的计算结果得到剂量毒性log曲线,确定每种中药注射剂的CV75的值。CV75值即剂量毒性log曲线中相对细胞成活率为75%时选用的样品剂量。根据CV75值确定正式试验的8个剂量为:1.2×CV75,1×CV75,1/1.2×CV75,1/1.22×CV75,1/1.23×CV75,1/1.24×CV75,1/1.25×CV75,1/1.26×CV75。
2.1.2 试验步骤 将THP-1细胞以0.1×106~ 0.2×106·ml-1铺于培养瓶,预培养48~72 h后,以1×106·ml-1的密度铺于24孔板,加入样品接触24 h。收集上述细胞,PBS(含0.1%BSA)清洗,4 ℃封闭培养15 min。将细胞平均分成3份,加入FITC标记的抗CD86、抗CD54以及同型对照的单克隆抗体,4 ℃孵育30 min。流式细胞仪分析CD86和CD54的平均几何荧光强度(mean fluorescence intensity,MFI)。
2.1.3 结果分析 首先通过PI染色去除死细胞,收集约10 000个活细胞,分析细胞表面CD86和CD54的MFI。然后,采用以下公式计算相对荧光强度(relative fluorescence intensity,RFI),以表示细胞表面CD86和CD54的表达量:RFI=(样品处理细胞组MFI-样品处理细胞同型对照IgG的MFI)/(空白对照细胞组MFI-空白对照细胞同型对照IgG的MFI)。
2.1.4 判断标准 在细胞成活率>50%的情况下,每个化合物的至少2次独立试验任一个剂量的CD86的RFI等≥150,或者至少2次独立试验任一剂量的CD54的RFI≥200,则该化合物可判断为受试物阳性。
2.1.5 致敏阳性的剂量计算 致敏作用都与剂量相关,因此受试物致敏为阳性时,要进一步利用RFI通过公式计算有效作用浓度(effective concentration,EC),FITC-CD86用EC150表示,PE-CD54用EC200表示。
当受试物致敏阳性时,从最低浓度开始计算,满足阳性标准的第1个浓度设置为B浓度,选择B浓度的上一个浓度为A浓度:A浓度的RFI比第一个浓度的RFI值至少要高10%,否则要向上再取一个浓度的RFI值,直到符合>10%的标准。
若A浓度的RFI>150或200,B浓度的RFI<150或200,则:EC150=B剂量+{(150-BRFI)/ [(ARFI-BRFI)(A剂量-B剂量)]};EC200=B剂量+ {(200-BRFI)/[(ARFI-BRFI)(A剂量-B剂量)]}。
若A浓度和B浓度的RFI均>150或200,则:EC150=2^{Log2(B剂量)+(150-BRFI)/(ARFI-BRFI)×[Log2(A剂量)-Log2(B剂量)]};EC200=2^{Log2(B剂量)+(200-BRFI)/(ARFI-BRFI)×[Log2(A剂量)-Log2(B剂量)]}。
参照中国药典2015年版所示方法,取豚鼠6只,隔日每只每次腹腔注射供试品溶液0.5 ml,共3次,致敏。每日观察每只动物的行为和体征,首次致敏和激发前称量并记录每只动物的体质量。然后将其均分为2组,每组3只,分别在首次注射后第14天和第21天,静脉注射供试品溶液1 ml进行激发。观察激发后30 min内动物有无过敏反应症状。
静脉注射供试品溶液30 min内,不得出现过敏反应。如在同一只动物上出现竖毛、发抖、干咳、连续喷嚏3声、连续咳嗽3声、紫癜和呼吸困难等现象中的2种或2种以上,或出现二便失禁、步态不稳或倒地、抽搐、休克、死亡现象之一者,判定供试品不符合规定。
首先对4种不同中药注射剂进行毒性试验,利用PI染色得到的活细胞进行流式分析,得到毒性剂量曲线,根据毒性剂量曲线计算得到每种中药注射剂的CV75,见表2。结果表明,除参麦注射液的CV75值为0.5体积比,其余丹参注射液、香丹注射液和黄芪注射液体积比均为0.03体积比。
根据预试验得到4种中药注射剂的CV75值,进行8个剂量的正式试验。用流式细胞仪分析每种中药注射剂的平MFI。根据RFI计算公式得到4种中药注射剂的CD86RFI和CD54RFI值。4种中药注射剂的CD86RFI都<150而CD54RFI都<200,见图1。因此按判定标准结果为阴性。
在过敏反应试验中,4种中药注射剂和阴性对照组豚鼠在第14天和第21天激发后均未观察到过敏反应症状,因此判定为阴性。
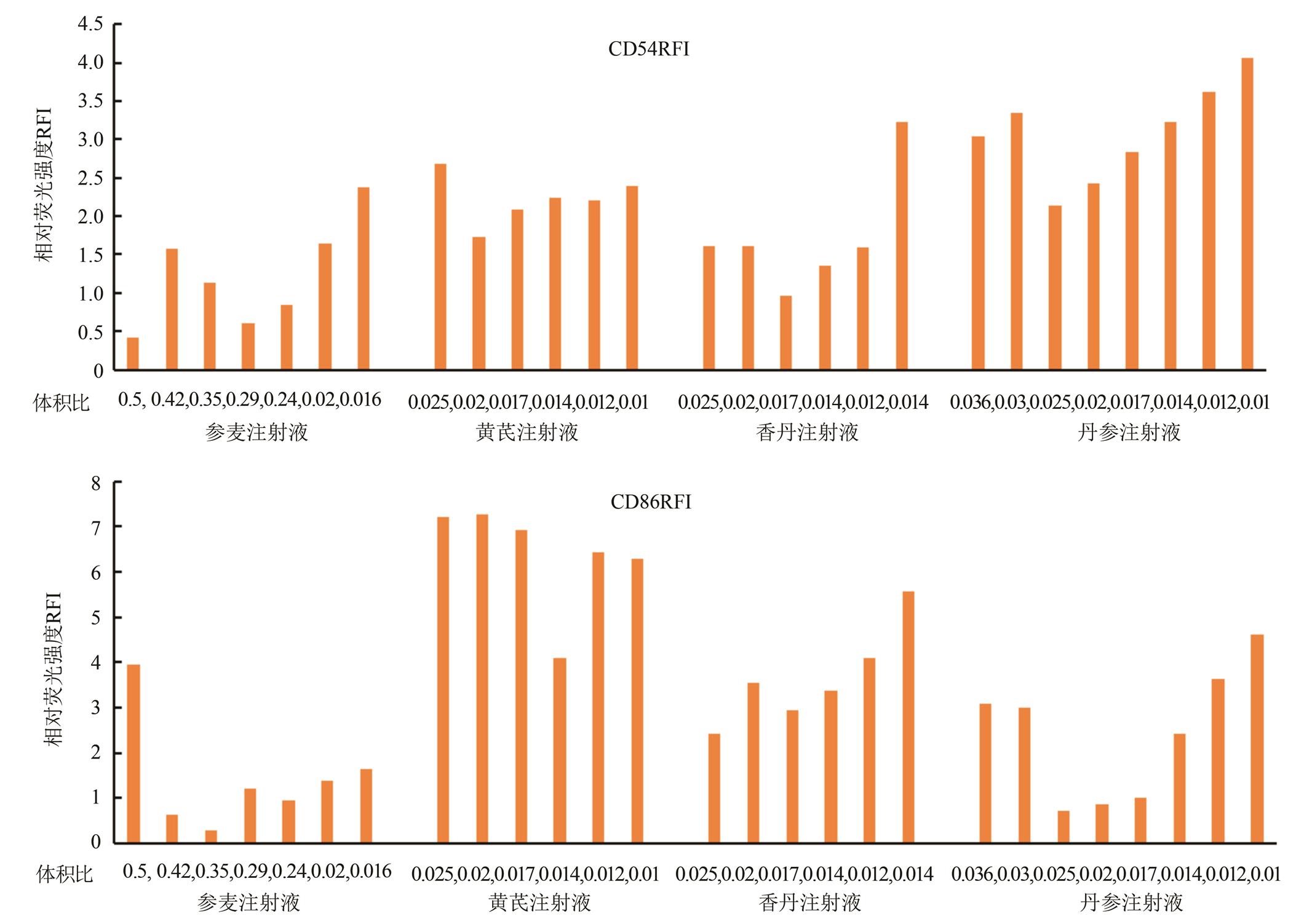
图1 4种中药注射剂CD54和CD86的RFI比较
Fig. 1 Comparison of the relative fluorescence intensity of CD54 and CD86 for 4 Chinese medicine injection
表2 4种中药注射剂体外过敏反应和体内过敏反应结果的比较(n=3,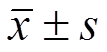 )
)
Tab.2 Comparison of the results for 4 Chinese medicine injection in sensitization tests in vitroandin vivo(n=3,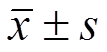 )
)

对体外人源细胞激活试验法和体内过敏反应试验法的优缺点进行比较,见表3。体外体内2种方法对中药注射剂的过敏反应结果的比较表明,中国药典2015年版以豚鼠为受试动物的体内方法,存在使用动物多(每组至少6只豚鼠);试验周期时间较长(至少需要21 d)、与人的过敏反应差异大(豚鼠和人对过敏原的反应有差异,可能造成假阳性和假阴性的结果),最终评价主观(结果由主观打分来进行判定)等问题。而体外过敏反应试验周期短(正式试验2~3 d),没有动物损耗,评价结果客观(根据流式细胞测定的相对荧光强度RFI来确定,不受主观因素的影响),灵敏性高。体外试验对操作人员技术要求高,由于灵敏度高,可能存在假阳性的可能。由于体外方法只能部分反映过敏的过程,因此需要结合其他体外方法进行最终判定。
表3 体外试验和体内试验优缺点的比较
Tab. 3 Comparison of advantages and disadvantages between sensitization testin vitroandin vivo

中国药典2015年版仍以传统的体内试验评价对中药注射剂的过敏反应。该方法使用动物多,周期长,且评价主观,灵敏度低,假阳性反应时有发生。而在国际倡导3R原则的大背景下,越来越多的体外方法以周期短,评价灵敏客观,操作简便,材料易获取等优点受到重视。根据中药注射剂引起的变态反应机制不同,主要分为Ⅰ型(速发型)、Ⅱ型(细胞毒型)、Ⅲ型(免疫复合物型)和Ⅳ(迟发型)变态反应。由于中药注射剂引起的Ⅳ型迟发过敏反应发病速度缓慢,出现症状不明显,目前药物的体外致敏检测方法多根据Ⅰ型和类过敏反应设计,如肥大细胞脱粒试验,体外补体激活试验[4-6]。而对Ⅳ型药物迟发变态反应检测方法的研究还处在空白阶段,因此找到一种针对Ⅳ型药物迟发变态反应设计的体外过敏试验是尤为必要的。
人源细胞激活试验作为2016年收录到OECD指南中的一种国际上公认的过敏体外测试方法正是针对Ⅳ型药物变态反应机制设计的。有研究表明,当Ⅳ型药物变态反应发生时,机体的非成熟型树突状细胞(immature dendritic cells,iDCs),也就是朗格汉斯细胞(Langerhans cells,LCs),能够将致敏物质识别,经过加工处理,并呈递给T淋巴细胞,启动特异性的免疫应答。在此过程中,iDCs分化为成熟的树突状细胞,并上调一系列细胞表面分子的表达,包括共刺激分子如CD80,CD86以及CD40,黏附分子如CD2,CD54,CD58等。人细胞激活试验就是利用检测DC样细胞系接触化学物后的激活状态,以树突状细胞表面分子CD86和CD56的表达变化作为判断致敏性的标准。目前该方法主要用于化妆品的体外测试中[7-9]。
本研究将人细胞激活试验法应用在中药注射剂Ⅳ型药物过敏反应的体外的研究上。通过对4种中药注射剂的体外过敏反应的测定,丹参注射液、香丹注射液、参麦注射液和黄芪注射液的相对荧光强度CD86RFI都<150而CD54RFI都<200,因此根据判定标准结果均为阴性,与体内豚鼠过敏反应结果一致。此外,针对中药注射剂特有成分复杂等特点,体外人源细胞激活试验法可通过CD54,CD86等一系列表面蛋白的表达进一步区分不同中药注射剂进行致敏潜在风险的比较。在流式细胞仪检测CD54和CD86的特异性表达峰,可见不同的中药注射剂CD86和CD54相对于同型对照的表达峰也有明显差异,见图2。丹参注射剂CD86和CD54的表达峰与同型对照基本重合,说明1#受试物在该体系中无致敏潜力,而黄芪注射剂的CD86和CD54的表达峰明显高于同型对照峰,说明该2#中药注射剂有一定的潜在的致敏风险。CD86和CD54的表达峰差异为不同中药注射剂的过敏反应进一步进行区分提供了可能。
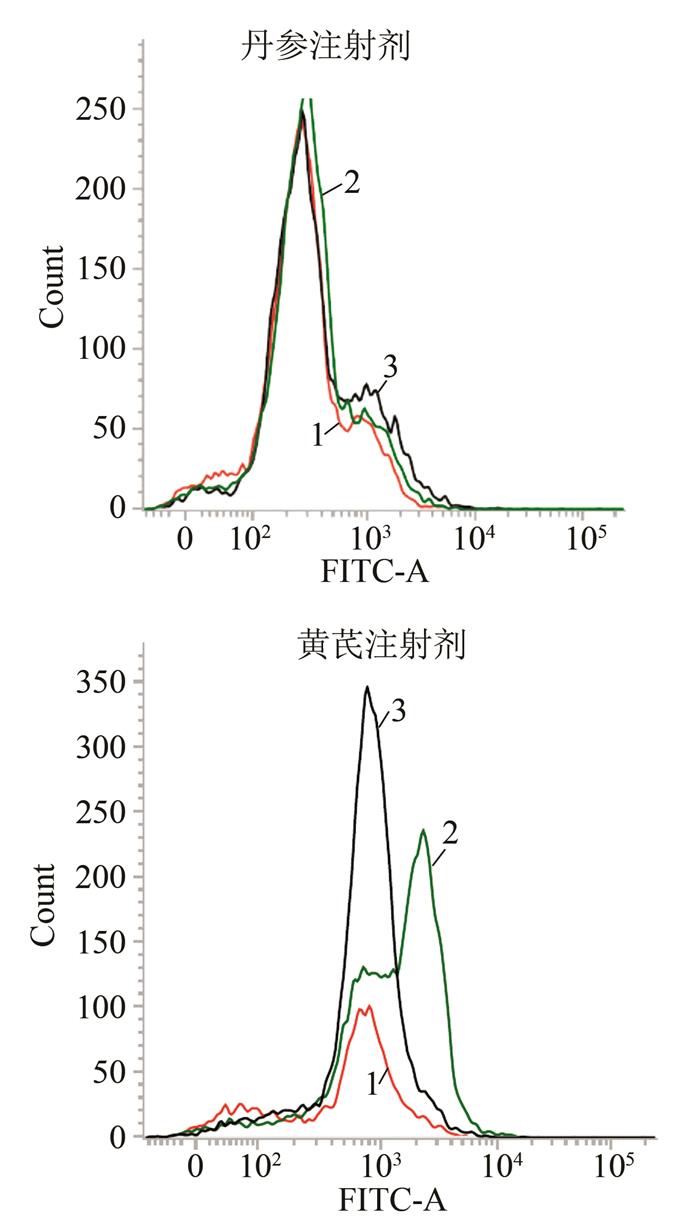
图2 2种不同成分的中药注射剂几何荧光强度值比较
曲线1为FITC标记的IgG同型对照,曲线2和3分别为FITC标记的CD86和CD54的标记的FITC几何荧光强度。
Fig. 2 Comparison of the geometric fluorescence intensity of CD54 and CD86 for 4 Chinese medicine injections
curve 1 is geometric fluorescence intensity of IgG-FITC, curve 2 is the geometric fluorescence intensity of CD86-FITC, curve 3 is geometric fluorescence intensity of CD54-FITC.
总之,通过体外人源细胞激活试验法对4种中药注射剂过敏反应检查的评价,发现针对Ⅳ型药物变态反应的人细胞激活试验应用到中药注射剂的致敏性的评价是可行的,这为中药注射剂初步快速检测提供了依据,同时为研究方法处在空白阶段的药品Ⅳ型药物变态反应检测的研究提供了一种新的思路。
REFERENCES
[1] 中国药典. 四部[S]. 2015: 1148
[2] In Vitro Skin Sensitisation, OECD Guidelines for the Testing of Chemicals, Section 4 Health Effects No. 442E [S]. 2016.
[3] Zhang J s, Sang J, Sun Y d, The Application of Direct Peptide Reactivity Assay for Sensitization Prediction of Chinese Medicine Injection [J]. Drug Standards of China, 2016, 17(4): 268-271.
[4] KANG R X, YOU R L, WANG R, e tal.In vitroexperiment of allergic reactions induced by traditional Chinese medicine injections [J]. China J Chin Mater Med(中国中药杂志), 2015, 40(13): 2503-2507.
[5] Azam P, Peiffer J L, Chamousset D, et al. The cytokine-dependent MUTZ-3 cell line as an in vitro model for the screening of contact sensitizers [J]. Toxicol Appl Pharmacol, 2006, 212(1): 14-23.
[6] ZHAO Y, LI Q, ZHANG X Y Study progress of type Ⅰ anaphylaxis reaction and anaphylactoid reaction on the basis of RBL-2H3 cell models [J]. ChinJ Clin Pharmacol Ther(中国临床药理学与治疗学), 2010, 15(11): 1310-1315.
[7] Ashikaga T.Development of anin vitroskin sensitization test (human Cell Line Activation Test; h-CLAT) using THP-1 cell (human monocytic leukemia cell line) [J]. Alternatives to Animal Testing & Experimentation Aatex, 2006, 11.
[8] Sakaguchi H, Ashikaga T, Miyazawa M, et. al Development of anin vitroskin sensitization test using human cell lines; human Cell Line Activation Test (h-CLAT) [J], Toxicol in Vitro, 2006, 20(5):774-784
[9] Sakaguchi H, Ashikaga T, Miyazawa M, et al.The relationship between CD86/CD54 expression and THP-1 cell viability in anin vitroskin sensitization test--human cell line activation test (h-CLAT) [J]. Cell Biol Toxicol, 2009, 25(2): 109-126.
(本文责编:曹粤锋)
Study on the Application ofin VitroHuman Cell Line Activation Test with Chinese Medicine Injection
Sang Jing, Chen Shuhuai, Meng Hong, Xie Zhen, Kuang Rong
*(Zhejiang Institute for Food and Drug Control, Hangzhou 310004, China)
ABSTRACT: OBJECTIVETo evaluate the possibility of allergic response test for Chinese medicine injections using human cell line activation testin vitro, and to explore the feasibility ofin vitrotest of type Ⅳ allergy reaction for traditional Chinese medicine injection.METHODSIn terms of OECD Guideline 442E, 4 different Chinese medicine injections were tested both in human cell line activation test with human leukemia THP-1 cellsin vitroand allergic responsein vivoat the same time.RESULTSFrom the result ofin vitroskin sensitization test, relative fluorescence intensity of specific surface antigen of dendritic cells CD86 was below 150 and CD54 below 200, which was negative according to the criteria. The results was the same asin vivotest.CONCLUSION In vitrotest has its advantages of short cycle, relatively simple and objective, and is a good alternative method for allergic response test for Chinese medicine injections.
KEY WORDS:human cell line activation test(h-CLAT); skin sensitization; alternative methods
中图分类号:R285.5
文献标志码:A
文章编号:1007-7693(2018)07-0975-05
DOI:10.13748/j.cnki.issn1007-7693.2018.07.006
引用本文:桑晶,陈舒怀,蒙宏,等. 人源细胞激活试验法应用于中药注射剂过敏反应检查的研究[J]. 中国现代应用药学, 2018, 35(7): 975-979.
基金项目:浙江省药品接触材料质量控制研究重点实验室(2014E10006)
作者简介:桑晶,女,博士,主管药师 Tel: (0571)86457970 E-mail: oliver169@163.com
*通信作者:匡荣,男,主任药师 Tel: 13989899796 E-mail: kuangrong@zjyj.org.cn
收稿日期:2017-11-29