
图1 痹痛消巴布膏中桑寄生和红花的TLC鉴别色谱图
詹强1,陈红梅1,俞忠明2,王娜妮2
(1.杭州市中医院,杭州 310007;2.浙江省中医药研究院,杭州 310007)
摘要:目的建立痹痛消巴布膏的质量标准。方法按照中国药典一部规定,进行薄层色谱鉴别和含量测定研究。以槲皮素为指标,建立桑寄生的鉴别方法;以红花药材为对照,建立红花的鉴别方法;以丹酚酸B为指标,建立丹参的HPLC含量测定方法。结果采用甲醇-水提取,酸水解,以甲苯(水饱和)-乙酸乙酯-甲酸(5∶4∶1)为展开剂,可鉴别巴布膏中的桑寄生;采用80%丙酮溶液提取,以乙酸乙酯-甲酸-水-甲醇(7∶2∶3∶0.4)为展开剂,可鉴别巴布膏中的红花。在Diamonsil C18色谱柱(250 mm×4.6 mm,5mm),以甲醇-乙腈(3∶1)为有机相(A),1.7%甲酸水溶液为水相(B),A∶B= 30%∶70%等度洗脱,流速1.0 mL·min-1,柱温30 ℃,进样量10 μL,检测波长286 nm条件下,巴布膏中丹酚酸B能有效分离,方法学考察符合含量测定要求。结论建立的质量标准能够用于痹痛消巴布膏的质量控制。
关键词:痹痛消巴布膏;质量标准;桑寄生;红花;丹参;高效液相色谱法
痹痛消巴布膏为笔者多年临床实践的经验方,目前已申请国家发明专利,它具有补益肝肾、强筋壮骨、活血化瘀、通络止痛之功效。方中独活、桑寄生补肝肾,强筋骨,祛风湿[1-2],为君药。细辛、丹参、当归协助君药发挥补气生血,通经络,除风湿,散瘀消肿之功效[3-4],为臣药。川芎、红花、乳香、没药皆能止痛,消肿,生肌,以上诸药合为佐药。芥子辛散功窜,消皮里膜外之痰[5],使药直达病所,故为使药。诸药合理配伍,标本兼治。巴布膏剂的质量控制指标一般包括含膏量、黏附性、药物成分含量等[6-7]。痹痛消巴布膏君药独活中含有二氢欧山芹醇当归酸酯、蛇床子素等主要成分,桑寄生中含有槲皮苷等黄酮类成分;丹参中含有丹酚酸B等酚酸类成分及丹参酮成分;红花中含有红花黄色素等有效成分,可作为痹痛消巴布膏的定性及定量指标。由于巴布膏以水溶性高分子为基质,为了使药材提取物与基质相容,药材的提取以极性溶剂为主。前期对含量测定指标进行选择,发现臣药丹参中的丹酚酸B含量较高,可作为含量测定指标。
本研究针对痹痛消巴布膏制备工艺及剂型特点,按照中国药典2015年版一部规定,开展质量标准研究,确定了桑寄生、红花的薄层鉴别方法,建立了丹参中丹酚酸B的HPLC含量测定方法[8],期望为痹痛消巴布膏的质量标准制定和制剂研发提供实验依据。
TLC scanner3薄层色谱扫描仪(瑞典卡玛);LC-20A vp高效液相色谱仪、SPD-20A UV检测器(日本岛津);METELLER电子分析天平(瑞士梅特勒)。槲皮素对照品(批号:100081-200406;纯度>99%)、丹酚酸B对照品(批号:111562-2003,纯度>99%)、红花对照药材均购自中国食品药品检定研究院;甲醇、乙腈为色谱纯,水为去离子水,其余均为分析纯。痹痛消巴布膏由浙江省中医药研究院中药中心制备,批号:151020,151025,151029,151103。
2.1.1 桑寄生 取痹痛消巴布膏膏体25 g,加甲醇-水(1.2︰1)100 mL,加热回流1 h。趁热滤过,滤液浓缩至约20 mL,加水10 mL,再加稀硫酸约0.5 mL,煮沸回流1 h,放冷,用乙酸乙酯振摇提取2次,每次30 mL,合并乙酸乙酯提取液,浓缩至1 mL,作为供试品溶液。另取槲皮素对照品,加乙酸乙酯制成每1 mL含0.5 mg的溶液,作为对照品溶液。照薄层色谱法(中国药典2015年版通则0502)试验,吸取供试品溶液和对照品溶液各10 μL,分别点于同一0.5%氢氧化钠溶液制备的硅胶G薄层板上,以甲苯(水饱和)-乙酸乙酯-甲酸(5∶4∶1)为展开剂,展开,取出,晾干,喷以5%三氯化铝乙醇溶液,置紫外光灯(365 nm)下检视,见图1A。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。缺味样品无干扰。
2.1.2 红花 取本品膏体约10 g,精密称定,加硅藻土研磨混合,加80%丙酮溶液10 mL,密塞,振摇15 min,静置,取上清液,作为供试品溶液。另取红花对照药材0.5 g,加80%丙酮溶液5 mL,密塞,振摇15 min,静置,取上清液制成对照药材溶液。照薄层色谱法(中国药典2015版通则0502)试验,吸取上述2种溶液各5 μL,分别点于同一硅胶H薄层板上,以乙酸乙酯-甲酸-水-甲醇(7∶2∶3∶0.4)为展开剂,展开,取出,晾干。如图1B所示,供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。缺味样品无干扰。

图1 痹痛消巴布膏中桑寄生和红花的TLC鉴别色谱图
A-桑寄生;B-红花;1-痹痛消巴布膏;2-缺桑寄生;3-槲皮素;4-缺红花;5-痹痛消巴布膏;6-红花对照药材。
Fig. 1 TLC identification ofTaxillus chinensisandCarthamus tinctoriusin Bitongxiao cataplasm
A-Taxillus chinensis; B-Carthamus tinctorius; 1-Bitongxiao cataplasm; 2-sample lack ofTaxillus chinensis;3-quercetin; 4-sample lack ofCarthamus tinctorius;5-Bitongxiao cataplasm; 6-Carthamus tinctorius (reference).
2.2.1 色谱条件 色谱柱为Diamonsil C18柱(250 mm×4.6 mm,5 μm),流动相为有机相A:甲醇-乙腈(3∶1);水相B:1.7%甲酸水溶液;A∶B= 30%∶70%,柱温30 ℃,进样量10 μL,检测波长286 nm。
2.2.2 对照品溶液制备 取丹酚酸B对照品,精密称定,加75%甲醇制成1 mL含丹酚酸B 0.155 mg的对照品溶液。
2.2.3 供试品溶液的制备 取痹痛消巴布膏膏体约10 g,精密称定,加2倍硅藻土研磨,使膏体分散均匀,精密加入75%甲醇50 mL,超声提取1 h,称重,用75%甲醇补充损失质量,过滤,取续滤液,作为供试品溶液。
2.2.4 缺味供试品溶液的制备 按照痹痛消巴布膏处方中药材比例,取除丹参外的其余药材,制得缺丹参的痹痛消巴布膏,按照“2.2.3”项下方法制得缺丹参供试品溶液。
2.2.5 方法专属性考察 取对照品溶液,供试品溶液及缺味供试品溶液,按照“2.2.1”项条件测定,色谱图见图2,表明在上述色谱条件下,巴布膏中其他成分对丹酚酸B没有干扰,含量测定方法符合专属性要求。
2.2.6 方法学考察
2.2.6.1 工作曲线及线性范围 取“2.2.2”项下对照品溶液,稀释成梯度浓度,对丹酚酸B的系列对照品溶液进行测定,以峰面积(y)对丹酚酸B的质量浓度(x,mg·mL-1)进行线性回归,得到线性方程y=191.2x+0.022 7(R²=0.999 9),表明丹酚酸B在0.011~0.110 mg·mL-1内,与峰面积呈良好线性关系。
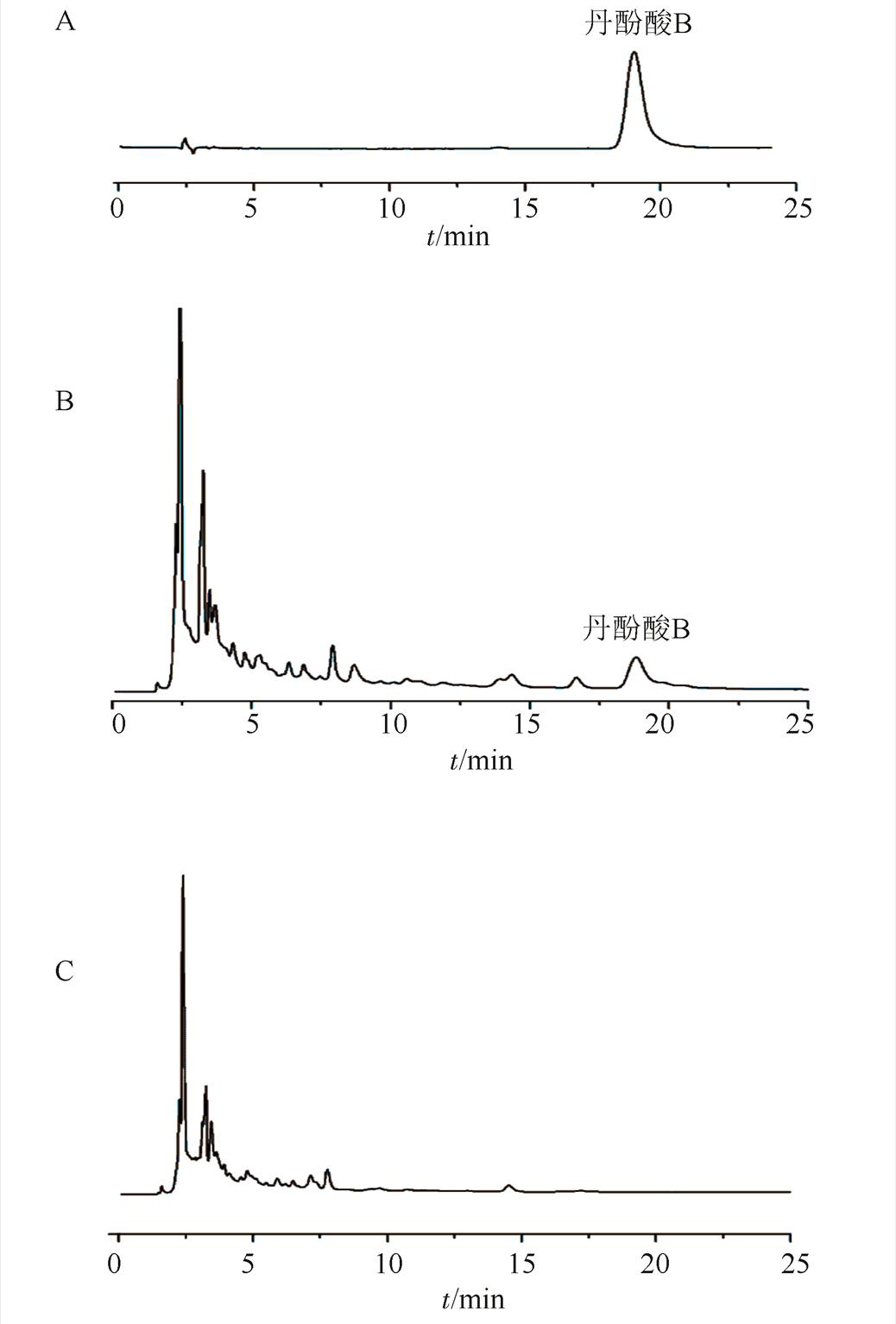
图2 痹痛消HPLC色谱图
A-丹酚酸B对照品;B-痹痛消巴布膏;C-缺丹参样品。
Fig. 2 HPLC chromatogram of Bitongxiao cataplasm
A-standard substance; B-sample of Bitongxiao cataplasm; C-sample lack ofSalvia miltiorrhiza.
2.2.6.2 仪器精密度试验 取“2.2.3”项下同一供试品溶液,按“2.2.1”项色谱条件,连续进样6次,记录丹酚酸B的峰面积,RSD为2.01%。
2.2.6.3 稳定性试验 取“2.2.3”项下同一供试品溶液,在0,2,4,8,12,24 h,按“2.2.1”项色谱条件进样测定,记录丹酚酸B的峰面积,RSD为1.45%。
2.2.6.4 重复性试验 取批号为151020的痹痛消巴布膏样品6份,按照“2.2.3”项供试品溶液制备方法操作,制得供试品溶液,按照“2.2.1”项色谱条件测定,记录丹酚酸B的峰面积,计算含量,RSD为2.52%。
2.2.6.5 加样回收率试验 取已知含量的痹痛消巴布膏9份,每份约5 g,按高、中、低比例,每组3份,分别精确加入丹酚酸B对照品,按照“2.2.3”项供试品溶液制备方法,制得供试品溶液,按“2.2.1”项色谱条件进样测定,丹酚酸B的平均加样回收率为101.32%,RSD为2.26%。
2.2.7 样品测定 取痹痛消巴布膏,按照“2.2.3”项供试品溶液制备方法操作,另取“2.2.2”项下对照品溶液,按“2.2.1”项下色谱条件进行测定,样品测定结果见表1。
表1 痹痛消巴布膏中丹酚酸B含量测定结果(n=3)
Tab. 1 Content determination results of salvianolic acid B in Bitongxiao cataplasm(n=3)

痹痛消巴布膏的鉴别研究中,曾经以二氢欧山芹醇当归酸酯、蛇床子素等指标,摸索了独活的鉴别条件;以阿魏酸等为指标,摸索了当归的鉴别条件;以细辛脂素为指标,摸索了细辛的鉴别条件;以欧当归内酯A和川芎嗪等为指标,摸索了川芎的鉴别条件;以芥子碱硫氰酸盐为指标,摸索了芥子的鉴别条件,均未获得满意结果。分析原因,首先是痹痛消巴布膏的药材组成较为复杂,其中部分药材在处方中用量较小,指标成分经提取后有所损失,导致含量过低,无法鉴别;其次是巴布膏采用的是水溶性基质,因而前期药材提取以水煎煮提取为主,上述指标成分有较多为脂溶性成分,无法充分提取。最终本研究确定了君药桑寄生和佐药红花的鉴别方法。
桑寄生中含有槲皮苷等黄酮类成分,槲皮素为槲皮苷经水解后的苷元。而独活、红花等药材中均含有黄酮苷成分。为了避免其他黄酮类成分干扰,对提取及水解的条件进行了比较,确定供试品提取溶剂中甲醇-水的比例,并进一步优化了薄层色谱条件,最终确定本研究中的鉴别条件。在该条件下,能够鉴别痹痛消巴布膏中桑寄生里的槲皮素,缺桑寄生样品无干扰。
丹酚酸B的含量测定研究较多,项目组曾经开展了复方制剂中丹酚酸B的含量测定研究[9],在前期建立方法的基础上,优化了色谱条件。由于巴布膏膏体黏稠,指标成分难以溶出,因此在供试品溶液制备时,加入了2倍量硅藻土研磨,使膏体疏松并分散均匀,有助于后续的成分提取。对提取溶剂、提取时间分别进行考察,结果显示75%甲醇提取效率高,杂质干扰少,超声提取1 h内随着提取时间的延长,提取率明显增高,1~1.5 h提取率基本趋于稳定,1.5 h后提取率下降。
巴布膏作为新型的外用制剂,具有载药量大、贴敷舒适度高等优点[10],中药巴布膏的研制具有临床应用价值及开发前景,质量控制研究是其中重要的内容。本实验总结的质量标准研究,能够为痹痛消巴布膏的质量标准制订提供客观依据。
REFERENCES
[1] ZHOU G, MA B H. The development on the study of Radix Angelicae Pubescentis [J]. China Mod Med(中国当代医药), 2012, 19(16): 15-16.
[2] SU B W, ZHANG X J, ZHU K X, et al. Optimization of extraction technology of quercitrin fromTaxillus chinensis[J]. Chin J Exp Tradit Med Form(中国实验方剂学杂志), 2013, 19 (2): 8-10.
[3] WANG X L, JIN L J, XU F X, et al. Research progress of Chinese herb-asarum [J]. Asia-pac Tradit Med(亚太传统医药), 2013, 9(7): 68-71.
[4] 李曦, 张丽宏, 王晓晓, 等. 当归化学成分及药理作用研究进展[J]. 中药材, 2013, 36(6): 1023-1028.
[5] 崔国静, 孙欢欢. 芥子的鉴别及炮制应[J]. 首都医药, 2014, 21(11): 44.
[6] 刘明海. 近年国内巴布剂体外透皮性能研究现状及进展[J]. 中成药, 2011, 33(6): 1033-1036.
[7] HU Y H, LIU A Q, LI J, et al. Study on the matrix of Chinese medicine patcher [J]. Med Recap(医学综述), 2012, 18(13): 2093-2096.
[8] 中国药典. 一部[S]. 2015: 76-77.
[9] SHOU D, YU Z M, LI Y P, et al. Determination of salvianolic acid B in Fuben Zengmai granules by high performance liquid chromatography with direct current amperometric detection [J]. Chin J Tradit Chin Med Pharm(中华中医药杂志), 2012, 27(1): 234-237.
[10] DU L N, ZHU W N, LIU X Y, et al. Preparation,in vitroandin vivoevaluation of cataplasm of white mustard seed varnish to prevent asthma [J]. China J Chin Mater Med(中国中药杂志), 2014, 39(23): 4596-4602.
(本文责编:李艳芳)
Quality Standard Research of Bitongxiao Cataplasm
ZHAN Qiang1, CHEN Hongmei1, YU Zhongming2, WANG Nani2
(1.Hangzhou Hospital of Traditional Chinese Medicine, Hangzhou 310007, China; 2.Zhejiang Institute of Traditional Chinese Medicine, Hangzhou 310007, China)
ABSTRACT: OBJECTIVETo establish the quality standard of Bitongxiao cataplasm.METHODSWith the guide of Chinese Pharmacopoeia, research work for TLC identification and quantitative analysis was carried out. The TLC identification forTaxillus chinensisandCarthamus tinctoriuswas improved based on reference methods, quercetin and safflower medicinab materials were used as indexes and controls, respectively. The content ofSalvia miltiorrhizawas determined by HPLC with salvianolic acid B as an indictor.RESULTS Taxillus chinensiscould be identified with toluene(water saturation)-ethyl acetate-formic acid(5︰4︰1) as developing agent.Carthamus tinctoriuscould be identified by TLC method with ethyl acetate-formic acid-water-methanol(7︰2︰3︰0.4) as developing agent. The separation of salvianolic acid B had effective separation on the HPLC condition as followes: the Diamonsil C18column(250 mm×4.6 mm, 5 μm)with the mobile phase containing methanol and acetonitrile(3:1) as the organic phase(A), 1.7% formic acid aqueous solution as the water phase(B), A∶B=30%∶70% of elution, the flow rate was 1.0 mL·min-1, the temperature of column was 30 ℃, injection volume was 10 μL, and the detection wavelength was 286 nm. Methodological investigation accorded with the requirement of content determination.CONCLUSIONThe established quality standard of Bitongxiao cataplasm is suitable for the quality control.
KEY WORDS:Bitongxiao cataplasm; quality standard;Taxillus chinensis;Carthamus tinctorius;Salvia miltiorrhiza; HPLC
中图分类号:R927.11
文献标志码:B
文章编号:1007-7693(2018)07-1050-04
DOI:10.13748/j.cnki.issn1007-7693.2018.07.023
引用本文:詹强, 陈红梅, 俞忠明, 等. 痹痛消巴布膏的质量标准研究[J]. 中国现代应用药学, 2018, 35(7): 1050-1053.
基金项目:浙江省经贸委中药现代化专项(31)
作者简介:詹强,男,硕士,主任中医师 Tel: (0571)85827931 E-mail: zqtow@163.com
收稿日期:2017-10-31