地塞米松为常见的糖皮质激素,这种激素对轻度面部皮炎等病症会产生明显的效果,使用后皮肤很快变得光滑。但长期使用会产生激素依赖,引起全身的不良反应[1],我国和欧盟早就将其列为禁用物质[2-3]。2015年8月22日国家食品药品监督管理总局关于11批次面膜类化妆品不合格的通告(2015年第56号)中,通报11批次面膜类产品存在非法添加糖皮质激素[4]。由于微商等网络渠道化妆品的兴起与发展,化妆品市场的安全性无法有效保障。经临床和市场抽样发现,化妆品中激素的添加成为一个日趋严重的问题,地塞米松就是常见的添加物质之一。检测糖皮质激素一般用GB/T24800.2-2009所载方法[5],但是需要2次提取以及过柱净化,前处理过程繁琐,非常不适合大批量处理,对操作要求也高,难以得到准确的结果。目前的相关文献中,部分涉及液质条件的优化[6],不能解决主要矛盾;部分提出了一些用于检测的新仪器和新方法[7-8],普遍有通用性不强和方法不够稳定的缺点。实际检测需要更实用、高效、快速、稳定、简便的方法。
本实验通过查阅文献和反复试验,使用内标追踪和C18净化的办法,建立了一套便捷、高效、准确地测定化妆品中地塞米松的方法,并检测了大量实际样品,验证了方法的可靠性。
1 材料与方法
1.1 仪器与试剂
Agilent 6490-G1290QQQ型液质联用仪(美国Agilent);涡旋振荡仪(广州依科 MS3);MULTIFUGE X1热电高速离心机(美国热电);57044型固相萃取仪(美国 Suplelco);Genpure UV/UF型热电纯水仪(美国热电);MV5型自动浓缩仪(北京莱伯泰科仪器股份有限公司)。
地塞米松对照品(批号:100129-201105,含量:99.7%)和泼尼松对照品(批号:100199-201503,含量:99.6%)均购自中国食品药品检定研究院;乙腈、甲醇(色谱纯,默克公司);乙酸锌、氯化钠、亚铁氰化钾(分析纯,国药集团);Qasis HLB固相萃取小柱(3 mL/60 mg,Waters公司);面膜来源:市场购买。
1.2 方法
1.2.1 对照品溶液的配制 精密称取地塞米松和泼尼松对照品约 10 mg,分别用甲醇稀释至10.0 mL,分别作为对照品和内标储备液。
1.2.2 标准曲线 取地塞米松和泼尼松储备液各适量,用40%乙腈稀释,使地塞米松浓度为0.05,0.1,0.2,0.4,0.8,1.0 μg·mL-1,其中内标的浓度恒定为0.5 μg·mL-1,对照品与供试品进样量均为 1 μL。
1.2.3 样品前处理 方法一:称取上述供试品(初筛为阳性的面膜)约0.2 g,分别加入内标适量(保证内标终浓度为0.5 μg·mL-1),于10 mL具塞离心管中,加入3 mL饱和氯化钠,涡旋混匀,加入2 mL乙腈,混匀,涡旋提取2 min,5 000 r·min-1离心10 min,取上层清液加C18粉末100 mg振摇1 min,5 000 r·min-1离心5 min,取上清进样分析。
方法二:按GB/T 24800.2-2009,称取供试品(与方法一中样品相同)约0.2 g于10 mL具塞离心管中,加入3 mL饱和氯化钠溶液,涡旋混匀,加入2 mL乙腈,混匀,涡旋提取2 min,5 000 r·min-1离心10 min。吸取上清于另一50 mL具塞离心管中,下层溶液用2 mL乙腈重复提取一次,合并2次乙腈提取液,准确加入40 mL水,混匀,加入10%亚铁氰化钾溶液0.2 mL,混匀,加入20%乙酸锌溶液 0.2 mL,混匀,5 000 r·min-1离心 10 min,取上清液进行固相萃取。
Waters Oasis HLB固相萃取小柱预先依次用甲醇5 mL,水10 mL活化后,将提取液样品用滤纸过滤后流经小柱,待样品溶液流尽后,使用10%乙腈水溶液10 mL清洗。待清洗液流尽后,准确吸取甲醇4 mL淋洗小柱,收集洗脱液,收集完成后氮气吹干,准确加入5 mL 50%甲醇溶解,得供试品溶液。
1.2.4 液质条件 色谱条件:色谱柱 SB-C18(100 mm×2.1 mm,1.8 μm),柱温 35 ℃,流动相为甲醇-0.1%甲酸(90∶10),流速:0.2 mL·min-1。
质谱条件:电离源ESI,毛细管温度为300 ℃,鞘气流速为7 L·min-1,源压力3.5 kV,正离子模式,扫描方式为多反应监测模式;母离子为359(泼尼松)和 393(地塞米松),子离子为 147(359)、341(359)、355(393)和 147(393),其中 359>341 和393>355分别为泼尼松和地塞米松的定量离子对。
2 结果
2.1 2种方法结果的比较
方法一供试品的平均检测结果为20.15 mg·kg-1,方法二供试品的平均检测结果为 19.75 mg·kg-1,结果偏差为1.7%,表明用方法一后也能得到准确结果。方法二步骤非常繁琐,耗材较贵,不适合大规模的样品处理,选择优化方法一的方法。
2.2 线性关系
以相对峰面积(y)对相对浓度(x,μg·mL-1)绘制内标标准曲线,方程y=0.404 7x+0.004 6,线性范围为 0.2~10 μg·mL-1,相关系数为 0.999 8,线性关系良好。
2.3 精密度试验
以浓度为 0.5 μg·mL-1的对照品(加入内标使浓度为 0.5 μg·mL-1)平行进样 6 次,测定比值(对照品峰面积/内标峰面积),计算RSD为0.5%。
2.4 稳定性试验
取中水平加标样品分别于 0,2,4,8,12,16,24,32,48 h测定其比值(对照品峰面积/内标峰面积),RSD为2.7%,稳定性良好。
2.5 重复性试验
平行制备 6份同水平加标样品(加标水平为1 mg·kg-1)进行测定,结果分别为 1.06,1.08,1.06,1.05,1.03,1.09 mg·kg-1,RSD 为 2.0%,重复性良好。
2.6 空白试验
选空白样品按方法一处理,上机分析,目标物出峰处无干扰,空白专属性良好,见图1。
2.7 回收率试验
称样品 9份,做高中低 3水平加标试验,每个水平平行 3份,加标水平分别为 0.2,0.5,1.0 mg·kg-1,按方法一处理得结果,回收率为90%~110%,RSD<1.5%,结果见表 1。加标回收率典型图谱见图2。
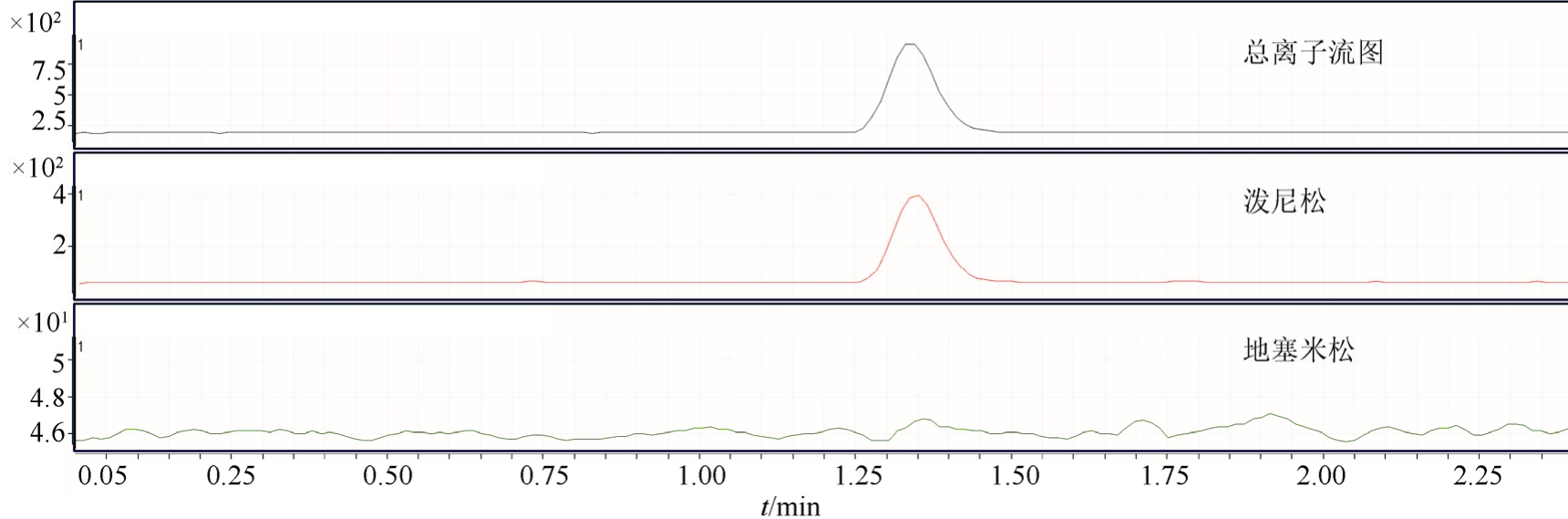
图1 空白样品典型图谱(总离子流图和提取离子流图)
Fig. 1 The typical chromatograms of blank sample (TIC and EIC)

图2 加标样品典型图谱(总离子流图和提取离子流图)
Fig. 2 The typical chromatograms of spiked sample (TIC and EIC)
表1 回收率测定结果
Tab. 1 The results of recovery test

2.8 检出限与定量限
称0.2 g空白样品,加入适当对照品,进行检出限和定量限试验,按照S/N=3和S/N=10分别计算得到检出限为0.005 mg·kg-1(S/N=3),定量限为0.2 mg·kg-1(S/N=10)。
2.9 实际样品检测
从市场上买来40批面膜样品,使用本方法检测,其中有 1批检出地塞米松,检出量为3.51 mg·kg-1,国标 GB/T 24800.2-2009 测试结果为3.48 mg·kg-1,偏差为0.4%,其余未检出结果一致。
3 总结与讨论
3.1 提取溶剂的选择
在提取试验阶段,采用甲醇、水、60%乙腈、40%乙腈、乙酸乙酯分别提取,发现甲醇、乙腈和乙酸乙酯提取效率不足 50%,60%和 40%乙腈水溶液乳化严重,离心和过滤都难以澄清,水提取发现杂质太多,难以净化,故仍然选择饱和氯化钠提取结合乙腈再次萃取的方式(饱和氯化钠可以和乙腈充分分层),效果良好。
3.2 净化条件的优化
采用C18、弗罗里硅土、PSA,各加入100 mg,其他实验过程相同,考察净化结果并比较,其中C18处理的回收率结果更接近 100%,弗罗里硅土和PSA的回收率结果在130%~140%之间,明显净化效果不好,故选择C18颗粒作为净化剂。
3.3 内标的选择
内标要选择一种结构类似、性质接近的物质,优化实验中曾经选取过倍他米松、氟米松、泼尼松、甲基泼尼松龙等糖皮质激素为内标,倍他米松离子对与地塞米松相同,不能区分,氟米松和甲基泼尼松龙作为内标,回收率<80%,综合考虑,选择泼尼松,与地塞米松结构类似,分子量接近且有区别,色谱行为类似,能明显地降低基质效应,且性质稳定,容易获得,实际试验效果良好。
3.4 LC-MS条件的选择
通过比较甲醇-甲酸,甲醇-甲酸铵,乙腈-甲酸,乙腈-甲酸铵体系,发现在甲醇-甲酸体系下这2种激素相应最佳,在90%的有机相条件下洗脱可大大缩短分析时间(2 min内出峰完成),提高效率且不影响结果的准确性,并通过 Agilent Masshunter Optimizer软件自动筛选定量及定性离子对,并对碰撞能量进行优化,得到多反应监测模式的实验条件,通过上述一系列的条件优化,实现快速准确地完成分析的目标。
泼尼松作为另一种糖皮质激素,与地塞米松结构类似,能够用泼尼松做内标,可以追踪实验全流程,简化提取净化过程,很好地规避提取过程的基质效应和损失,不需过柱和复溶,使过程大大简化,且不使用固相萃取柱和相关试剂,明显降低成本,实现对整体实验过程的全面优化,从而达到方便高效准确地分析面膜中地塞米松的目的。目前仅限于面膜基质,其他基质需要进一步优化和试验,但本研究为糖皮质激素的测定提供了一种新的思路,并为监管提高效率提供支持,前景广阔。
REFERENCES
[1] LU H G. Facial corticosteroid addictive dermatitis [J]. J Clin Dermatol, 2006, 35(10): 682-684.
[2] 化妆品安全技术规范[S]. 2015: 57.
[3] The Cosmetics Directive of the Council European Communities. 76/768/EEC [S]. 2008: 81.
[4] 国家食品药品监督管理总局. 国家食品药品监督管理总局关于11批次面膜类化妆品不合格的通告(2015年第56号)[EB/OL][2015-08-22]. http: //www.sda.gov.cn/WS01/CL0087/127700. html.
[5] GB/T 24800. 2-2009. Determination of 41 glucocorticoids in cosmetics by LC-MS-MS and TLC method [S]. 2009: 1-19.
[6] ZHAO X Y, LIN Y F, HU X Z et al. Determination of 9 glucocorficoids in cosmetics by reversed-phase high performance liquid chromatography [J]. Chin J Anal Lab(分析试验室), 2009, 28(2): 111-115.
[7] OU B L, ZHAO J L, ZOU Y, et al. Simultaneous determination of 16 glucocorticoids added in Chinese patent medicine and health products by HPLC [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2016, 33(9): 1178-1182.
[8] LIU F K, CHANG Y C. Using thiol-capped gold nanoparticlesin the background solution of MEKC to concentrateand separate neutral steroids [J]. Chromatographia,2010, 72(11/12): 1129-1135.