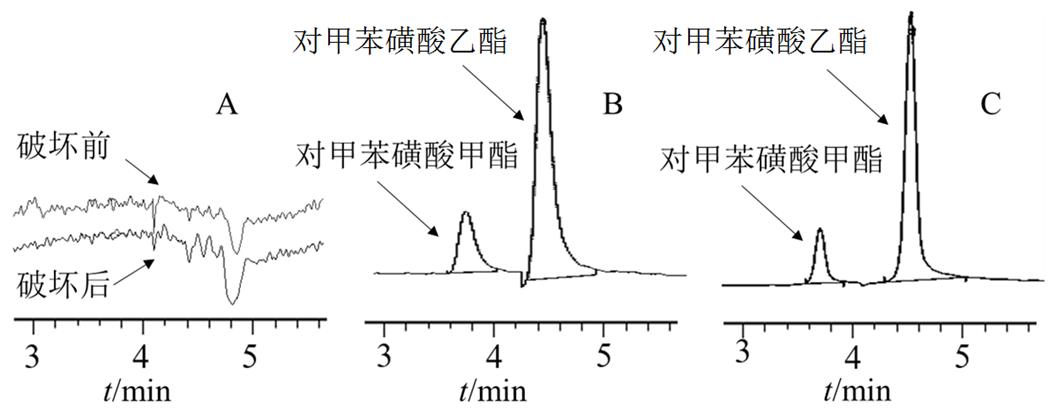
图1 专属性试验代表性图谱
芦飞1,邢珊珊1,王咏2*
(1.仙居县人民医院,浙江 台州 317300;2.浙江仙琚制药股份有限公司,浙江 台州 317300)
摘要:目的建立醋酸甲羟孕酮中的基因毒性杂质对甲苯磺酸甲酯及对甲苯磺酸乙酯的LC-MS检测方法。方法采用XDB-C18(50 mm×4.6 mm,1.8 μm)色谱柱;10 mmol·L-1醋酸铵(氨水pH 7.0)-乙腈为流动相;质谱:正离子模式,检测离子m/z187.1,201.1。结果对甲苯磺酸甲酯和对甲苯磺酸乙酯在0.05~5.08mg·mL-1内线性关系良好。对甲苯磺酸甲酯定量限为0.1 ng,检测限均为0.05 ng;对甲苯磺酸乙酯定量限为0.03 ng,检测限为0.02 ng;对甲基苯磺酸甲酯平均回收率101.6%,RSD 为3.46%;对甲基苯磺酸乙酯平均回收率98.7%,RSD 为2.22%。结论本方法适用于样品醋酸甲羟孕酮中对甲基苯磺酸甲酯和对甲基苯磺酸乙酯的检测。
关键词:醋酸甲羟孕酮;对甲苯磺酸甲酯;对甲苯磺酸乙酯;基因毒性杂质;LC-MS
醋酸甲羟孕酮又名安宫黄体酮,广泛应用于月经不调、功能性子宫出血、先兆流产或习惯性流产等症状,注射剂可用作长效避孕药,大剂量用于治疗乳腺癌、肾癌等,对肿瘤进行化疗时,有保护骨髓、减轻消化反应,抑制人结肠癌LS1747T细胞等作用[1]。在醋酸甲羟孕酮原料药合成过程中使用对甲苯磺酸、甲醇、乙醇等可能会生成基因毒性杂质对甲苯磺酸甲酯和对甲苯磺酸乙酯,须严格控制其毒理学关注阈值(threshold of toxicological concern,TTC)[2-3]。人用药品注册技术要求国际协调会(ICH)发布的M7(毒性杂质评估与控制)中规定,可以以TTC控制基因毒性杂质,TTC 为1.5 μg·d-1(相当于十万分之一的患癌风险)[4],醋酸甲羟孕酮制剂用于抗肿瘤治疗最大日给药剂量为1 000 mg,因此需要将对甲苯磺酸甲酯、对甲苯磺酸乙酯在醋酸甲羟孕酮原料药中含量控制在1.5 μg·g-1以下。基因毒性杂质限量要求极低,相关研究多采用液相或气相质谱联用等技术检测,如梁键谋等[5]利用LC-MS/MS 技术建立了草酸右旋西酞普兰中对甲苯磺酸酯类基因毒性杂质的检测方法,李靖坤等[6]研究了用气相色谱-质谱联用法对吉非替尼中对苯磺酸酯类(对甲苯磺酸甲酯、对甲苯磺酸乙酯、对甲苯磺酸异丙酯)的含量检测方法。液相单四级杆质谱在购买及维护成本、操作简便程度等方面相对串联质谱等大型质谱均有较大优势,在重复检测稳定性方面比气相质谱联用好,对样品要求较低,在医药科研院所及企业普及度很高,并已成为广泛用于产品中微量杂质检测放行的标准方法。本研究建立了醋酸甲羟孕酮中对甲苯磺酸甲酯、对甲苯磺酸乙酯的LC-MS检测方法,无需内标、样品进样浓度高,相对含量检测灵敏度高,可为用药安全提供有力保障。
1200高效液相色谱仪,6120 质谱检测器(美国安捷伦公司); XDB-C18(50 mm×4.6 mm,1.8 μm)色谱柱(安捷伦公司);BP211D十万分之一电子天平(德国赛多利斯公司)。
醋酸甲羟孕酮(药用级,浙江仙琚制药股份有限公司,批号:X2-110823);对甲基苯磺酸甲酯(上海阿拉丁生化科技股份有限公司,批号:F1012054;纯度:98.0%);对甲苯磺酸乙酯(上海阿拉丁生化科技股份有限公司,批号:E1012037;纯度:98.0%);乙腈、二氯甲烷为色谱纯;其他试剂均为分析纯,去离子水。
2.1.1 稀释剂 乙腈、二氯甲烷的1∶1混合溶液。
2.1.2 对照品储备液的制备 精密称取对甲基苯磺酸甲酯、对甲基苯磺酸乙酯各约20 mg,置20 mL量瓶中,并用稀释剂稀释到刻度,混合均匀后精密量取1.0 mL置100 mL量瓶中,用稀释剂稀释到刻度,混合均匀,作为杂质对照品储备液。
2.1.3 对照品溶液的制备 精密量取杂质对照品储备液5.0 mL置20 mL量瓶中,并用稀释剂稀释至刻度,混合均匀,即得。
2.1.4 供试品溶液的制备 精密称取约200 mg醋酸甲羟孕酮样品置1 mL量瓶中,并用稀释剂稀释至刻度,混合均匀,即得。
2.2.1 色谱条件 色谱柱XDB-C18(50 mm× 4.6 mm,1.8 μm);柱温:30 ℃;流动相:10 mmol·L-1醋酸铵(氨水pH 7.0)(A)-乙腈(B),梯度洗脱(0~ 8 min,75%→0%A;8~11 min,0%A;11~11.1 min,0%→75%A);流速:1.0 mL·min-1;进样体积:2 μl。
2.2.2 质谱条件 电喷雾电离源;检测离子: [M+H]+m/z187.1(对甲苯磺酸甲酯),201.1(对甲苯磺酸乙酯);碎裂电压:75 eV;干燥气流速:12 L·min-1;干燥气温度:350 ℃;雾化气压力:40 psi;毛细管电压:3 000 V。
分别称取约200 mg的醋酸甲羟孕酮样品置1 mL量瓶中,分别于60 ℃、48 000 Lx紫外可见光、40 ℃、75%湿度条件下放置1周,用稀释剂稀释至刻度,混合均匀,得高温、光照、高湿破坏样品。另分别称取约200 mg醋酸甲羟孕酮样品置2 mL量瓶中,分别加入对照品溶液、1.0 mL 1 mol·L-1的HCl,1.0 mL 0.1 mol·L-1的NaOH,1.0 mL 30%过氧化氢溶液,混合均匀,室温下放置1 h,加入稀释剂至刻度,振摇,得供试品加对照品溶液、酸、碱、氧化破坏样品。取对照品溶液、稀释剂、供试品溶液及各破坏样品溶液等分别按“2.2”项下方法进样分析,在对甲苯磺酸甲酯、对甲苯磺酸乙酯出峰位置均无干扰峰出现,代表性图谱见图1。

图1 专属性试验代表性图谱
A-样品高温破坏前后对比;B-供试品加对照品溶液;C-对照品溶液。
Fig. 1 Specification typical chromatograms
A-comparation of before and after heat degradation; B-sample solution added reference standard; C-standard solution.
分别精密量取杂质对照品储备液5.0,5.0,1.0,1.0,0.5 mL置10,20,10,20,20 mL量瓶中,用稀释剂稀释至刻度,混合均匀后,此溶液为L5、L4、L3、L2、L1。精密量取2.0 mL L1溶液置10 mL量瓶中,用稀释剂稀释至刻度,混合均匀,此溶液作为L6溶液。L1~L6溶液分别按“2.2”项下方法进样分析,以浓度为横坐标,峰面积为纵坐标,按最小二乘法进行线性回归,得回归方程。对甲苯磺酸甲酯回归方程:y=5 780.6x-164.51,r=1.000,对甲苯磺酸甲酯回归方程y=29 672x-1 292.6,r=0.999 8,对甲苯磺酸甲酯和对甲苯磺酸甲酯在0.05~5.08mg·mL-1内线性关系良好。
以信噪比>10为定量限,信噪比>3为检测限。线性溶液L6即为对甲苯磺酸甲酯定量限溶液,精密量取3.0 mL L6溶液置10 mL量瓶中,用稀释剂稀释至刻度,混合均匀,此溶液对甲苯磺酸乙酯定量限溶液;分别精密量取对苯磺酸甲酯、对甲苯磺酸乙酯定量限溶液5.0 mL置不同10 mL量瓶中,用稀释剂分别稀释至刻度,混合均匀,此溶液作为检测限溶液,分别按“2.2”项下方法进样分析。对甲苯磺酸甲酯定量限为0.10 ng(S/N=14.1),检测限均为0.05 ng(S/N=4.0),对甲苯磺酸乙酯定量限为0.03 ng(S/N=12.2),检测限为0.02 ng(S/N=5.3)。
按“2.1”对照品溶液制备方法,分别配置6份精密度测试溶液,分别按“2.2”项下方法进样分析。对甲苯磺酸甲酯峰面积的RSD为4.70%,对甲基苯磺酸乙酯面积的RSD为4.00%。
精密量取0.7 mL线性试验中L3、L2、L1浓度溶液分别置1 mL量瓶中,每个浓度配制3份,分别精密称定醋酸甲羟孕酮样品200 mg(批号:X2-110823,对甲苯磺酸甲酯、对甲苯磺酸乙酯均未检出),置各量瓶中,混合均匀,然后“2.2”项下方法分别进样分析,结果见表1。
表1 准确度试验结果(n=9)
Tab. 1 Results of recovery test (n=9)

取线性溶液L1在不同柱温(25,30,35 ℃),不同流动相A(pH为6.7,7.0和7.2)分别按“2.2”项下方法进样分析,对甲苯磺酸甲酯、对甲苯磺酸乙酯均能有效分离,方法进行微调时对检测结果无影响,方法耐用性良好。
提高进样浓度是最直接有效增加微量基因毒性杂质检测能力的办法,醋酸甲羟孕酮在三氯甲烷中极易溶解,在丙酮中溶解,在乙酸乙酯中略溶,在无水乙醇中微溶,在水中不溶[7]。通过筛选,醋酸甲羟孕酮在常用有机试剂二氯甲烷中溶解度极高,但因为反相高效液相流动相以水和乙腈、甲醇等有机相组成,样品溶液中化合物浓度和二氯甲烷浓度过高都会因为化合物析出或者二氯甲烷与水相体系分层堵塞色谱柱,无法完成检测。通过筛选,二氯甲烷-乙腈(1∶1) 1 mL可以快速溶解200 mg醋酸甲羟孕酮,2 μl的进样体积可以保证样品进样顺利完成。
对甲苯磺酸甲酯、对甲苯磺酸乙酯结构上只有一个甲基的差异,为满足同时快速分析2个物质,选择色谱柱XDB-C18(50 mm×4.6 mm,1.8 μm),13 min内完成一个样品测试,同时2个物质仍可以有效的分离,峰形好,提高了信噪比。对甲苯磺酸甲酯、对甲苯磺酸乙酯有较强的电负性,加入醋酸铵并调节pH值至7.0可以有效的减少峰拖尾,改善峰型,提高理论板数。
提高离子源气体流速、干燥气体温度等均可以改善质谱检测灵敏度。本研究发现在相同浓度时,对甲苯磺酸甲酯、对甲苯磺酸乙酯在质谱中的信噪比有较大差异,对甲苯磺酸乙酯色谱峰的峰高明显高于对甲苯磺酸甲酯色谱峰,这可能是由于结构上的差异使对甲苯磺酸乙酯更易接收质子带电从而获得更高的灵敏度,这方面我们将在后续的工作中深入研究。
醋酸甲羟孕酮中对甲基苯磺酸甲酯,对甲基苯磺酸乙酯的LC-MS检测方法验证结果表明线性、重复性、精密度、专属性和系统耐用性好,最低检测限为≤0.13 μg·g-1,远小于限量1.5 μg·g-1要求,方法灵敏度高,此方法适用于醋酸甲羟孕酮样品中对甲基苯磺酸甲酯及对甲基苯磺酸乙酯的检测。
REFERENCES
[1] 叶思款, 季波, 吴佩兹, 等. 醋酸甲羟孕酮的药理作用与临床应用[J]. 中国药业, 2010, 19(1): 63-64.
[2] CDER. Guidance for Industry Genotoxic and Carcinogenic Impurities in Drug Substances and Products: Recommended Approaches [EB/OL]. (2008-10).
[3] CHMP. Guideline on the Limits of Genotoxic Impurities [EB/OL]. (2006-06-28).
[4] ICH. Guideline: Genotoxic Impurities Guidelines of Assessment and Control of DNA Reactive (Mutagenic) Impurities in Pharmaceuticals to Limit Potential Carcinogenic Risk M7(R1) [EB/OL]. (2017-03-31).
[5] LIANG J M, FU C, CHEN Y. Determination of genotoxic impurities in Escitalopram Oxalate by LC-MS/MS [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2016, 11(33): 1436-1440.
[6] LI J K, W S S, L Y L. Validation of GC-MS method for determination of genotoxic impurities p-toluene sulfonic acid esters [J]. Contemp Chem Indust(当代化工), 2017, 2(46): 378-380.
[7] 中国药典. 二部[S]. 2015: 1527.
(本文责编:曹粤锋)
Determination of Methyl p-Toluenesulfonate and Ethyl p-Toluenesulfonate in Medroxyprogesterone Acetate by LC-MS
Lu Fei1, Xing Shanshan1, Wang Yong2*
(1.Xianju People’s Hospital, Taizhou 317300, China; 2.Zhejiang Xianju Pharmaceutical Company LTD., Taizhou 317300, China)
ABSTRACT: OBJECTIVETo establish a method for detecting genotoxin methyl p-toluenesulfonate and ethyl p-toluenesulfonate in medroxyprogesterone acetate by LC-MS.METHODSThe determination was peformed on XDB-C18 column (50 mm×4.6 mm, 1.8 μm) with mobile phase A(10 mmol·L-1ammonium acetate, adjust pH to 7.0 with aqueous ammonia) and mobile phase B(acetonitrile). The mass spectrometer was performed in SIMm/z: 187.1, 201.1 by positive monitoring.RESULTSBoth of methyl p-toluenesulfonateand ethyl p-toluenesulfonate were linear in the range of0.05-5.08mg·mL-1. LOQ and LOD of methyl p-toluenesulfonate was 0.10 ng and 0.05 ng, LOQ and LOD of ethyl p-toluenesulfonate was 0.03 ng and 0.02 ng. Their recoveries were 101.6% and 98.7%, with RSDs of 3.46% and 2.22%, respectively.CONCLUSIONThis method is applicable to the detection of methyl p-toluenesulfonate and ethyl p-toluenesulfonate in medroxyprogesterone acetate.
KEY WORDS:medroxyprogesterone acetate; methyl p-toluenesulfonate; ethyl p-toluenesulfonate; genotoxic impurities; LC-MS
中图分类号:R917.101
文献标志码:B
文章编号:1007-7693(2018)05-0657-03
DOI:10.13748/j.cnki.issn1007-7693.2018.05.008
引用本文:芦飞, 邢珊珊, 王咏. LC-MS测定醋酸甲羟孕酮中对甲苯磺酸甲酯及对甲苯磺酸乙酯的含量[J]. 中国现代应用药学, 2018, 35(5): 657-659.
收稿日期:2017-11-01
作者简介:芦飞,女,主管药师 Tel: 18705866264 E-mail: 43250639@qq.com
*通信作者:王咏,男,博士,高级工程师 Tel: 13666852756 E-mail: wywangyong2004@126.com