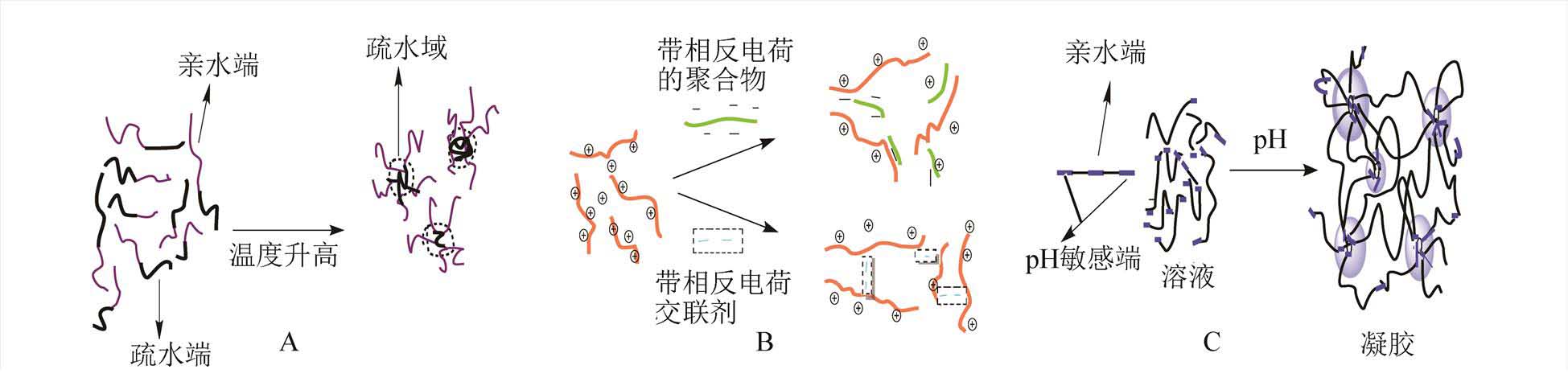
图1 原位凝胶形成机制图[12]
黄星雨1,袁佳敏1,杨琼梁2,欧阳婷1,3,周宇婷1,颜红1,4*
(1.湖南中医药大学药学院,长沙 410208;2.浏阳市中医医院药剂科,湖南 浏阳 410300;3.湖南中医药大学第一附属医院,长沙 410007;4.中药成药性与制剂制备湖南省重点实验室,长沙 410208)
摘要:鼻用原位凝胶剂近年已成为药剂学研究热点。本文参阅近年来国内外相关文献,从鼻用原位凝胶剂的特点、分类、制备、评价方法和应用进行了综述,以期为鼻用原位凝胶剂的进一步研究与应用提供依据。
关键词:鼻用原位凝胶剂;特点;分类;制备;评价方法;应用
鼻部给药是一种传统的给药方式,常用来治疗各种鼻腔和鼻窦疾病,亦可作与鼻病有关的邻近器官疾患的辅助用药[1]。原位凝胶剂(在位凝胶)是一种新型的药物剂型,系指一类以溶液状态给药后,能在用药部位立即发生相转变,由液态转化形成非化学交联半固体凝胶的制剂[2],并且原位凝胶可以作为缓释载体与脂质体等新剂型结合增加药物稳定性[3]。本文查阅了近年来国内外文献,从原位凝胶剂的特点、类型、制备、评价方法和应用等方面阐述了该制剂的研究进展,以期为鼻用原位凝胶剂的进一步研究与应用提供依据。
目前市场上的鼻用制剂多为滴鼻剂、喷雾剂等液体制剂,这类普通鼻用制剂使用便捷,患者用药的顺应性强,但由于鼻黏膜纤毛运动,致使该类制剂在鼻黏膜表面的滞留时间很短(15~30 min)[4],生物利用度较低。而鼻用软膏剂、鼻用乳膏剂等半固体鼻用制剂虽能延长药物在鼻黏膜滞留时间,但其黏度较高,存在给药剂量不准确、使用不方便的缺点。鼻用原位凝胶剂具有亲水性三维网络结构和独特的溶液-凝胶转变性能,以溶液状态给药,在用药部位即可发生相转变,由液体转变成半固体,具有良好的组织相容性和生物黏附性,增强了对黏膜组织的亲和力、延长了药物的滞留时间。鼻用原位凝胶剂结合了液体与半固体鼻用制剂的优点,同时弥补了两者的缺点,从而备受青睐。除此之外,原位凝胶作为一种新型缓控释给药载体,能够以液体状态加载药物,达到组织兼容、缓控释释放的独特优势,且其工艺简单易行,适合于工业大生产。
原位凝胶制备工艺简单,选择合适的溶剂将辅料与药物溶解在其中即可。研究表明,影响原位凝胶成型的因素主要有基质浓度、离子强度、体系pH值等,常根据其形成机制的不同,将原位凝胶分为温度敏感型、离子敏感型、pH敏感型、复合敏感型等。
温度敏感型原位凝胶是一类对温度变化敏感的原位凝胶,即环境温度低于最低临界相变温度(LCST)时呈现液体状态,高于LCST时呈现半固体凝胶状态,而鼻腔温度大约为32~35 ℃,大部分温敏型鼻用原位凝胶的胶凝温度都在32~34 ℃之间,故其用于鼻腔时形成半固体凝胶,可延长药物在鼻黏膜的黏附时间,从而提高生物利用度[5]。温敏型原位凝胶处于室温时(20~25 ℃)为液态,当接触到体液(35~37 ℃)后立即发生相转变,温度敏感型凝胶在结构上均包含一定比例的疏水和亲水嵌段,温度升高使得不同性质的嵌段间和溶剂间发生相互作用,从而形成凝胶[6](图1A)。温度敏感型原位凝胶常用的基质有泊洛沙姆、壳聚糖和纤维素衍生物等[7]。目前研究较多为泊洛沙姆和壳聚糖(CS),有研究者单用泊洛沙姆或壳聚糖作为温敏型原位凝胶基质,亦有将两者合用,通过优选其比例以确定最佳制剂处方。肖金宝等[8]采用正交实验优选出银杏叶提取物温度敏感型鼻用原位凝胶的最佳制备工艺为泊洛沙姆407(F127)︰泊洛沙姆188(F68)为15︰20、壳聚糖0.4%、HP-β-CD 30%,测得其胶凝温度为35.8 ℃。药效学研究表明该凝胶具有良好的缓释作用,可通过鼻-脑通道直接进入脑内发挥药效。李美燕等[9]优选出壳聚糖质量浓度为2%,采用壳聚糖溶液/β-甘油磷酸钠的混合体系,载入氢溴酸东莨菪碱,研制了氢溴酸东莨菪碱鼻用原位凝胶,其胶凝温度为34 ℃,以此考察凝胶的温敏特性。Shelke等[10]选用F127为基质,分别以卡波姆934和羟丙甲纤维素为黏附剂制备温敏型佐米曲普坦纳米脂质体鼻用原位凝胶,采用析因设计法优化处方,得到最优制剂处方是18%P407和3%卡波姆934或者是18%P407和1%的羟丙甲纤维素。此外,还有研究报道以壳聚糖与葡萄糖磷酸二钠为基质材料制备鲑鱼降钙素温敏型原位凝胶[11]。
离子敏感型原位凝胶主要是基质聚合物与体液中的K+、Na+、Ca2+等阳离子络合,从而发生构象改变形成凝胶。离子原位凝胶剂形成的两种方法,一是加入带相反电荷的聚合物,另一种是加入相反电荷的小分子交联剂,从而形成网络状凝胶(图1B)。此类凝胶的基质一般为多糖类衍生物,常以去乙酰结冷胶(DGG)、结冷胶和海藻酸钠为基质。研究者发现以DGG为基质制备的离子敏感型鼻用原位凝胶,对鼻黏膜的刺激性小、预防和治疗慢性鼻炎具有潜在的价值,故笔者统计了近年来以DGG为基质制备的离子敏感型原位凝胶,具体见表1。此外,有研究者[13]采用离心失水实验考察了鼻液中单独阳离子与DGG形成凝胶的能力。结果发现对不同浓度的DGG溶液,Ca2+形成凝胶的持水能力均最强,Na+、K+较弱,且两者之间无明显差异。肖春雷[14]等以结冷胶为凝胶材料,制备氢溴酸高乌甲素鼻用原位凝胶,并比较了3种不同吸收促进剂(β-环糊精,吐温-80 和冰片)对其的促吸收作用。Pathan等[15]以不同浓度结冷胶为基质,不同浓度的羟丙甲纤维素E4M作为黏附剂,使用析因设计筛选出盐酸氮卓斯汀鼻用原位凝胶剂的最佳配方为0.4%的结冷胶和0.1%羟丙甲纤维素E4M,在该配方下的凝胶能延长盐酸氮卓斯汀在鼻内的停留时间。Salunke等[16]发现用离子活化的结冷胶作为基质制备的硫酸沙丁胺醇鼻用原位凝胶具有良好的平喘效果。此外,亦有单用海藻酸盐作为基质的报道,研究者通过测定胶凝时的最佳Ca2+浓度,采用搅拌法以海藻酸钠作为辅料成功制备了猫爪草离子敏感型原位凝胶[17]。

图1 原位凝胶形成机制图[12]
A-温敏型;B-离子型;C-pH型。
Fig. 1 Mechanism of sensitive in-situ gelling system
A -temperature sensitive type; B-Ionic type; C-pH type.
表1 DGG作为离子敏感型鼻用原位凝胶基质的应用[18-22]
Tab. 1 Application of DGG as an ion sensitive nasal in situ gel matrix

pH敏感型原位凝胶是由于体内外pH的不同而发生相转变形成的凝胶,鼻黏液的pH一般在5.5~7.0之间,此类体系的聚合物分子骨架中均含有大量的可解离基团,其胶凝行为是电荷间的排斥作用导致分子链伸展与相互缠结的结果(图1C),常用基质为卡波姆。宋逍等[23]通过黏度实验进行鸦胆子油鼻用pH敏感型原位凝胶的处方筛选,考察了不同的pH值、不同基质浓度条件,筛选出凝胶胶凝时最佳pH值为5.5,优选的制剂处方为0.5%卡波姆、0.25%羟丙基甲基纤维素SHE50、10.44 g吐温-80、2.18 gN-甲基吡咯烷酮和5 mL鸦胆子油。刘宏伟[24]考察了泊洛沙姆407、羟丙基甲基纤维素、羧甲基纤维素钠等不同黏合剂与卡波姆的配比,结果发现卡波姆和羟丙基甲基纤维素流变学特征类似,在pH 4.0时为低黏度的流体,pH值在6.5以上时胶凝,释放度试验也表明两者均具有缓释作用,故采用0.5%卡波姆和1.4%羟丙基甲基纤维素为辅料制备了磷酸川芎嗪pH敏感型原位凝胶。此外还有柴胡鼻用pH敏感型原位凝胶、硫酸沙丁胺醇鼻用pH敏感型原位凝胶的报道[25-26]。
单一的原位凝胶虽有其自身的优点,但也存在用药范围窄、相变温度低、凝胶溶蚀快、药物突释等缺点。而复合型原位凝胶通常是由两种不同类型的基质制备而成,具有改善药物溶解性、提高稳定性、减小刺激性、用药范围广、缓控释等优点,越来越受研究者青睐。常见复合型原位凝胶有温度-pH双敏型和温度-离子双敏型。程刚等[27]以F127和F68为温度敏感型基质材料,以壳聚糖为pH敏感型基质材料,并以胶凝温度和胶凝时间为考察指标,筛选出石杉碱甲微乳温度/pH鼻用原位凝胶的最佳处方(20.41%F127、1.58%F68和0.65%CS),使得该复合凝胶在生理环境(29~34 ℃、pH 6.0~7.0)时发生相转变,同时还对该凝胶进行了澄清度、体外释药行为等研究。研究者[28]以临界相变温度、临界相变离子强度为指标筛选温敏及离子敏感材料,以透析袋法评价该温度-离子敏感复合凝胶的凝胶外排水量、溶蚀速率和体外释放度,并以断裂距离为指标评价凝胶的黏膜黏附力。结果表明以0.3% DGG和18.0% F127为复合基质制备的利巴韦林温度-离子敏感复合型原位凝胶最佳,此时的临界相变温度为32.6 ℃,临界相变阳离子强度为93.4 mmol·kg-1,该复合凝胶较之用这两种基质单独制备的凝胶外排水量小、溶蚀速率小、黏附性好,具有良好的缓释效果,且该复合型原位凝胶基质很适宜作为水溶性药物的鼻用缓释载体。
对一种制剂应用效果进行评价是该类制剂安全性和有效性的保证。目前已有研究者从以下几方面开展鼻用原位凝胶的评价,但大多集中于基本评价,鼻用原位凝胶评价的实验方法和质量控制方法仍不是很完善,有待进一步的研究[29]。
研究者针对鼻用原位凝胶剂的外观及理化性质开展了研究。田效志等[30]采用稳定性试验评价了葛根素鼻用原位凝胶剂的外观性状,结果表明该制剂的外观澄清透明,符合中国药典的相关要求。黄秋艳等[31]采用离心法,对室温(25 ℃)和胶凝温度(34 ℃)下放置2周的苍艾油包合物-鼻用温敏原位凝胶进行离心,结果表明两者离心后均未分层,且外观透明、均一性好。pH值常作为评价鼻用原位凝胶剂理化性质的指标之一,制剂的pH值通常都在5.5~7.5之间,符合鼻用制剂的pH值。此外,亦有研究者采用粒径和表面电位作为制剂成型的评价指标。药物的粒径和凝胶的致密度可影响药物在鼻腔的溶出度,Zeta电位可影响凝胶的稳定性。李晓云等[32]采用贝克曼粒度电位仪测定了姜黄素微乳温敏原位凝胶的粒径与电位,结果表明其粒径分布均匀,平均粒径为21.2 nm,Zeta电位为-26.13 mV,呈稳定状态。
此外,关于鼻用原位凝胶剂的胶凝温度、胶凝时间、相转变温度、相转变离子强度、黏度、黏附力、制剂载药量等评价指标的研究亦有报道。温敏型原位凝胶常以胶凝温度为评价指标,采用一定实验方法优化处方及制备工艺[33-34]。杨军宣等[35]制备栀子环烯醚萜苷鼻用原位凝胶时以临界相变阳离子浓度作为评价指标,并发现该凝胶在阳离子浓度达到人工鼻黏液的1/2时即发生相转变。Sheri等[36]以胶凝温度、胶凝时间和pH值为指标评价氯雷他定鼻用原位凝胶制剂,结果发现该制剂胶凝温度在(33.1±0.43)℃和(34.8±0.82)℃之间,胶凝时间范围在(4.0±0.21)s~(11.3±0.22)s之间,pH值在5.6±0.004和6.0±0.003之间,且制剂对黏膜无刺激性。鼻用原位凝胶剂的流变学指标通常有黏度、黏附力和涂展性等。董芙蓉等[37]评价芷冰鼻腔原位凝胶时,采用黏度计测定凝胶黏度为406 mPa·s,采用位移法测定其黏附力为5 h之内仅移动1 cm左右,表明该凝胶黏附力强。陈奋等[38]采用流变仪考察平阳霉素原位凝胶体系的流变学性质,发现随着温度升高到37 ℃左右时,原位凝胶溶液发生了从溶液向凝胶的相转变过程。
目前鼻用原位凝胶剂采用的含量测定方法有HPLC-UV、RP-HPLC、GC和HPLC,最常用为HPLC。朱铁梁等[39]用甲醇稀释溶解复方更昔洛韦氢化可的松琥珀酸钠鼻用原位凝胶,并采用HPLC同时测定该制剂中更昔洛韦和氢化可的松琥珀酸钠的含量。结果表明,更昔洛韦和氢化可的松琥珀酸钠在一定浓度范围内与峰面积线性均良好,平均回收率好。
药物的释放是很关键的一步,通常使用释放度来评价鼻用原位凝胶的体外释放。鼻用原位凝胶剂的释药方式主要符合有膜溶出模型和无膜溶出模型,释放机制通常符合Higuchi方程和Fick定律。有膜溶出法通常有Franz扩散池法、改良的美国药典溶出度测定第三法、渗析池法。无膜溶出法主要是通过溶蚀机制释放药物。肖金宝等[8]采用了无膜释放法、透牛、羊鼻黏膜释放法和透析袋法研究银杏叶提取物温度敏感型鼻用原位凝胶,发现该凝胶是通过扩散作用释放。邓小丽等[40]优化丙酸氟替卡松鼻用温敏凝胶处方时用Franz扩散池法对其体外释放进行了考察,结果发现其体外释放符合Higuchi方程。此外还有鼻用原位凝胶通过溶蚀机制释放药物的,谢悦良[41]等研究川陈皮素温敏型鼻用原位凝胶体外释药行为时采用扩散池法、无膜溶出法以及渗析池法,研究发现川陈皮素温敏型鼻用原位凝胶主要通过无膜溶出机制释药,其释放符合一级动力学方程。
目前鼻用原位凝胶剂在体的评价方法主要为在体局部评价、在体药效学评价和在体药动学评价。在体局部评价涉及凝胶对动物黏膜的局部刺激性和鼻黏膜纤毛毒性评价。罗洁琦等[20]将三七总皂苷离子敏感型鼻用原位凝胶用于家兔眼结膜内以检测其对黏膜的刺激性。结果发现家兔眼结膜未见明显充血、流泪、羞明、水肿等刺激症状,表明制剂对兔眼结膜无明显刺激作用,并能延长药物与鼻黏膜的接触时间。闫智慧等[42]采用在体蟾蜍上颚法来评价天麻素鼻腔温敏原位凝胶的纤毛毒性,实验表明天麻素原位凝胶对蟾蜍上颚纤毛无毒性。
在体药效学和药动学评价通常是利用整体动物模型考察该类制剂的在体治疗作用。如卓玉娟等[19]采用大鼠慢性鼻炎模型检测辛芷离子敏感鼻用原位凝胶的药效,结果发现该凝胶对大鼠慢性鼻炎具有一定的治疗作用。Bhandwalkar等[43]通过黏膜组织病理学评价盐酸文拉法辛原位凝胶在大鼠体内的药效学研究,结果表明该凝胶给药后鼻黏膜未有明显病变,未造成大鼠鼻腔上皮损伤、无刺激性且明显提高了盐酸文拉法辛治疗抑郁症的疗效。王爽等[44]研究姜黄素微乳原位凝胶剂体内药物动力学时,发现鼻腔给药组与注射组均符合二室模型,鼻腔给药的峰浓度明显小于注射给药的峰浓度,但药物在血液中的平均滞留时间、生物半衰期、表观分布容积等都明显延长或增大。
鼻黏膜分布着丰富的血管,药物可由此直接进入体循环,有效避免肝脏的首过效应,所以鼻部给药适用于不能注射和不便口服的药物,但由于鼻纤毛具有自动清除机制,对以溶液状态进入鼻腔的药物保留时间短,而鼻用原位凝胶剂具有较好的生物黏附性,可以延长药物在鼻黏膜的滞留时间,提高生物利用度,常用来治疗鼻部疾病如慢性鼻炎,过敏性鼻炎等。刘梅采用0.3% DGG和18.0% P407为基质制备辛芷复方温度-离子敏感型鼻用原位凝胶,并用大鼠做鼻炎模型,结果表明该凝胶对慢性鼻炎具有良好的治疗效果[45]。研究者以丙酸氟替卡松为主药,P407、P188为基质,采用冷法制备丙酸氟替卡松鼻用温敏凝胶用于治疗过敏性鼻炎[40]。
鼻黏膜在解剖生理上与脑部存在独特的天然联系,经鼻给药后,药物通过嗅神经通路和嗅黏膜上皮通路进入脑,因此许多小分子和大分子药物经鼻给药后能迅速到达脑内,发挥脑靶向作用。鼻用原位凝胶剂具有良好的组织相容性和生物黏附性,故该制剂与黏膜组织亲和力强、延长了药物的滞留时间,能显著提高药物的脑靶向性。陶涛等[46]通过比较石杉碱甲的鼻用原位凝胶、注射液和市售片剂在大鼠脑内的浓度,发现原位凝胶鼻腔给药较静注和灌胃显著增加了药物在脑内的浓度,对治疗老年痴呆和良性衰老遗忘症具有良好效果。陈溪等[47]优化了姜黄素鼻用原位凝胶的处方,将其制成温敏型,以大鼠为模型,考察姜黄素原位凝胶的脑靶向性及脑内分布,并与其静脉注射剂相比较。实验表明,原位凝胶在大脑、小脑、海马、嗅球中的药物靶向效率(DTE)都高于静脉给药,原位凝胶给药显著增强了姜黄素的脑靶向性,可加强姜黄素的抗炎,抗氧化和抗癌作用。
鼻用原位凝胶具有使用方便、与鼻黏膜组织亲和力强、脑靶向性好、控制释药性能良好等优点,近年来已成为国内外药剂学工作者的研究热点。但鼻用原位凝胶在实际应用方面还存在一些问题,如药物突释现象,这可能与制剂的基质材料有关。制剂质量评价的指标,鼻用原位凝胶基质材料的研发、制剂的释药机制、制剂在体内的吸收以及制剂在中药方面的应用等问题仍都有待进一步研究。
REFERENCES
[1] 周莉妤, 鄂淑云, 周莉婷, 等. 鼻黏膜给药的研究进展[J]. 中国现代药物应用, 2009, 3(4): 198-199.
[2] SHU Y, LI X F, WU S, et al. Progress of in situ gel drug delivery system in the application of traditional Chinese medicine preparation [J]. J Chengdu Univ Tradit Chin Med(成都中医药大学学报), 2014, 37(3): 120-123.
[3] CAO J W, NI J J, YAO J, et al. Preparation of rifampicin liposomes in situ gel system and its in vitro release mechanism [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2016, 33(2): 183-187.
[4] 陆彬. 药物新剂型与新技术[M]. 第2版. 北京: 人民卫生出版社, 2005: 643-644.
[5] ZHAO J T, LIU H, LI G K, et al. Research and application progress of thermo-sensitive gels [J]. Guangzhou Chem Indust(广州化工), 2013, 41(24): 9-11.
[6] RUEL-GARIEPY E, LEROUX J C. In situ-forming hydrogels—review of temperature-sensitive systems [J]. Eur J Pharm Biopharm, 2004, 58(2): 409-426.
[7] KARAVASILI C, FATOUROS D G. Smart materials: In situ gel-forming systems for nasal delivery [J]. Drug Discov Today, 2016, 21(1): 157-166.
[8] 肖金宝. 银杏叶提取物温度敏感型鼻用原位凝胶的研究 [D]. 吉林: 延边大学, 2013.
[9] 李美燕. 氢溴酸东莨菪碱温敏型鼻用原位凝胶的研制[D]. 重庆: 重庆医科大学, 2015.
[10] SHELKE S, SHAHI S, JALALPURE S, et al. Poloxamer 407-based intranasal thermoreversible gel of zolmitriptan- loaded nanoethosomes: formulation, optimization, evaluation and permeation studies [J]. J Liposome Res, 2016, 26(4): 313-323.
[11] WANG X N, CHANG T W, QU Y, et al. Preparation and evaluation of a thermosensitive in situ gel containing salmon calcitonin [J]. Sci Technol Chem Ind(化工科技), 2017, 25(2): 39-43.
[12] KUTE P R, GONDKAR S B, SAUDAGAR R B. Ophthalmic in-situ gel: an overview [J]. World J Pharm Pharm Sci, 2015, 4(4): 549-568
[13] CAO S L, XU F, JIANG X G, et al. Preparation of ion-activated in situ gel systems for nasal use and its elimination pharmacokinetic study in rabbits [J]. Chin Pharm J(中国药学杂志), 2007, 42(11): 844-848.
[14] XIAO C L, ZHU J B, SUN C. An in situ gel system for nasal delivery of lappaconitine hydrobromide:preparation and formulation evaluation [J]. Prog Pharm Sci(药学进展), 2009, 33(9): 416-419.
[15] PATHAN I B, CHUDIWAL V, FAROOQUI I, et al. Formulation design and evaluation of nasal in situ gel as a novel vehicle for azelastine hydrochloride [J]. Int J Drug Deliv, 2013, 5(3): 284-290.
[16] SALUNKE S R, PATIL S B. Ion activated in situ gel of gellan gum containing salbutamol sulphate for nasal administration [J]. Int J Biol Macromol, 2016(87): 41-47.
[17] 胡春晖. 猫爪草提取物离子敏感型原位凝胶的制备及体外释药研究[J]. 时珍国医国药, 2015, 26(10): 2412-2413.
[18] ZANG Q Z, TANG T, LONG K H, et al. Preparation of α-Asarone nanoparticle ion-sensitive in situ nasal gel and its drug releasing performance in vitro [J]. Chin J Hosp Pharm(中国医院药学杂志), 2015, 35(23): 2115-2118.
[19] ZHOU C M, WANG Y N, ZHANG L M, et al. Nanoemulsion and in-situ gel nasal drops of Haheilili extract [J]. Chin Tradit Pat Med(中成药), 2015, 37(6): 1210-1215.
[20] 郑欣. 尼古丁鼻用离子型原位凝胶的制备与考察[D]. 重庆: 重庆医科大学, 2015.
[21] ZHUO Y J, LIU X, YU L R, et al. Preparation of Xinzhi ion-activated nasal in situ gel and evaluation of drug release in vitro [J]. Chin J Hosp Pharm(中国医院药学杂志), 2010, 30(1): 30-33.
[22] LUO J Q, SHA X Y, FANG X L. Preparation of Panax notoginseng saponins ion-sensitive in situ nasal gel [J]. Chin Tradit Herb Drugs(中草药), 2011, 42(7): 1299-1304.
[23] SONG X, DUAN X, TANG Z S, et al. Preparation and drug release in vitro of the pH sensitive in-situ gel system containing Brucea java fruit for oil nasal [J]. J Liaoning Univ Tradit Chin Med(辽宁中医药大学学报), 2016, 18(10): 45-47.
[24] 刘宏伟. 磷酸川芎嗪鼻用pH敏感型原位凝胶及其PK/PD结合模型研究[D]. 广州: 广州中医药大学, 2010.
[25] CHEN E, CHEN J, CAO S L, et al. Preparation and cooling effect of nasal pH-sensitive in situ gel system of Radix Bupleuri [J]. Chin J Pharm(中国医药工业杂志), 2008, 39(9): 666-670.
[26] CHENG H Z, YANG X Y. Preparation of salbutamol sulphate for nose in situ gel and its release rate in vitro [J]. Anti-infec Pharm(抗感染药学), 2016, 13(1): 18-22.
[27] 程刚. 石杉碱甲微乳温度/pH鼻用原位凝胶的研究[D]. 安徽: 安徽中医药大学, 2016.
[28] LUAN L, GAN Y, ZHANG X X, et al. Preparation and in vitro evaluation of thermo-and ion-sensitive in situ gels of vibavirin via intranasal administration [J]. J Shenyang Pharm Univ(沈阳药科大学学报), 2009, 26(4): 249-253.
[29] 关玲玲, 张开莲. 鼻用原位凝胶的研究进展[J]. 泸州医学院学报, 2011, 34(1): 97-99.
[30] TIAN X Z, ZHOU N, JIA Y Y, et al. Studies on the stability of puerarin in nasal situ gel [J]. Guangming J Chin Med(光明中医), 2013, 28(7): 1342-1344.
[31] 黄秋艳. 苍艾油包合物—原位凝胶的制备及其鼻腔吸收药动学研究[D]. 昆明: 云南中医学院, 2016.
[32] 李晓云, 窦金凤, 王爽, 等. 姜黄素微乳温敏原位凝胶剂的制备及其理化性质研究[J]. 药物生物技术, 2013, 20(3): 225-228.
[33] RAVI P R, ADITYA N, PATIL S, et al. Nasal in-situ gels for delivery of rasagiline mesylate: improvement in bioavailability and brain localization [J]. Drug Deliv, 2015, 22(7): 903-910.
[34] XU R C, LIN Y J, WU P J. Optimization for preparation technology of baicalin-phospholipid complex in situ nasal gel by central composite design-response surface method [J]. Chin Tradit Herb Drugs(中草药), 2012, 43(6): 1092-1096.
[35] YANG J X, ZHANG H Y, ZHOU N H, et al. Preparation of nasal in situ gel of gardenia iridoid glycosides [J]. Chin Tradit Pat Med(中成药), 2014, 36(7): 1402-1406.
[36] SHERAFUDEEN S P, VASANTHA P V. Development and evaluation of in situ nasal gel formulations of loratadine [J]. Res Pharm Sci, 2015, 10(6): 466-476.
[37] DONG F R, LIU L, CHEN Z L, et al. Quality evaluationa on stability of zhibing in-situ gel nasal-cavity [J]. Chin J Exp Tradit Med Form(中国实验方剂学杂志), 2011, 17(4): 19-22.
[38] CHEN F, JIA L Q, QIN X J, et al. Preparation and in vitro evaluation of Pingyangmycin loaded chitosan thermogels [J]. Chin J Hosp Pharm(中国医院药学杂志), 2017, 37(9): 792-796.
[39] ZHU T L, DAI X W, WANG Z Q, et al. Preparation and quality control of nasal gel of ganciclovir- hydrocortisone sodium succinate compound [J]. J Logis Univ PAPF(Med Sci)武警后勤学院学报(医学版), 2016, 25(1): 32-36.
[40] DENG X L, QIN D M, CHEN W. Optimization of the formulation of fluticasone propionate thermosensitive in-situ Gel nasal drops by central composite design-response surface methodology and investigation of vitro release retention [J]. J Shihezi Univ(Nat Sci)石河子大学学报(自然科学版), 2017, 35(1): 119-123.
[41] XIE Y L, FAN J H, DING J S, et al. In vitro release of nobiletin thermosensitive nasal in situ gel [J]. Chin J Pharm(中国医药工业杂志), 2011, 42(3): 189-192.
[42] YAN Z H, TAN Y, XIAO M. Cilia toxicity and mucosal irritation of gastrodin nasal temperature-sensitive in situ gel [J]. China Pharmacist(中国药师), 2017, 20(2): 253-255.
[43] BHANDWALKAR M J, AVACHAT A M. Thermoreversible nasal in situ gel of venlafaxine hydrochloride: formulation, characterization, and pharmacodynamic evaluation [J]. AAPS Pharm Sci Tech, 2013, 14(1): 101-110.
[44] 王爽. 姜黄素微乳原位凝胶剂鼻腔给药的研究[D]. 济南: 山东大学, 2012.
[45] 刘梅. 辛芷复方温度—离子敏感型鼻用原位凝胶[D]. 重庆: 重庆医科大学, 2012
[46] TAO T, ZHAO Y, YUE P, et al. Preparation of huperzine A nasal in situ gel and evaluation of its brain targeting following intranasal administration [J]. Acta Pharm Sin(药学学报), 2006, 41(11): 1104-1110.
[47] CHEN X, YANG H B, HU Y Q, et al. Enhanced brain targeting of curcumin by intranasal administration of a thermosensitive poloxamer hydrogel [J]. Pharm Clin Res(药学与临床研究), 2013, 21(1): 9-12.
(本文责编:李艳芳)
Research Progress of Nasal In-situ Gel
HUANG Xingyu1, YUAN Jiamin1, YANG Qiongliang2, OUYANG Ting1,3, ZHOU Yuting1, YAN Hong1,4*
(1.School of Pharmacy, Hunan University of Chinese Medicine, Changsha 410208, China; 2.Parmacy Department, Liuyang Traditional Chinese Medicine Hospital, Liuyang 410300, China; 3.The First Hospital of Hunan University of Chinese Medicine, Changsha 410007, China; 4.Hunan Provincial Key Laboratory of Druggability and Preparation Modification of TCM, Changsha 410208, China)
ABSTRACT: Nasal in-situ gel has become a hot spot in pharmaceutics research in recent years. The purpose of this paper is to summarize the characteristics, classification, prepration, evaluation methods and applications of nasal in-stiu gel by reviewing the relevant literatures at home and abroad in the late years. So as to provide theoretical support and method guidance for its further development.
KEY WORDS: nasal in-situ gel; characteristics; classification; peparation; evaluation methods; applications
中图分类号:R944.9
文献标志码:A
文章编号:1007-7693(2018)03-0448-06
DOI: 10.13748/j.cnki.issn1007-7693.2018.03.033
收稿日期:2017-07-13
引用本文:引用本文:黄星雨, 袁佳敏, 杨琼梁, 等. 鼻用原位凝胶剂的研究进展[J]. 中国现代应用药学, 2018, 35(3): 448-453.
基金项目:湖南省科技计划项目(2016TP1017);湖南省教育厅科学研究项目(17K068)
作者简介:黄星雨,女,硕士生 Tel: 18711024580 E-mail: 2473410898@qq.com
*通信作者:颜红,女,副教授,硕导 Tel: 13975335696 E-mail: yh8632@126.com