HPLC同时测定衢枳壳中7种指标成分的含量
黄文康1,岳超2,宋剑锋3,丁国琴4,张文婷2*,赵维良2*
(1.浙江中医药大学,杭州 310053;2.浙江省食品药品检验研究院,杭州 310052;3.衢州市食品药品检验研究院,浙江 衢州 324000;4.杭州市中医院,杭州 310007)
摘要:目的 建立HPLC同时测定衢枳壳中芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、木犀草素、川陈皮素和桔皮素含量。方法 采用Agilent Extend C18(4.6 mm×250 mm,5 μm)色谱柱,检测波长:330 nm,以乙腈-0.1%甲酸溶液为流动相,梯度洗脱,流速:1 ml·min-1,柱温:30 ℃。结果 芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、木犀草素、川陈皮素、桔皮素分别在23.30~1 164.80 ng,170.84~8 541.91 ng,17.22~861.20 ng,156.17~7 808.64 ng,3.13~156.48 ng,0.90~45.23 ng,0.85~42.27 ng内线性关系良好(r≥0.999 5,n=6),平均回收率分别为98.8%,101.3%,98.3%,96.8%,101.8%,101.7%,108.9%。结论 首次建立了衢枳壳中7个成分HPLC含量测定方法,该方法简便,结果准确,可为综合评价衢枳壳质量提供依据。
关键词:衢枳壳;高效液相色谱法;芸香柚皮苷;柚皮苷;橙皮苷;新橙皮苷;木犀草素;川陈皮素;桔皮素
衢枳壳为芸香科植物常山胡柚Citrus changshan-huyou Y.B.Chang的干燥未成熟果实,7月果皮尚绿时采收,主产浙江,以常山为重点产区。现代药理研究表明胡柚主要有效成分为黄酮[1],具有抗菌、抗氧化、降血脂和降氧化等作用[2-5]。胡柚青果在民间药用历史悠久,具有镇咳化痰、清热解毒、解酒醒脑等药用价值,但其质量评价和控制研究尚未完善,质量控制研究报道较少,宋剑锋等[6]建立了胡柚花和胡柚青果中柚皮苷、橙皮苷和新橙皮苷的HPLC含量测定方法,赵庆春等[7]建立了胡柚汁中柚皮芸香苷、柚皮苷和新橙皮苷的HPLC含量测定方法,郅景梅等[8]建立了HPLC测定胡柚皮中桔皮素和甜橙素含量的方法,其他成分含量分析未见报道。本实验首次建立了HPLC同时测定芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、木犀草素、桔皮素和川陈皮素7个成分含量测定方法,为进一步完善衢枳壳质量评价和控制提供参考依据。
1 仪器与试药
Agilent 1260高效液相色谱仪(美国Agilent公司);CP225D电子分析天平(德国赛多利斯);4020P超声波清洗器(韩国JAC公司)。
柚皮苷对照品(批号:110722-201312;含量按94.7%计)、橙皮苷对照品(批号:110721-201316;含量按95.3%计)、新橙皮苷对照品(批号:111857-201102;含量按99.6%计)和木犀草素对照品(批号:111520-200504;供含量测定用)均购自中国药品生物制品检定研究院;芸香柚皮苷对照品(批号:131208;含量>98%)、桔皮素对照品(批号:130708;含量>98%)和川陈皮素对照品(批号:130108;含量>98%)均购自维克奇生物科技有限公司。乙腈(色谱纯,美国Merck公司),其余试剂为分析纯,实验用水为超纯水。
实验共收集不同产地样品11批,经浙江省食品药品检验研究院郭增喜主任中药师鉴定,均为芸香科植物常山胡柚Citrus changshan-huyou Y. B. Chang的果实,详见表1。
表1 样品信息表
Tab. 1 Sample information

编号名称来源产地 S1衢枳壳衢州市食品药品检验研究院常山招贤 S2衢枳壳衢州市食品药品检验研究院航埠镇 S3衢枳壳衢州市食品药品检验研究院华驻 S4衢枳壳衢州市食品药品检验研究院常山大桥 S5衢枳壳衢州市食品药品检验研究院廿里 S6衢枳壳衢州市食品药品检验研究院石梁镇 S7衢枳壳衢州市食品药品检验研究院九华 S8衢枳壳衢州市食品药品检验研究院常山溪口 S9衢枳壳衢州市食品药品检验研究院常山柑橘园 S10衢枳壳衢州市食品药品检验研究院常山 S11衢枳壳衢州市食品药品检验研究院常山柑橘园
2 方法与结果
2.1 供试品溶液制备
取衢枳壳粗粉0.3 g精密称定,加50%甲醇适量,超声20 min,放冷至室温,加50%甲醇定容至25 mL量瓶中,摇匀,离心,取上清液,即得。
2.2 对照品溶液制备
取对照品适量,精密称定,加50%甲醇分别制成每1 ml含芸香柚皮苷46.59 μg,柚皮苷360.80 μg,橙皮苷3.45 μg,新橙皮苷312.35 μg,木犀草素6.26 μg,桔皮素1.01 μg,川陈皮素1.09 μg的混合对照品溶液,即得。
2.3 色谱条件
色谱柱:Agilent Extend C18柱(4.6 mm× 250 mm,5 mm)。流动相:乙腈(A)-0.1%甲酸溶液(B)。梯度洗脱:0~2 min,10%A;2~5 min,10%→18%A;5~10 min,18%A;10~25 min,18%→20%A;25~45 min,20%→50%A;45~70 min,50%→100%A。检测波长:330 nm;柱温:30 ℃;流速:1.0 ml·min-1。
2.4 系统适用性试验
分别精密吸取混合对照品溶液5 μl,供试品溶液10 μl,按“2.3”项下色谱条件进行测定,结果样品中各成分达到基线分离,理论板数按柚皮苷峰计算应≥3 000。色谱图见图1。
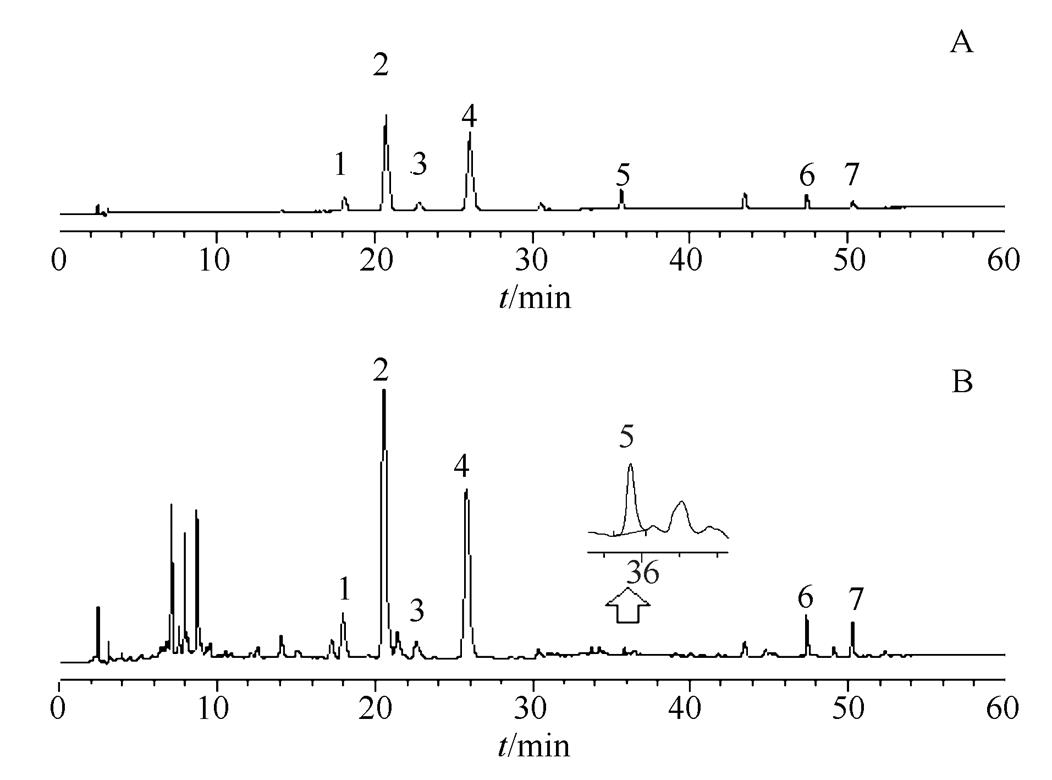

图1 高效液相色谱图
A -混合对照品;B-样品;1-芸香柚皮苷;2-柚皮苷;3-橙皮苷;4-新橙皮苷;5-木犀草素;6-桔皮素;7-川陈皮素。
Fig. 1 HPLC Chromatograms
A- standards solution; B-sample; 1-narirutin; 2-naringin; 3-hesperidin; 4-neohesperidin; 5-luteolin; 6-nobiletin; 7-hesperetin.
2.5 方法学考察
2.5.1 线性范围考察 将“2.2”项下混合对照品溶液分别进样1,5,10,20,30,40,50 μl,按“2.3”项下色谱条件进行测定,以色谱峰面积(Y)对进样量(X)进行回归,计算回归方程,结果见表2。
2.5.2 仪器精密度 精密吸取“2.2”项下混合对照品溶液5 μl,按“2.3”项下色谱条件重复进样6次,记录色谱峰峰面积,计算色谱峰面积RSD。芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、木犀草素、桔皮素和川陈皮素RSD(n=6)均≤2.0%,表明仪器精密度良好。
表2 7种指标成分的线性关系
Tab. 2 Linearity of determination of 7 index componenes
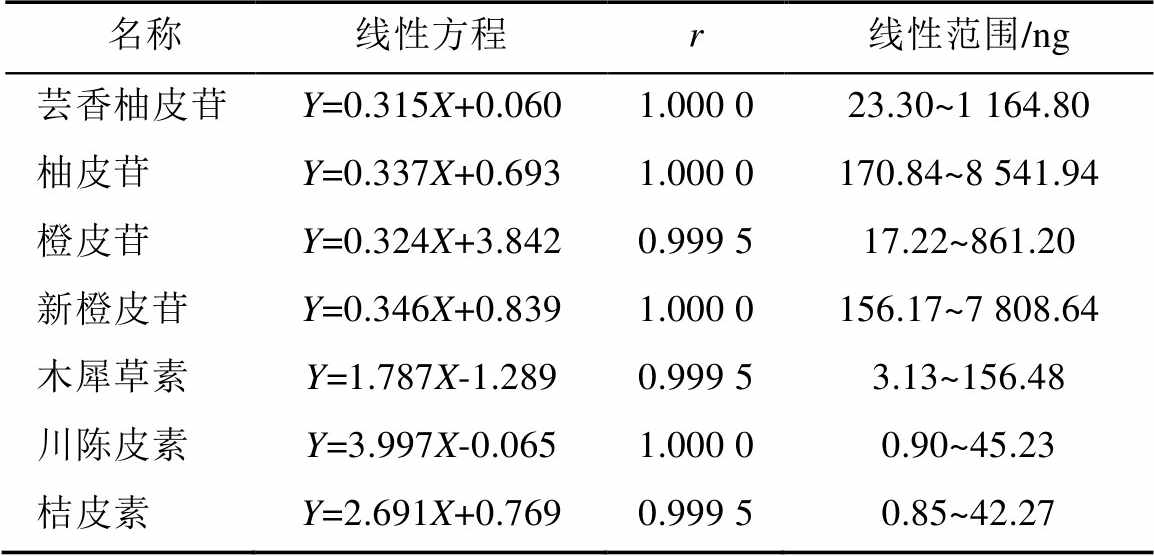
名称线性方程r线性范围/ng 芸香柚皮苷Y=0.315X+0.0601.000 023.30~1 164.80 柚皮苷Y=0.337X+0.6931.000 0170.84~8 541.94 橙皮苷Y=0.324X+3.8420.999 517.22~861.20 新橙皮苷Y=0.346X+0.8391.000 0156.17~7 808.64 木犀草素Y=1.787X-1.2890.999 53.13~156.48 川陈皮素Y=3.997X-0.0651.000 00.90~45.23 桔皮素Y=2.691X+0.7690.999 50.85~42.27
2.5.3 重复性试验 精密称量同一批号供试品(S1)6份,按“2.1”项下方法制备供试品溶液,按“2.3”项下色谱条件进行测定并计算含量。芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、木犀草素、川陈皮素、桔皮素的平均含量分别为7.318 3,52.453 9,4.870 5,50.616 9,0.129 7,0.277 2,0.174 7 mg·g-1,RSD分别为1.21%,0.75%,1.15%, 0.75%,2.69%,0.78%,0.53%,表明方法的重复性良好。
2.5.4 加样回收率试验 精密称取同一批供试品(S1)6份,分别精密加入芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、木犀草素、川陈皮素、桔皮素对照品,按“2.1”项下供试品制备方法制备并按“2.3”项下色谱条件进行测定,计算回收率和RSD,结果见表3。
2.5.5 稳定性实验 精密吸取“2.2”项下混合对照品溶液和重复性试验(S1)的供试品溶液,分别在0,6,9,16,20,25 h进样,按“2.3”项下色谱条件测定,记录峰面积,计算RSD。芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、木犀草素、川陈皮素、桔皮素的对照品峰面积的RSD(n=6)分别为1.7%,1.9%,2.6%,1.8%,1.4%,1.6%,1.8%;供试品峰面积RSD(n=6)分别为1.70%,0.50%,0.82%,0.54%,1.72%,0.48%,0.52%,表明对照品溶液和供试品溶液在25 h内基本稳定。
2.6 含量测定
分别取实验收集的11批样品,按“2.1”项下方法制备供试品溶液,按“2.3”项下色谱条件对7个成分进行检测,计算含量,结果见表4。
3 讨论
3.1 波长的选择
将混合对照品溶液用HPLC-DAD进行检测,经DAD光谱分析,结果在330 nm波长处可兼顾各成分的紫外吸收,故以330 nm作为检测波长。
表3 7种指标成分加样回收率测定结果
Tab. 3 Results of recovery test for 7 index componenes
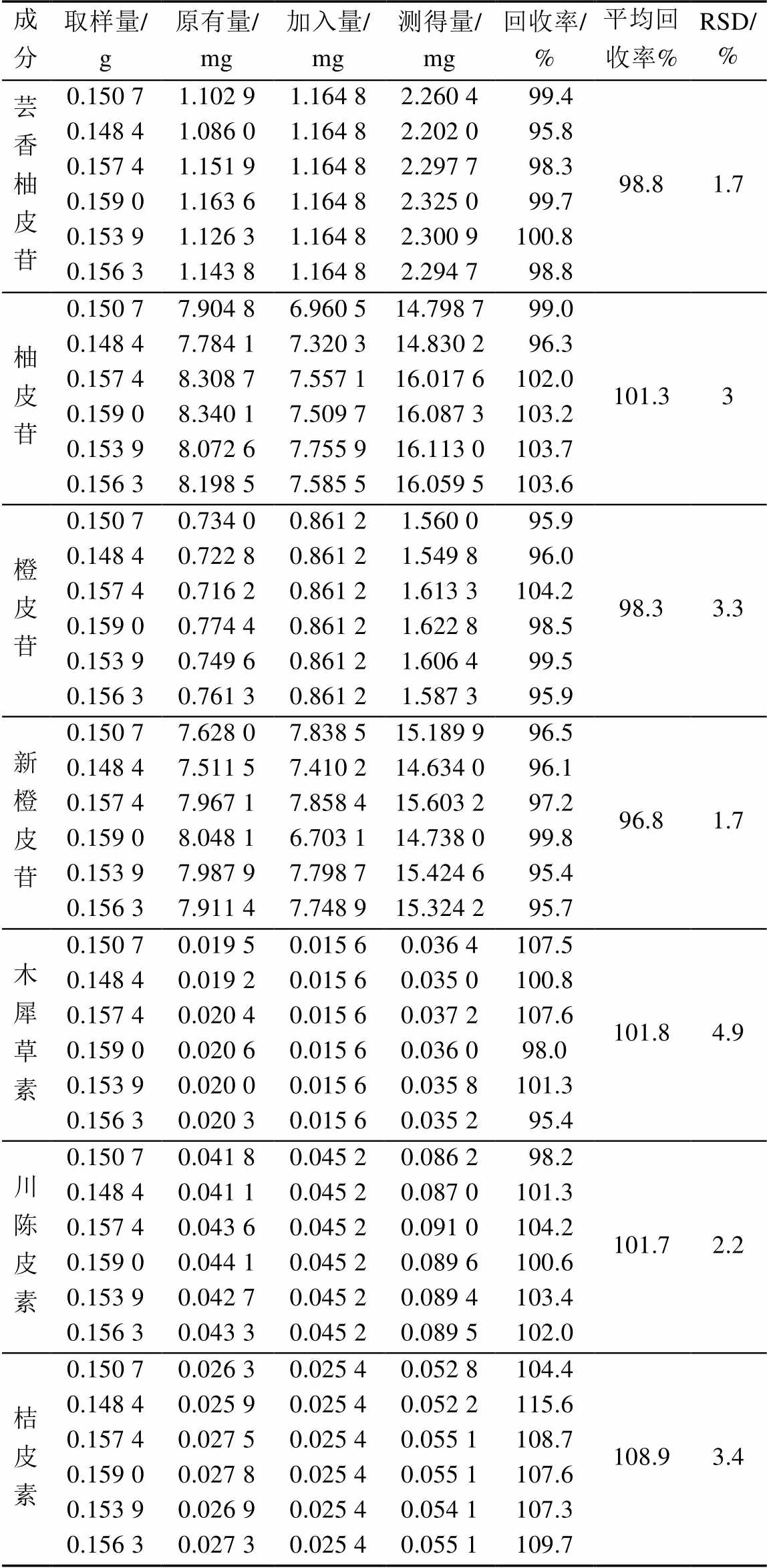
成分取样量/g原有量/mg加入量/mg测得量/mg回收率/%平均回收率%RSD/% 芸香柚皮苷0.150 71.102 91.164 82.260 4 99.498.81.7 0.148 41.086 01.164 82.202 0 95.8 0.157 41.151 91.164 82.297 7 98.3 0.159 01.163 61.164 82.325 0 99.7 0.153 91.126 31.164 82.300 9100.8 0.156 31.143 81.164 82.294 7 98.8 柚皮苷0.150 77.904 86.960 514.798 7 99.0101.33 0.148 47.784 17.320 314.830 2 96.3 0.157 48.308 77.557 116.017 6102.0 0.159 08.340 17.509 716.087 3103.2 0.153 98.072 67.755 916.113 0103.7 0.156 38.198 57.585 516.059 5103.6 橙皮苷0.150 70.734 00.861 21.560 0 95.998.33.3 0.148 40.722 80.861 21.549 8 96.0 0.157 40.716 20.861 21.613 3104.2 0.159 00.774 40.861 21.622 8 98.5 0.153 90.749 60.861 21.606 4 99.5 0.156 30.761 30.861 21.587 3 95.9 新橙皮苷0.150 77.628 07.838 515.189 9 96.596.81.7 0.148 47.511 57.410 214.634 0 96.1 0.157 47.967 17.858 415.603 2 97.2 0.159 08.048 16.703 114.738 0 99.8 0.153 97.987 97.798 715.424 6 95.4 0.156 37.911 47.748 915.324 2 95.7 木犀草素0.150 70.019 50.015 60.036 4107.5101.84.9 0.148 40.019 20.015 60.035 0100.8 0.157 40.020 40.015 60.037 2107.6 0.159 00.020 60.015 60.036 098.0 0.153 90.020 00.015 60.035 8101.3 0.156 30.020 30.015 60.035 2 95.4 川陈皮素0.150 70.041 80.045 20.086 2 98.2101.72.2 0.148 40.041 10.045 20.087 0101.3 0.157 40.043 60.045 20.091 0104.2 0.159 00.044 10.045 20.089 6100.6 0.153 90.042 70.045 20.089 4103.4 0.156 30.043 30.045 20.089 5102.0 桔皮素0.150 70.026 30.025 40.052 8104.4108.93.4 0.148 40.025 90.025 40.052 2115.6 0.157 40.027 50.025 40.055 1108.7 0.159 00.027 80.025 40.055 1107.6 0.153 90.026 90.025 40.054 1107.3 0.156 30.027 30.025 40.055 1109.7
表4 衢枳壳中7种指标成分的含量测定结果(n=2)
Tab. 4 Contents of seven componenes in Citrus changshan- huyou Y.B.Chang (n=2) mg·g-1
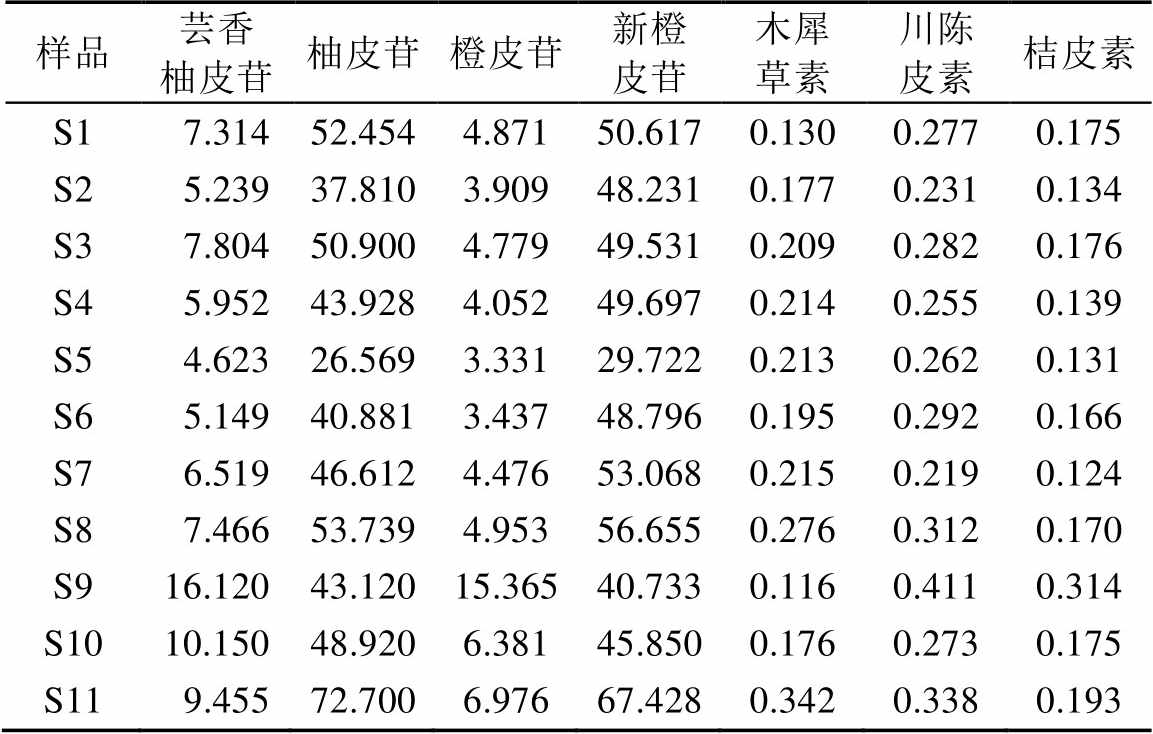
样品芸香柚皮苷柚皮苷橙皮苷新橙皮苷木犀草素川陈皮素桔皮素 S1 7.31452.4544.87150.6170.1300.2770.175 S2 5.23937.8103.90948.2310.1770.2310.134 S3 7.80450.9004.77949.5310.2090.2820.176 S4 5.95243.9284.05249.6970.2140.2550.139 S5 4.62326.5693.33129.7220.2130.2620.131 S6 5.14940.8813.43748.7960.1950.2920.166 S7 6.51946.6124.47653.0680.2150.2190.124 S8 7.46653.7394.95356.6550.2760.3120.170 S916.12043.12015.36540.7330.1160.4110.314 S1010.15048.9206.38145.8500.1760.2730.175 S11 9.45572.7006.97667.4280.3420.3380.193
3.2 供试品提取条件的优化
实验对提取溶剂(30%甲醇、50%甲醇、80%甲醇)、提取方式(超声、回流)、提取时间(10,20,30 min)、取样量(0.1,0.3,0.5 g),综合考虑色谱峰峰面积、分离度、峰形和供试品制备方法的简单高效,故确定供试品制备方法:取衢枳壳粗粉0.3 g精密称定,置25 ml量瓶中,加50%甲醇适量,超声20 min,放冷至室温,加50%甲醇至刻度,摇匀,离心,取上清液,即得。
3.3 色谱条件的优化
实验对Agilent Extend XDB C18(250 mm× 4.6 mm,5 μm)、Agilent Eclipse C18(250 mm× 4.6 mm,5 μm)、Kromasil 100-5 C18(250 mm× 4.6 mm,5 μm)和Diamond C18(250 mm×4.6 mm,5 μm)4根色谱柱进行分析,结果各组分均能达到有效分离;在25,30,35 ℃柱温条件下进行分析,不同柱温下各化合物均能达到有效分离,仅影响相对保留时间。综上表明实验色谱条件具有良好的耐用性。
芸香柚皮苷、柚皮苷和新橙皮苷成分在衢枳壳中含量相对较高,衢枳壳中芸香柚皮苷的含量范围为4.623~16.120 mg·g-1,柚皮苷的含量范围为26.569~72.700 mg·g-1,新橙皮苷的含量范围为29.722~67.428 mg·g-1,其余成分含量较低。不同采集地衢枳壳成分含量差异明显。本方法简便、高效、准确、可靠,可为衢枳壳质量全面、准确的评价和控制提供参考。
REFERENCES
[1] ZHAO X M, YE X Q, XU Y F, et al. Isolation and identification of effective constituents from the peels of Citrus paradisi cv. changshanhuyou and their pharmacological activities [J]. J Fruit Sci(果树学报), 2006, 23(3): 458-461.
[2] ZHAO X M, YE X Q, XU Y F, et al. Flavonoids in peels of Citrus changshan-huyou [J]. Chin Tradit Herb Drugs(中草药), 2003, 34(1): 14-16.
[3] ZHAO X M, YE X Q, XU Y F. Study on the extraction of flavonoids and antioxidation in Huyou peels [J]. J Fruit Sci(果树学报), 2003, 20(4): 261-265.
[4] Fang B, Ruiting Q I, Zhang Y. Active components and antioxidant activities of different parts of Citrus paradise fruit [J]. Food Sci(食品科学), 2015, 36(10): 158-163.
[5] WANG Y l, ZHANG J, CHU W j et al. Study on the hypoglycemic effects of Huyou fruits and the distribution of hypoglycemic components [J]. Chin Nutr Soc(营养学报), 2015, 37(2): 173-177.
[6] Song J F, Feng J Q, HU J h et al. Simultaneous determination for contents of naringin, hesperidin, and neohesperidin in flower of Citrus changshan-huyou by RP-HPLC [J]. Chin Tradit Herb Drugs(中草药), 2014, 45(6): 854-856.
[7] ZHAO Q C, MIN P, SHI G B, et al. Simultaneous determination of contents of narirutin, naringin and neohesperidin in Citrus changshan-huyou Y. B.Chang by HPLC [J]. J Shengyang Pharm Univ(沈阳药科大学学报), 2010, 27(9): 737-740.
[8] Zhi J M, Wang M. Determination of plymethoxylated favones in Citrus grandis peel by HPLC method [J]. Inf Tradit Chin Med(中医药信息), 2013, 30(2): 26-27.
(本文责编:曹粤锋)
Simultaneous determination of seven constituents in Citrus changshanhuyou Y. B. Chang by HPLC
HUANG Wenkang1, YUE Chao2, SONG Jianfeng3, DING Guoqin4, ZHANG Wenting2*, ZHAO Weiliang2*
(1.Zhejiang Chinese Medical University, Hangzhou 310053, China; 2.Zhejiang Institute for Food and Drug Control, Hangzhou 310052, China; 3.Quzhou Institute for Food and Drug Control, Quzhou 324000, China; 4.Hangzhou Hospital of Traditional Chinese Medicine, Hangzhou 310007, China)
ABSTRACT: OBJECTIVE To establish a method for the simultaneous determination of the contents of narirutin, naringin, hesperidin, neohesperidin, luteolin, nobiletin and hesperetin of Citrus changshan-huyou Y.B.Chang by HPLC.METHODS The HPLC method was adopted with Agilent Extend C18 column (250 mm×4.6 mm, 5 μm). The mobile phase was acetonitrile and 0.1% methanoic acid with gradient elution. The flow rate was 1 mL·min-1. The detection wavelength was 330 nm and column temperature was 30 ℃.RESULTS The linear relation of narirutin, naringin, hesperidin, neohesperidin, luteolin, nobiletin and hesperetin was excellent within the range of 23.30-1 164.80 ng, 170.84-8 541.91 ng, 17.22-861.20 ng, 156.17-7 808.64 ng, 3.13-156.48 ng, 0.90-45.23 ng, 0.85-42.27 ng (r≥0.999 5, n=6), and the mean recovery was 98.8%, 101.3%, 98.3%, 96.8%, 101.8%, 101.7%, 108.9%.CONCLUSION It is the first time to establish the HPLC method of the simultaneous determination for the seven contents of Citrus changshan-huyou Y.B.Chang. The method is simple, reliable and accurate, which provides the reference for the quality control for Citrus changshan-huyou Y.B.Chang.
KEY WORDS: Citrus changshan-huyou Y.B.Chang; HPLC; narirutin; naringin; hesperidin; neohesperidin; luteolin; nobiletin; hesperetin
中图分类号:R917.101
文献标志码:B
文章编号:1007-7693(2018)03-0404-04
DOI: 10.13748/j.cnki.issn1007-7693.2018.03.021
引用本文:黄文康, 岳超, 宋剑锋, 等. HPLC同时测定衢枳壳中7种指标成分的含量[J]. 中国现代应用药学, 2018, 35(3): 404-407.
收稿日期:2017-07-11
作者简介:黄文康,男,硕士生 Tel: 15858111454 E-mail: 846087613@qq.com
*通信作者:张文婷,女,博士,主任中药师 Tel: (0571)86459425 E-mail: leozhwt@163.com 赵维良,男,硕士,主任中药师 Tel: (0571)86452373 E-mail: zwl@zjyj.org.cn





