 (1)
(1)华育晖1,汪维佳1,王刚2,郑小丽1,沈雁3*
(1.杭州市第一人民医院集团,杭州市肿瘤医院药剂科,杭州 310002;2.杭州市第一人民医院药剂科,杭州 310006;3.中国药科大学,南京 211198)
摘要:目的制备奥沙利铂长循环脂质体(long-circulating liposome,LCL),并考察其在体内外的性质。方法利用逆相蒸发法制备奥沙利铂LCL,观察其形态,测定粒径电位、包封率、载药量等理化性质。采用SD大鼠进行药动学研究,考察脂质体在动物体内的药动学参数与生物利用度。结果奥沙利铂LCL的平均粒径为(195.1±1.8)nm,电位为(-29.53±0.57)mV,包封率为18%,载药量为2.4%。药动学研究结果显示,奥沙利铂的血浆清除率是LCL的71倍,LCL能够显著降低奥沙利铂的血浆清除率,延长药物体内滞留时间,LCL的药时曲线下面积(AUC)是奥沙利铂溶液的70倍,显著提高了生物利用度。结论本研究选择逆相蒸发法制备并筛选出具有合适包封率,低毒性和高药效的奥沙利铂LCL。
关键词:奥沙利铂;长循环脂质体;理化性质;药动学
奥沙利铂是继顺铂和卡铂之后的第3代铂类抗肿瘤药,也是至今为止唯一对结直肠癌具有显著活性的络铂类药物[1]。奥沙利铂通过与DNA结合,形成交联体,从而阻碍DNA的复制及转录,抑制肿瘤细胞分裂[2]。相比于前2代铂类药物,奥沙利铂在体内外的抗肿瘤作用效果好,抗瘤谱广,对结直肠癌、非小细胞肺癌和卵巢癌等实体瘤,以及对顺铂和卡铂的耐药肿瘤株均具有明显的抑制作用,临床上用于转移性结直肠癌的一线治疗[3-4]。然而,奥沙利铂具有严重的心脏和神经系统毒性,且血浆结合率很高,使得注射入体内后在肿瘤组织蓄积较少,难以达到治疗浓度。
脂质体是一种具有类生物膜双分子层结构的药物载体,由于其具有低毒、细胞亲和性及靶向性等特点,广泛作为药物、疫苗、营养物、诊断物质等生物学分子的有效载体使用[5-8]。普通脂质体与单核吞噬细胞系统MPS的亲和力较大,容易较快地被系统清除。而聚乙二醇(PEG)修饰的长循环脂质体(long-circulating liposome,LCL)可以增强药物的稳定性,减少与脂蛋白和吞噬系统的结合,从而降低清除率,延长作用时间,并增加药物在作用器官的聚集[9-11]。因此,该系统可以改变所包载药物的药动学性质及其在体内的分布。将奥沙利铂包载于LCL,利用LCL独特的性质,可以提高奥沙利铂的治疗效果,同时减轻奥沙利铂的不良反应,在临床上具有很大的开发应用前景。
本研究通过逆相蒸发法将奥沙利铂制备成LCL,通过理化性质考察及药动学研究,对其进行综合评价。
奥沙利铂(山东铂源药业有限公司,批号:1410010X);大豆卵磷脂A(SPC,上海太伟药业有限公司,纯度>80%,批号:20141204);功能化磷脂(DSPE-mPEG,上海艾韦特医药科技有限公司,批号:B30617);胆固醇(上海艾韦特医药科技有限公司,批号:B40333);DMSO(上海凌峰化学试剂有限公司,批号:20130118,分析纯);大豆卵磷脂B(SPC,德国Cargill公司,批号:159002;纯度>90%);大豆卵磷脂C(SPC,阿拉丁试剂,批号:G1517069;纯度>98%);蛋黄卵磷脂(PC-98T,上海艾韦特医药科技有限公司,批号:EL13025;纯度>98%);二硬脂酰基磷脂酰胆碱(DSPC,批号:X0212)、氢化大豆磷脂(HSPC,批号:B40932)(上海艾韦特医药科技有限公司);聚乙二醇辛基苯基醚(上海凌峰化学试剂有限公司,批号:20130220,分析纯);硝酸(南京化学试剂有限公司,批号:4091730466,优级纯);三氯甲烷、乙醚、葡萄糖、盐酸、硫酸等均为分析纯。
RE-52AA旋转蒸发仪(上海亚荣生化仪器厂);KQ-250型超声波清洗器(昆山市超声仪器有限公司);SCIENTZ-ⅡD超声波细胞粉碎仪(南京先欧仪器有限公司);ZetaPlus激光粒度仪(美国Brookhaven Instruments Corporation);HPLC系统(日本岛津公司);ZORBAX SB-C18色谱柱(5 μm,4.6 mm×250 nm,Agilent公司);iCE-3300原子吸收光谱仪(美国赛默飞世尔科技公司);SHZ-28A水浴恒温振荡器(太仓华美生化仪器厂)。
SD大鼠,♂,体质量(220±20)g(南京市青龙山动物繁殖场,N201611734)。实验动物合格证号:201611734。
采用逆相蒸发法制备奥沙利铂LCL。将卵磷脂(5% DSPE-mPEG)和胆固醇按质量比4∶1混合,加入乙醚和氯仿(2∶1)溶解,所得类脂溶液置于50 mL烧杯中。用注射器向烧杯中逐滴加入5 mL 4 mg·ml-1奥沙利铂5% 葡萄糖溶液。50% 功率超声5 min,得乳白色混悬液。40 ℃旋转蒸发去除有机相,形成白色凝胶状物质后继续旋转蒸发得奥沙利铂LCL溶液。过0.22 μm微孔滤膜2次,降低脂质体粒径。普通脂质体以同上方法制备,但不含 DSPE-mPEG。脂质体制备中进行了单因素筛选。
1.4.1 磷脂种类 考察大豆卵磷脂A、大豆卵磷脂B、大豆卵磷脂C、PC-98T、DSPC、HSPC共计6种磷脂制备得到的奥沙利铂LCL,方法同上。
1.4.2 药脂比 药脂比对包载水溶性药物脂质体性质的包封率具有较大影响。本实验考察了药脂比为1∶15,1∶12.5,1∶10,1∶7.5,1∶5条件下制备得到的奥沙利铂脂质体的性质。
1.4.3 溶剂种类和比例 溶剂种类和比例对逆相蒸发法的中间步骤,探头超声制备反相胶束有一定的影响,因此本实验考察了常用溶剂三氯甲烷、乙醚及其混合溶液对奥沙利铂LCL性质的影响。
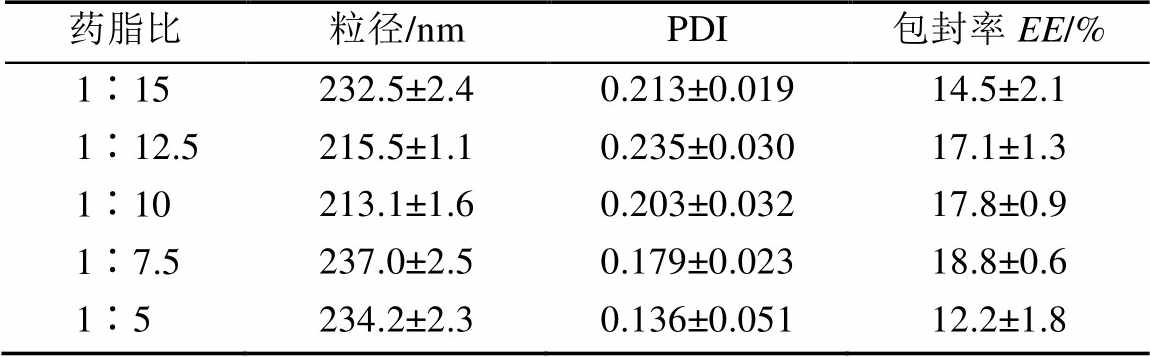
采用动态光散射法(DLS)测定脂质体的粒径及其分布以及Zeta电位,通过透析法除去游离奥沙利铂,用同倍体积的10% Triton于60 ℃水浴10 min破坏脂质体,然后采用HPLC测定脂质体的包封率、载药量及放置一段时间后的泄漏量。按如下公式,计算奥沙利铂的包封率和载药量。
 (1)
(1) (2)
(2)
分别取奥沙利铂LCL 1 mL放置于4 ℃和37 ℃ 1个月,测定其粒径、PDI和药物保留率。透析过夜后破坏脂质体检测药物浓度,计算药物的保留率。
1.7.1 药动学含量测定的方法学验证 选择石墨炉原子吸收光谱法测定大鼠体内奥沙利铂的浓度。原子吸收色谱条件:灯电流为10.0 mA;波长为265.9 nm;光谱通带宽度为0.2 nm;载气为高纯氩气,流量为0.3 L·min-1;进样量为20 μL。升温程序:100 ℃干燥60 s;1 200 ℃灰化8 s;2 700 ℃原子化3 s;2 750 ℃清除残留3 s。用铂标准品建立原子吸收检测标准曲线,考察专属性,加样回收率及精密度。
1.7.2 动物处理 取12只体质量在(220±20)g内的大鼠,随机分为3个实验组,A组为奥沙利铂市售溶液组,B组为普通脂质体组,C组为奥沙利铂LCL,设定每组4只大鼠,分别经尾静脉给药,给药量按奥沙利铂净含量计算为5 mg·kg-1。分别于给药后5,15,30 min,1,2,4,8,12,24,48 h共10个时间点分别从大鼠眼眶取血约0.75 mL,静置于肝素化离心管中10 min后待用。
1.7.3 血浆样品处理 将静置10 min后的血浆样品置于高速冷冻离心机中,低温下4 000 r·min-1离心20 min,吸取上层血浆待用。每份血浆样品取160 μL置于10 mL量瓶中,并加入等体积1% Triton溶液破坏脂质体,并用2%王水溶液消解稀释定容后,进原子吸收光谱仪检测血浆样品中的铂含量。
1.7.4 数据处理 记录检测的铂响应值,并根据标准曲线计算各时间点血浆样品中的奥沙利铂的含量。以时间(h)为横坐标,铂浓度(ng·ml-1)为纵坐标绘制奥沙利铂的药时曲线图,通过药时曲线利用药动学软件WinNonlin 5.2计算脂质体在体内的药动学参数。
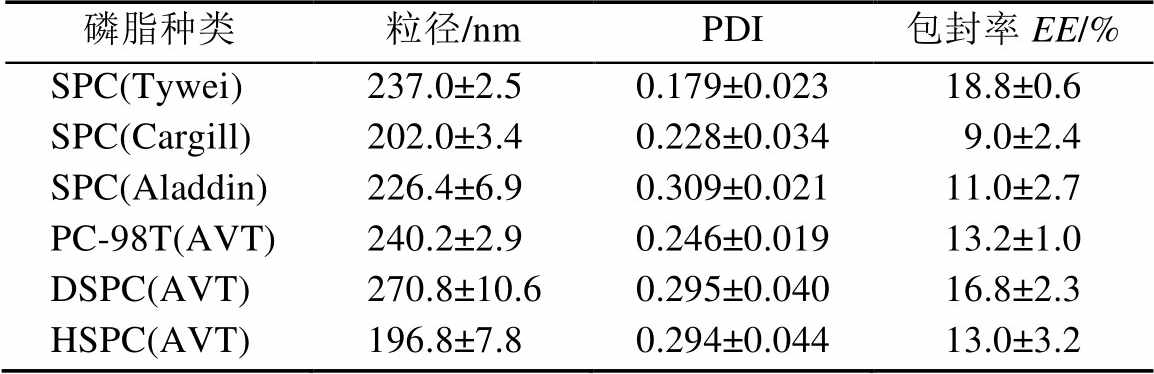
2.1.1 磷脂种类对脂质体性质的影响 本实验在制备过程中选用了不同纯度、不同生产厂家的卵磷脂。表1的实验结果表明,磷脂本身材料对奥沙利铂脂质的体粒径和包封率有显著影响,这可能是由于磷脂所带电荷、分子间作用力等的不同导致了脂质体形态、结构的不同引起的。其中,采用上海太伟药业有限公司生产的大豆卵磷脂制备的奥沙利铂LCL包封率明显高于其他磷脂,且多分散系数(PDI)较小,作为后续实验的磷脂。
表1 磷脂种类对包封率、粒径和PDI的影响(n=3,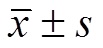 )
)
Tab. 1 Effects of types of phosphatidylcholine on the particle size, PDI and entrapment efficiency(n=3,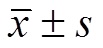 )
)
2.1.2 药脂比对脂质体性质的影响 药脂比是影响脂质体产品包封率和后期工业转化的重要因素,表2的实验结果表明奥沙利铂LCL的包封率随药脂比先增大后减小,当药脂比为1∶7.5时达到最大。
表2 药脂比对包封率、粒径和PDI的影响(n=3,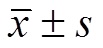 )
)
Tab. 2 Effects of drug to lipid on the partical size, PDI and entrapment efficiency (n=3,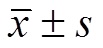 )
)
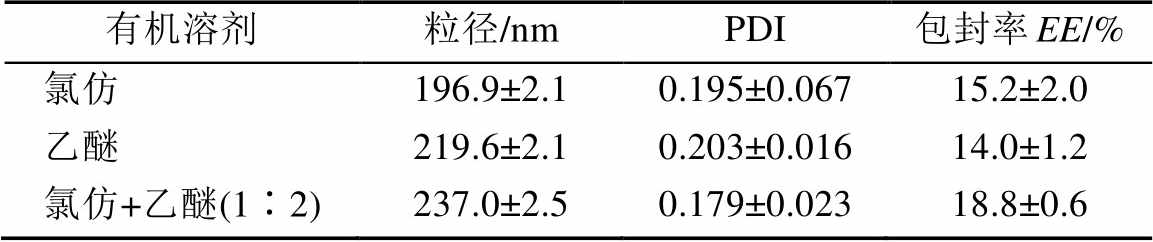
2.1.3 溶剂种类和比例对脂质体性质的影响 分别采用了氯仿、乙醚及二者的混合溶液作为有机相制备奥沙利铂LCL,表3的结果表明采用氯仿和乙醚的混合溶剂作为有机相时制备得到的奥沙利铂LCL包封率较高。在制备中将水相加入混合溶剂的有机相中,由于其密度介于氯仿和乙醚之间,将会在有机相层中形成小液滴,有利于乳状液的形成,因此制备得到的奥沙利铂LCL包封率较高。
表3 有机溶剂对包封率,粒径和PDI的影响(n=3,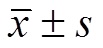 )
)
Tab. 3 Effects of ratio of organic solvents on the particle size, PDI and entrapment efficiency (n=3,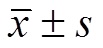 )
)
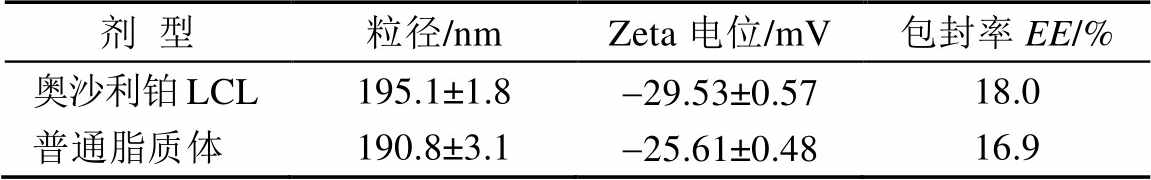
奥沙利铂LCL的粒径电位和包封率载药量见表 4。奥沙利铂LCL的粒径在200 nm左右,PDI≤0.2,说明粒径分布较为均匀,粒子大小趋于一致。奥沙利铂LCL的电位在-29 mV左右,表明脂质体的电荷稳定性,脂质体的包封率在20% 左右,相比于疏水性药物,奥沙利铂的包封率较低,但是得到的包封率与其他文献中的结果基本保持一致[12-14]。
表4 奥沙利铂LCL的物理化学性质
Tab.4 Physical and chemical properties of oxaliplatin LCL
将奥沙利铂LCL分别在4 ℃和37 ℃放置1个月后,药物泄漏量见表 5。可知,奥沙利铂LCL在4 ℃条件下均有少量泄漏,但<5%,粒径和PDI无明显改变,而在常温下,泄露量接近30%,且粒径增大,PDI升高,表明其需做成冻干粉针制剂以增加其稳定性,表明天然磷脂由于其本身的相变温度较低,使得其稳定性有所降低。
表5 奥沙利铂LCL的稳定性考察(n=3)
Tab. 5 Stability investigation of oxaliplatin LCL(n=3)

2.3.1 体内试验含量测定的方法学验证
2.3.1.1 专属性 奥沙利铂的石墨炉原子吸收光谱图见图1。从图中可以看出,奥沙利铂的光谱峰峰形良好,无干扰,脂质体、血浆、Triton等辅料和溶剂均不会对铂的含量测定造成影响。
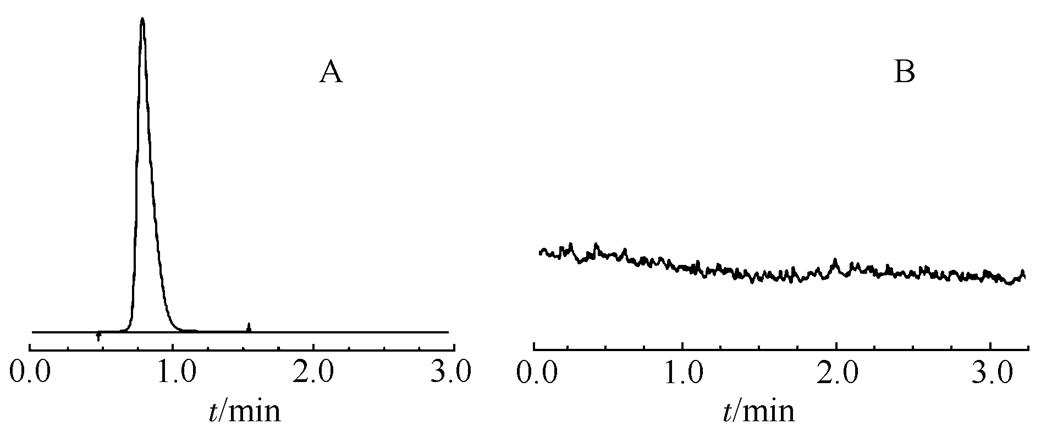
图1 石墨炉原子吸收光谱图
A-奥沙利铂原料药;B-空白脂质体。
Fig. 1 The graphite furance atomic absorption spectrogram
A-oxaliplatin crude drug; B-blank liposome.
2.3.1.2 线性 以奥沙利铂浓度X为横坐标,峰高Y为纵坐标作图并进行线性回归,得到的线性回归方程为Y=0.001 88X+0.002 1,r=0.998 4,线性良好。
2.3.1.3 精密度 铂溶液含量测定的日内精密度和日间精密度的RSD均<5%,实验结果符合要求,结果见表6。
表6 铂溶液含量测定的精密度(n=3)
Tab. 6 Precision of detection method of platinum standard solution (n=3)

2.3.1.4 加样回收率 3组不同浓度的标准铂溶液的回收率分别为103.36%,100.10%和100.96%,均在95%~105%的回收率要求范围内,回收率良好,结果见表7。
2.3.2 大鼠体内药动学 大鼠分别给予奥沙利铂、奥沙利铂普通脂质体和奥沙利铂LCL后的药时曲线见图2。
表7 铂溶液含量测定的回收率
Tab. 7 Recovery of detection method of platinum standard solution

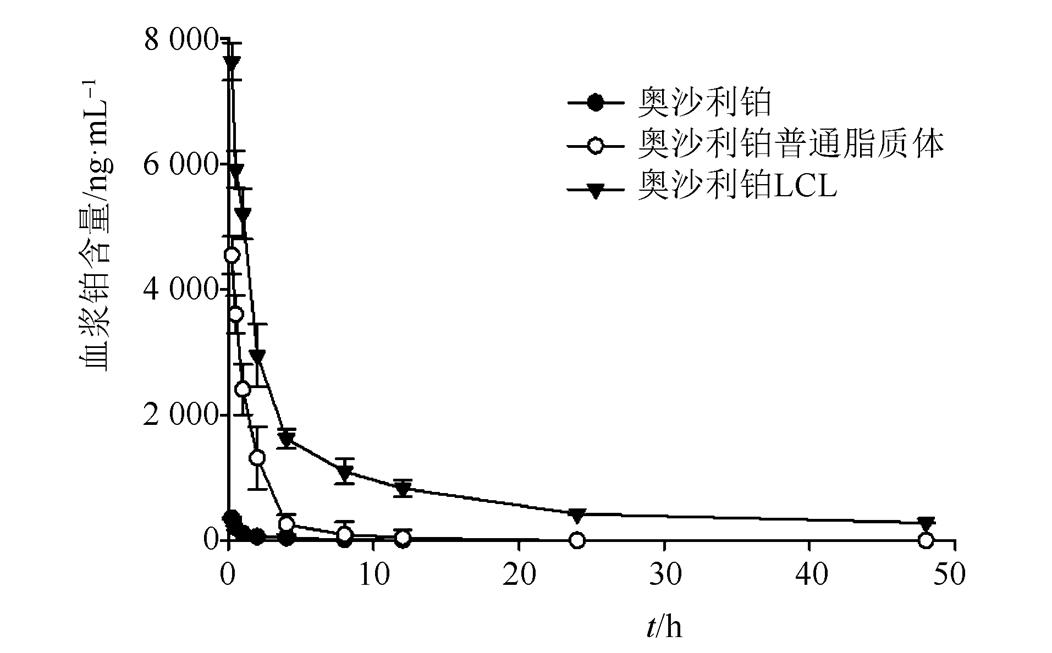
图2 奥沙利铂、奥沙利铂普通脂质体和奥沙利铂LCL的血浆铂含量-时间曲线(以4.4 mg·kg-1的给药剂量计) (n=4)
Fig. 2 Plasma platinum concentration-time curves of oxaliplatin(oxal), oxaliplatin liposome and oxaliplatin LCL following intravenous injection in SD rats at a dosage of 4.4 mg·kg-1(n=4)
由图2可知,给予市售溶液后,大鼠血浆中的铂浓度在前4 h内迅速降低,表明奥沙利铂游离药物容易被体内清除,同时给与奥沙利铂LCL的大鼠体内铂血浆浓度在各个时间点的样品都要明显高于市售奥沙利铂注射液。主要原因可能是奥沙利铂本身由于暴露于体液环境中,而脂质体剂型包载奥沙利铂从而有效地避免了奥沙利铂在体内的这种结合和被清除,也证明了脂质体作为一种新型制剂的独特优点。另一方面,奥沙利铂LCL在体内滞留时间明显高于奥沙利铂脂质体和市售奥沙利铂注射液,表明这种LCL表面修饰的PEG能够逃避单核吞噬细胞系统的清除,实现在血液中的长循环作用不被清除。
2.3.3 数据分析 采用药动学软件WinNonlin 5.2将血药浓度对单剂量静脉注射一室、二室模型分别进行拟合,实验结果见表8,并计算AIC值,选择最小的AIC值为最优拟合模型。实验结果表明,相比之下,二室模型拟合下的AIC值最小,因此初步断定静脉注射奥沙利铂、奥沙利铂脂质体以及奥沙利铂LCL均符合二室模型,根据模型拟合参数推导出它们的血浆药动学方程分别如下:
COxaliplatin=550.04e-3.08t+102.28e-0.22t (3)
CLipoxal=815.82e-1.59t+102.44e-0.19t(4)
CLCL=5 068.47e-0.88t+467.70e-0.25t(5)
静脉注射奥沙利铂注射液、奥沙利铂脂质体及奥沙利铂LCL的主要药动学参数见表9。从表中可看出,奥沙利铂LCL的生物利用度是奥沙利铂注射剂的71.5倍,大大增加了奥沙利铂在体内的治疗浓度,从中可以得出,脂质体作为新型制剂,能够显著降低奥沙利铂的清除率,提高其在血浆中的浓度和稳定性。奥沙利铂LCL的半衰期增加显著,证明了LCL在体内的稳定作用,从而为奥沙利铂在肿瘤部位的蓄积并充分发挥奥沙利铂更好的抗癌作用提供科学依据。
表8 奥沙利铂、奥沙利铂普通脂质体和奥沙利铂LCL的隔室模型分析(n=4)
Tab. 8 Compartmental analysis of plasma data after injection of oxaliplatin, oxaliplatin liposome and oxaliplatin- loaded LCL (n=4)
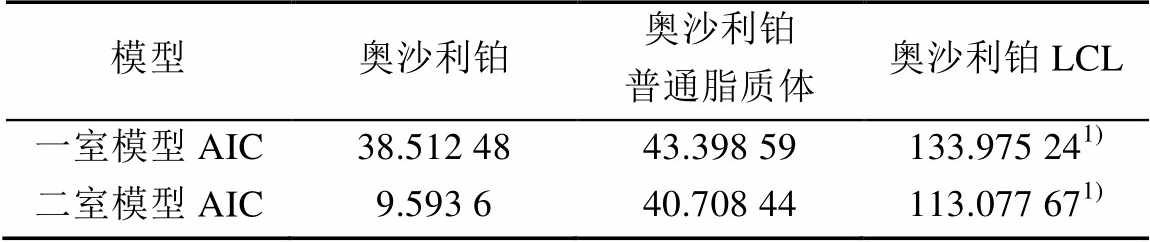
注 :与奥沙利铂普通脂质体比较,1)p<0.01。
Note: Compared with oxaliplatin liposome group,1)p<0.01.
表9 奥沙利铂、奥沙利铂普通脂质体和奥沙利铂LCL的药动学参数(n=4)
Tab. 9 Pharmacokinetic parameters of oxaliplatin, oxaliplatin liposome and oxaliplatin-loaded LCL after injection (n=4)
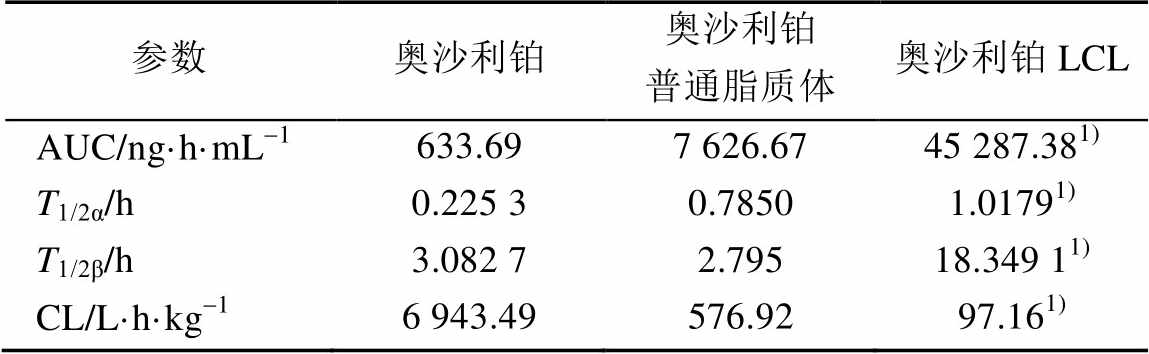
注 :与奥沙利铂普通脂质体比较,1)p<0.01。
Not e: Compared with oxaliplatin liposome group,1)p<0.01.
脂质体作为一具有类生物膜双分子层结构的药物载体,具有低毒、细胞亲和性和靶向性等特点,在新型抗肿瘤药物的研究中具有广阔的应用前景。奥沙利铂有其独特优点的同时,也存在铂类药物的一般不良反应,如出现特异的心脏毒性、具有明显的周围神经毒性等,为此,通过脂质体载药等制剂新技术降低其不良反应,是近年来奥沙利铂新剂型和新制剂研发的重点和方向。本项目旨在利用脂质体的安全性和对肿瘤的被动靶向性提升奥沙利铂的治疗效果,同时减轻奥沙利铂的不良反应。
笔者设计并合成了一种具有长循环效果的奥沙利铂脂质体,并进行了体内外的初步评价。结果发现,该药物最终产品质量稳定,且具有较高的包封率和稳定性。该脂质体能够明显延长奥沙利铂在体内的滞留时间,降低了奥沙利铂的清除率,达到了长循环的效果,明显提高了奥沙利铂的生物利用度。研究结果证明本研究设计的奥沙利铂LCL安全、有效、稳定、质量可控,具有很大的开发前景,有望成为新型纳米抗癌制剂。
References
[1] IBRAHIM A, HIRSCHFELD S, COHEN M H, et al. FDA drug approval summaries: oxaliplatin [J]. Oncologist, 2004, 9(3): 8-12.
[2] SUZUKI R, TAKIZAWA T, KUWATA Y, et al. Effective anti-tumor activity of oxaliplatin encapsulated in transferrin- PEG-liposome [J]. Int J Pharm, 2008, 346(1): 143-150.
[3] RAYMEND E, FAIVRE S, WOYNAROWSKI J M, et al. Oxaliplatin: mechanism of action and antineoplastic activity [J]. Semin Oncol, 1998, 25(2): 4-12.
[4] NOBILI S, CHECCACCI D F, DEL S, et al. Bimonthly chemotherapy with oxaliplatin, irinotecan, infusional 5-fluorouracil/folinic acid in patients with metastatic colorectal cancer pretreated with irinotecan- or oxaliplatin-based chemotherapy [J]. J Chemother, 2008, 20(5): 622-631.
[5] LI W, ZHANG C L, LIU D. Modern research of Calculus Bovis (Third): preparation technology [J]. Her Med(医药导报), 2017, 36(3): 237-240.
[6] TORCHILIN V P, Recent advances with liposomes as pharmaceutical carries [J]. Nat Rev Drug Dislov, 2005, 4(2): 145-160.
[7] HOFHEINZ R D, GNAD S U, BEYER U, et al. Liposomal encapsulated anti-cancer drugs [J]. Anticancer Drugs, 2005, 16(7): 691-707.
[8] GENG L L, SUI L, ZHANG M M, et al. Preparation and quality evaluation of pH-sensitive chrysophanol liposomes [J]. Chin J New Drugs(中国新药杂志), 2017, 27(10): 1189-1193.
[9] ZHANG L. Long circulating liposomes delivery system in diagnosis and treatment of tumor [J]. Her Med(医药导报), 2017, 36(5): 463-468.
[10] FANG J, NAKAMURA H, MAEDA H. The EPR effect: Unique features of tumor blood vessels for drug delivery, factors involved, and limitations and augmentation of the effect [J]. Adv Drug Deliv Rev, 2011, 63(3): 136-151.
[11] GRESIH K. Enhanced permeability and retention (EPR) effect for anticancer nanomedicine drug targeting [J]. Methods Mol Biol, 2010(624): 25-37.
[12] ZALBA S, NAVARRO I, TROCOTIA I F, et al. Application of different methods to formulate PEG-liposomes of oxaliplatin: evaluationin vitroandin vivo[J]. Eur J Pharm Biopharm, 2012, 81(2): 273-280.
[13] 杨美燕. 奥沙利铂长循环热敏脂质体研究[D]. 北京: 军事医学科学院毒物药物研究所, 2007.
[14] LIU X P, GEN D Q, XU H X, et al. Research on the preparation of Oxaliplatin liposome [J]. J Wuhan Univ Technol(武汉理工大学学报), 2008, 30(9): 50-53.
(本文责编:曹粤锋)
Preparation and evaluation of oxaliplatin long-circulating liposomes
HUA Yuhui1, WANG Weijia1, WANG Gang2, ZHENG Xiaoli1, SHEN Yan3*
(1.Pharmacy Department of Hangzhou Cancer Hospital, Hangzhou First People’s Hospital Group, Hangzhou 310002, China; 2.Pharmacy Department of Hangzhou First People’s Hospital, Hangzhou 310006, China; 3.China pharmaceutical university, Nanjing 211198, China)
Abstract: ObjectiveTo prepare oxaliplatin long-circulating liposomes(LCL) and perform evaluationsin vitroandin vivo.MethodsOxaliplatin-loaded LCL were prepared by reverse phase evaporation method. Physicochemical properties of LCL were investigated, including particle size and encapsulation efficiency(EE). Pharmacokinetic study was conducted on rat model.ResultsThe average particle size of oxaliplatin LCL was (195.1±1.8) nm and the potential was (-29.53±0.57) mV. In addition, the encapsulation efficiency was 18% and the drug loading was 2.4%. Pharmacokinetic studies showed that the plasma clearance rate of oxaliplatin is 71-fold LCL, so LCL could significantly reduce the plasma clearance rate of oxaliplatin and prolong drug the residence timein vivo. The AUC of LCL was 70-fold of that for oxaliplatin solution which significantly improved the bioavailability.ConclusionThis study select reverse phase evaporation method to prepare and obtain the optimal oxaliplatin LCL with suitable entrapment efficiency, low toxicity and high efficacy.
Key words:oxaliplatin; long-circulating liposome; physicochemical property; pharmacokinetic
中图分类号:R941
文献标志码:B
文章编号:1007-7693(2018)03-0335-05
DOI:10.13748/j.cnki.issn1007-7693.2018.03.007
引用本文:华育晖,汪维佳, 王刚, 等. 奥沙利铂长循环脂质体的制备和体内外评价[J]. 中国现代应用药学, 2018, 35(3): 335-339.
收稿日期:2017-06-27
作者简介:华育晖,女,副主任药师 Tel: 15958003407 E-mail: hyh87652698@163.com
*通信作者:沈雁,女,博士,副教授 Tel: 13814045497 E-mail: shenyan19820801@126.com