UHPLC同时测定进口西洋参4个化学成分的含量
陆静娴,施贝,董婷,陈碧莲,马临科,祝明*
(浙江省食品药品检验研究院,杭州 310000)
摘要:目的建立UHPLC同时测定进口西洋参中4个活性成分(人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd)含量的方法。方法采用Zorbax SB C18(2.1 mm×100 mm, 1.8 μm)色谱柱,以乙腈为流动相A,水为流动相B,梯度洗脱,流速0.5 mL·min-1,柱温30 ℃,检测波长为203 nm。结果4种成分的分离度良好,且在各自浓度范围内呈现良好的线性关系(r≥0.999 9),平均回收率为95.7%~100.3%(RSD1.4%~1.8%)。结论该方法操作简单,缩短了分析时间,重复性好,为评价进口西洋参的质量提供了可靠的方法。
关键词:西洋参;超高效液相色谱法;人参皂苷Rg1;人参皂苷Re;人参皂苷Rb1;人参皂苷Rd
西洋参为五加科植物西洋参Panax quinquefoliumL.的干燥根,系栽培品[1]。研究表明,西洋参具有抗氧化,抗自由基等功效,具有镇静、镇痛、催眠、镇惊、解热、全身性抗缺氧、抗疲劳、促进学习记忆等作用[2-4]。西洋参中的化学成分包括皂苷类、挥发油类、氨基酸类、糖类和聚炔类等,其主要活性成分为皂苷类[5]。进口西洋参标准收载于《儿茶等43种进口药材质量标准》,以2个普通液相系统分别对西洋参中人参皂苷Rg1和人参皂苷Re的总量及人参皂苷Rb1的含量进行测定。但采用常规HPLC对皂苷类成分进行分析往往时间较长[6],且各成分间较难达到完全分离,因此有必要对分析方法进行改进。近年来,由于超高效液相色谱法(UHPLC)的使用,很多成分复杂的中药都达到了良好的分离,同时分析时间较短[7]。刘莉等[8-10]采用UHPLC对西洋参中人参皂苷Rg1、人参皂苷Re和人参皂苷Rb1进行定量分析,提高了分析效率的同时又节约溶剂。研究表明,除上述3种成分外,人参皂苷Rd同样具有较好的活性,可以通过抑制自由基介导的脂质过氧化反应,使细胞膜免受氧自由基的影响,保护肾近端小管[11]。同时,人参皂苷Rd能使高糖状态下HMC(human message cells)对TGF-β1合成和分泌减少,可能是防治糖尿病肾病的有效成分之一[12]。综上,本研究采用UHPLC对上述4种皂苷类成分进行同时分离测定。
1 仪器与试药
Agilent 1290型UHPLC液相色谱仪、Agilent 1100型HPLC液相色谱仪(Agilent科技有限公司);戴安U3000RSLC型高效液相色谱仪(赛默飞世尔科技);AE240型电子天平(梅特勒-托利多);Milli-Q超纯水处理系统(默克生命科学)。
人参皂苷Rg1对照品(批号:110703-201128;纯度为93.4%)、人参皂苷Re对照品(批号:110754-201324;纯度为92.7%)、人参皂苷Rb1对照品(批号:110705-200306;纯度为92.9%)和人参皂苷Rd对照品(批号:111818-201001;纯度为94.4%)均由中国食品药品检定研究院提供。甲醇、正丁醇均为分析纯;乙腈为色谱纯。西洋参样品共23批,经浙江省食品药品检验研究院中药所郭增喜主任中药师鉴定为五加科植物Panax quinquefoliumL.的根茎,供样信息详见表1。
表1 进口西洋参样品来源
Tab. 1 Origins of importedPanax quinquefoliumL.

编号批号来源供样单位质量/g 1XYS-ZJS-1加拿大广州普宁药材市场50 2XYS-ZJS-2美国广州清平药材市场100 3XYS-ZJS-3加拿大浙江英特医药有限公司500 4XYS-ZJS-4加拿大浙江震元医药公司250 5XYS-ZJS-5加拿大浙江英特医药有限公司500 6XYS-ZJS-6加拿大杭州华东医药股份有限公司1 500 7XYS-ZJS-7加拿大衢州南孔中药有限公司50 8XYS-ZJS-8加拿大温哥华广东普宁药材市场200 9XYS-ZJS-9加拿大多伦多广东普宁药材市场250 10XYS-ZJS-10美种广东普宁药材市场100 11XYS-ZJS-11美种广东普宁药材市场100 12XYS-ZJS-12加货多伦多软肉广东普宁药材市场250 13XYS-ZJS-13加货多伦多硬肉广东普宁药材市场250 14XYS-ZJS-14加拿大安大略广州市食品药品检验所50 15XYS-ZJS-15美国威斯康辛广州市食品药品检验所15 16XYS-ZJS-16美国威斯康辛广州市食品药品检验所15 17XYS-ZJS-17美国威斯康辛广州市食品药品检验所15 18XYS-ZJS-18美国威斯康辛广州市食品药品检验所15 19XYS-ZJS-19美国北京市药品检验所50 20XYS-ZJS-20美国北京市药品检验所50 21XYS-ZJS-21美国北京市药品检验所50 22XYS-ZJS-22美国北京市药品检验所50 23XYS-ZJS-23美国威斯康辛广州市食品药品检验所15
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液 取人参皂苷Rg1对照品、人参皂苷Re对照品、人参皂苷Rb1对照品和人参皂苷Rd对照品适量,精密称定,加甲醇制成每1 mL各含人参皂苷Rg10.1 mg、人参皂苷Re 0.4 mg、人参皂苷Rb11 mg、人参皂苷Rd 0.3 mg的混合溶液,即得。
2.1.2 供试品溶液 取本品粉末(过三号筛)约0.75 g,精密称定,置具塞锥形瓶中,精密加入水饱和的正丁醇50 mL,称定质量,置水浴加热回流提取2 h,放冷,再称定质量,用水饱和正丁醇补足减失的质量,摇匀,滤过。精密量取续滤液25 mL,置蒸发皿中,蒸干,残渣加50%甲醇适量使溶解,转移至10 mL量瓶中,加50%甲醇至刻度,摇匀,滤过,取续滤液,即得。
2.2 色谱条件
Agilent Zorbax SB C18色谱柱(2.1 mm× 100 mm,1.8 μm);流动相:乙腈(A)-水(B),梯度洗脱(0~9.5 min,20%A;9.5~11.5 min,20%→75%A;11.5~25 min,75%→60%A);检测波长:203 nm;流速:0.5 mL·min-1;进样量:2 µL。在上述色谱条件下,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd与其邻近峰均可达到基线分离,见图1。
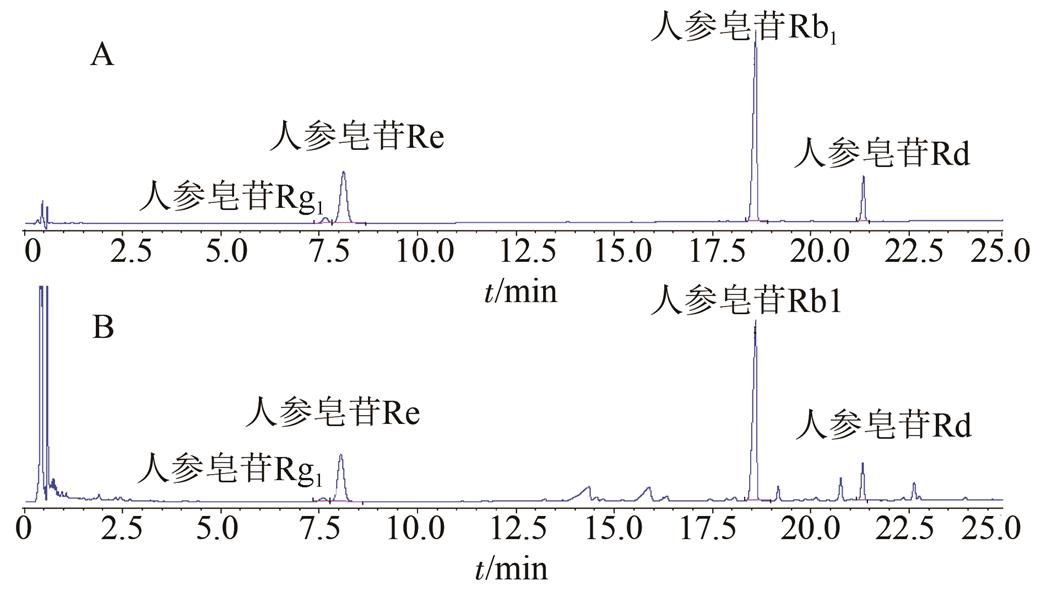
图1 西洋参含量测定色谱图
A-混合对照品;B-西洋参供试品溶液。
Fig. 1 Typical HPLC chromatograms ofPanax quinquefoliumL.
A-mixed standards; B-samples ofPanax quinquefoliumL..
2.3 方法学验证
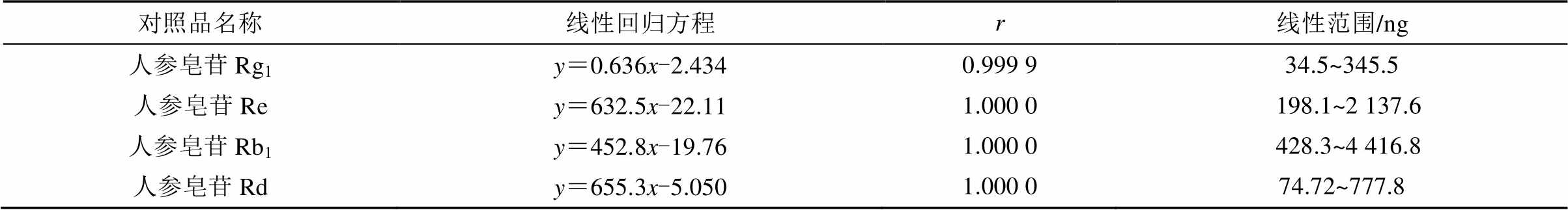
2.3.1 线性关系 精密称取人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd对照品适量,分别用甲醇溶解制成浓度为0.069 1,0.682 5,0.962 2,0.239 0 mg·mL-1的混合对照品溶液,精密吸取混合对照品溶液0.5,1,1.5,2,2.5,3,4,5 µL,注入液相色谱仪,按“2.2”项下色谱条件测定,以色谱峰面积为纵坐标(y),以进样量(ng)为横坐标(x),进行线性回归,结果表明,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rd进样量分别在34.5~345.5,198.1~2 137.6,428.3~4 416.8和74.72~777.8 ng内与峰面积呈良好线性关系,结果见表2。
表2 西洋参4个成分线性关系考察表
Tab. 2 Linear relationship of 4 components inPanax quinquefoliumL.
对照品名称线性回归方程r线性范围/ng 人参皂苷Rg1y=0.636x-2.4340.999 934.5~345.5 人参皂苷Rey=632.5x-22.111.000 0 198.1~2 137.6 人参皂苷Rb1y=452.8x-19.761.000 0 428.3~4 416.8 人参皂苷Rdy=655.3x-5.0501.000 074.72~777.8
2.3.2 仪器精密度试验 取供试品溶液,按“2.2”项下色谱条件测定,重复进样6次,测定峰面积,结果人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rd的RSD分别为1.0%,0.1%,0.2%和0.2%,表明仪器精密度良好。
2.3.3 稳定性试验 取同一供试品溶液,分别间隔0,3,9.5,13,15,18 h按“2.2”项下色谱条件测定1次,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd峰面积的RSD分别为1.5%,0.3%,0.4%和0.7%,结果显示供试品溶液在18 h内基本稳定。
2.3.4 重复性试验 取同一批样品(批号:XYS-ZJS-6)6份,按“2.1.2”项下方法制备6份供试品,按“2.2”项下色谱条件测定,结果人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd的平均含量分别为0.93 mg·g-1(RSD 1.3%),12.44 mg·g-1(RSD 1.0%),38.59 mg·g-1(RSD 1.0%)和3.85 mg·g-1(RSD 1.5%),说明方法重复性好。
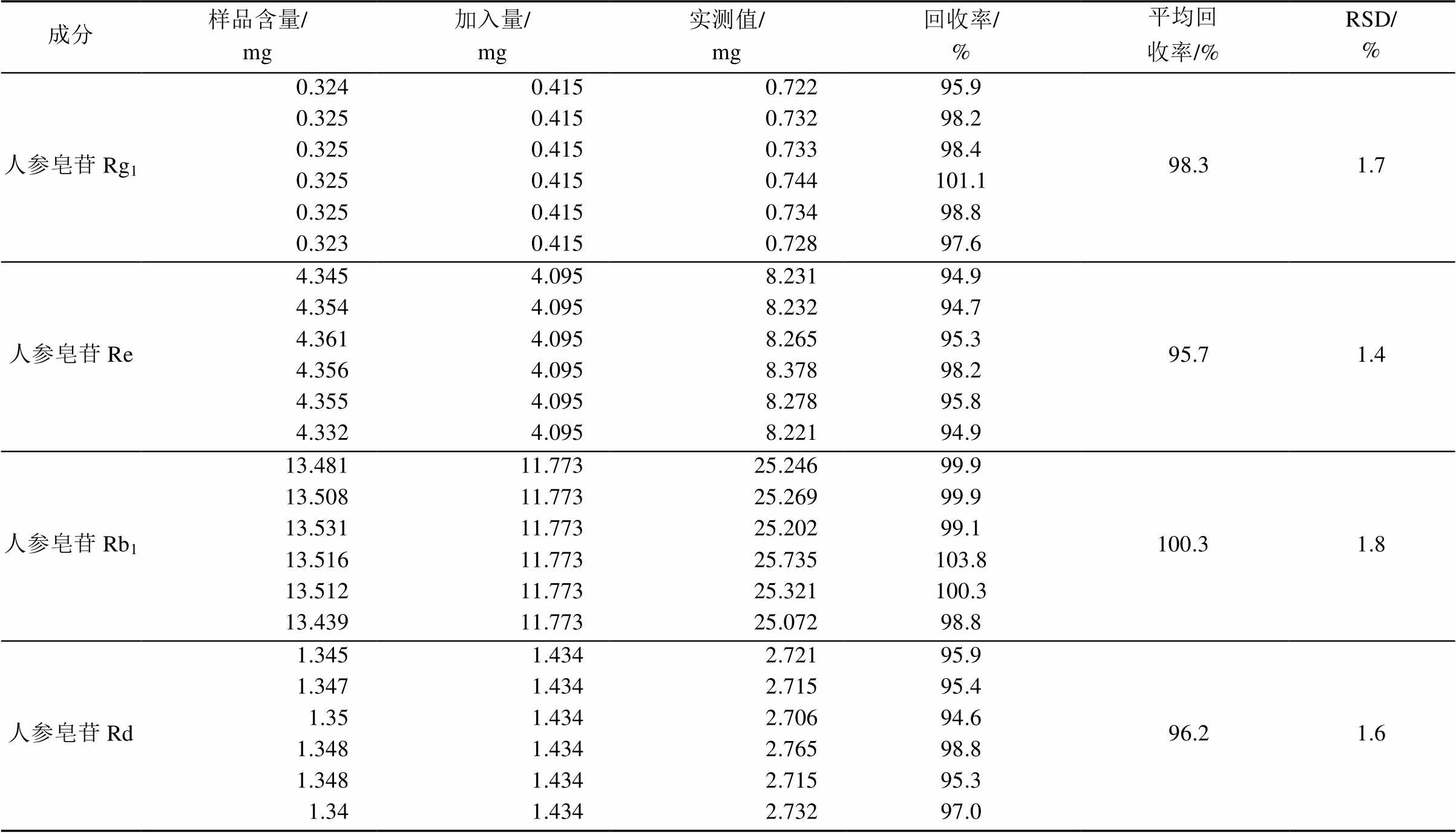
2.3.5 回收率试验 采用加样回收法,取已知含量的样品(批号:XYS-ZJS-6),按中间浓度,精密加入对照品溶液适量,按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件测定供试品中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd的含量,计算回收率,结果见表3。结果平均回收率分别为98.3%(RSD 1.7%),95.7%(RSD 1.4%),100.3%(RSD 1.8%),96.2%(RSD 1.6%)。
2.4 耐用性试验
2.4.1 不同色谱柱比较 对不同的色谱柱进行比较:Agilent Eclipse Plus C18色谱柱(100 mm× 2.1 mm,1.8 μm)、Kromasil KR100-5 C18色谱柱(100 mm×2.1 mm,1.8 μm)和Agilent Zorbax SB C18色谱柱(2.1 mm×100 mm,1.8 μm),结果3种色谱柱均能得到很好的分离,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd含量的RSD分别为2.6%,4.0%,1.4%和2.3%。
表3 进口西洋参中4个成分加样回收率测定(n=6)
Tab. 3 Results of recovery test of 4 components in improtedPanax quinquefoliumL.(n=6)
成分样品含量/mg加入量/mg实测值/mg回收率/%平均回收率/%RSD/% 人参皂苷Rg10.3240.4150.72295.9 98.31.7 0.3250.4150.73298.2 0.3250.4150.73398.4 0.3250.4150.744101.1 0.3250.4150.73498.8 0.3230.4150.72897.6 人参皂苷Re4.3454.0958.23194.9 95.71.4 4.3544.0958.23294.7 4.3614.0958.26595.3 4.3564.0958.37898.2 4.3554.0958.27895.8 4.3324.0958.22194.9 人参皂苷Rb113.48111.77325.24699.9100.31.8 13.50811.77325.26999.9 13.53111.77325.20299.1 13.51611.77325.735103.8 13.51211.77325.321100.3 13.43911.77325.07298.8 人参皂苷Rd1.3451.4342.72195.9 96.21.6 1.3471.4342.71595.4 1.351.4342.70694.6 1.3481.4342.76598.8 1.3481.4342.71595.3 1.341.4342.73297.0
2.4.2 不同柱温比较 采用Agilent Zorbax SB C18色谱柱,柱温分别为20,25,30,35 ℃进行试验,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd含量的RSD分别为2.8%,0.4%,0.3%和0.4%。但随着柱温升高,人参皂苷Rg1和人参皂苷Re之间的分离度变差,而柱温降低会导致柱压升高。综合考虑后确定柱温为30 ℃。
2.4.3 不同流速比较 采用Agilent Zorbax SB C18色谱柱,流速分别为0.4,0.5,0.6 mL·min-1进行试验,结果在不同流速下4个成分均得到较好的分离。人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd含量的RSD分别为1.6%,0.2%,0.2%和0.5%。
2.4.4 不同仪器比较 试验中比较了不同生产厂家(Agilent公司和戴安公司)的仪器,结果2个公司的仪器均能得到很好的分离。人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd含量的RSD分别为1.4%,2.9%,1.6%和2.2%。
2.5 样品测定
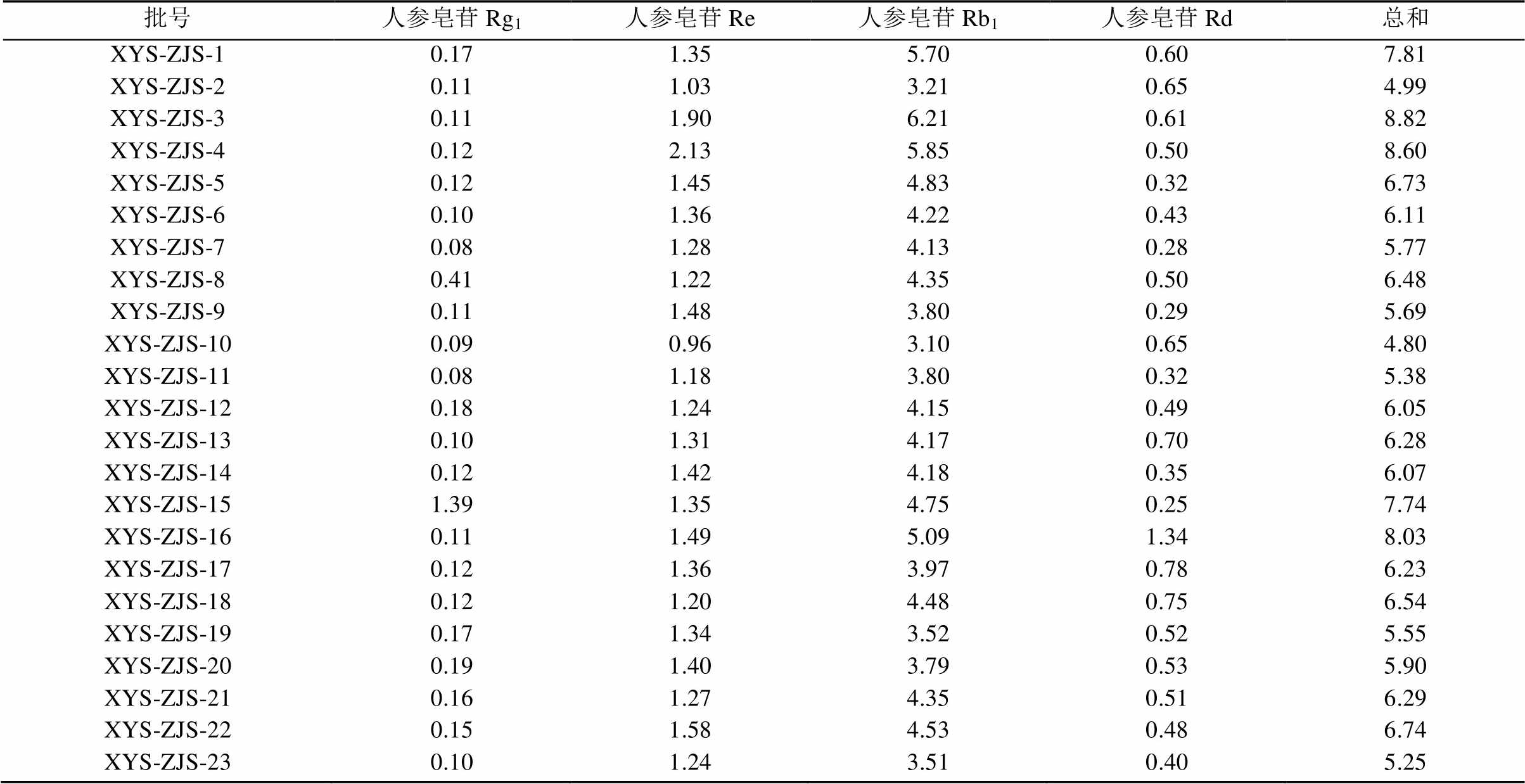
取进口西洋参样品,按“2.1.2”项下方法制备供试品溶液,每个样品平行2份,并按照“2.2”项下色谱条件进行测定,计算各进口西洋参样品中4个成分的含量,结果见表4。
表4 进口西洋参含量测定结果
Tab. 4 Contents of 4 constituents in importedPanax quinquefoliumL. %
批号人参皂苷Rg1人参皂苷Re人参皂苷Rb1人参皂苷Rd总和 XYS-ZJS-10.171.355.700.607.81 XYS-ZJS-20.111.033.210.654.99 XYS-ZJS-30.111.906.210.618.82 XYS-ZJS-40.122.135.850.508.60 XYS-ZJS-50.121.454.830.326.73 XYS-ZJS-60.101.364.220.436.11 XYS-ZJS-70.081.284.130.285.77 XYS-ZJS-80.411.224.350.506.48 XYS-ZJS-90.111.483.800.295.69 XYS-ZJS-100.090.963.100.654.80 XYS-ZJS-110.081.183.800.325.38 XYS-ZJS-120.181.244.150.496.05 XYS-ZJS-130.101.314.170.706.28 XYS-ZJS-140.121.424.180.356.07 XYS-ZJS-151.391.354.750.257.74 XYS-ZJS-160.111.495.091.348.03 XYS-ZJS-170.121.363.970.786.23 XYS-ZJS-180.121.204.480.756.54 XYS-ZJS-190.171.343.520.525.55 XYS-ZJS-200.191.403.790.535.90 XYS-ZJS-210.161.274.350.516.29 XYS-ZJS-220.151.584.530.486.74 XYS-ZJS-230.101.243.510.405.25
3 讨论
本实验建立的UHPLC同时测定进口西洋参中人参皂苷Rg1、Re、Rb1和Rd 4种成分,与原标准中HPLC相比,显著缩短分析时间,节约大量溶剂,同时含量测定结果接近,RSD均<4.5%。
3.1 供试品溶液制备方法的考察
考察了甲醇、50%甲醇和水饱和正丁醇50 mL 3种溶剂的提取效率,结果水饱和正丁醇作为溶剂提取效率较高,杂质较少;考察回流2 h和超声30 min 2种提取方式对试验的影响,结果回流提取方式提取效果较好。分别称取样品粉末0.5,0.75,1.0 g进行试验,结果显示不同取样量对含量测定结果影响不大,以0.75 g时峰响应值较为理想,因此选择取样量为0.75 g。对提取时间进行考察,分别回流1,2,3 h,结果显示,2 h即可提取完全。
3.2 测定结果分析
《儿茶等43种进口药材质量标准》中对西洋参中皂苷含量限度规定为:含人参皂苷Rb1不得<1.2%,含人参皂苷Rg1和人参皂苷Re不得<0.8%;中国药典2015年版一部对西洋参中皂苷含量限度规定为:含人参皂苷Rg1、人参皂苷Re和人参皂苷Rb1的总量不得<2.0%。同时上述标准中对西洋参水分的要求均为不得>13.0%。本次23批样品以干燥品计,故含量限度有所提高。测得人参皂苷Rd的含量平均为0.5%,人参皂苷Rg1、人参皂苷Re和人参皂苷Rb1的总量平均为5.9%。综合已有标准中皂苷含量限度及样品测定结果,暂定西洋参中皂苷类成分含量限度为:本品按干燥品计算,含人参皂苷Rg1(C42H72O14)、人参皂苷Re (C48H82O18)、人参皂苷Rb1(C54H92O23)和人参皂苷Rd(C48H82O18)的总量不得<3.0%。
REFERENCES
[1] 王旭,周富荣. HPLC法测定西洋参中人参皂苷Rb1的含量[J]. 中国中药杂志, 1999, 24(4): 227.
[2] NG T B, LIU F, WANG H X. The antioxidant effects of aqueous and organic extracts ofPanax quinquefolium,Panax notoginseng,Codonopsis pilosula,Pseudostellaria heterophyllaandGlehnia littoralis[J]. J Ethnopharmacol, 2004, 93(2/3): 285-288.
[3] LIU F, NG T B. Antioxidative and free radical scavenging activities of selected medicinal herbs [J]. Life Sci, 2000, 66(8): 725-735.
[4] KITTS D D, WIJEWICKREME A N, HU C. Antioxidant properties of a North American ginseng extract [J]. Mol Cell Biochem, 2000, 203(1/2): 1-10.
[5] MEN-OLIVIER L L, RENAULT J H, THEPENIER P, et al. Purification of the main ginsenosides from a French crop ofPanax quinquefoliusL. [J]. J Liq Chromatogr Relat Technol, 1995, 18(8): 1655-1662.
[6] ZHANG C X, BAO J C, LI X G, et al. HPLC determination of the amount of ginsenosides in different part ofPanax ginsengC. A. Mey. andP. quinquefolius L. andP. notoginseng(Burk) F. H. Chen [J]. Chin J Pharm Anal(药物分析杂志), 2005, 25(10): 1190-1194.
[7] ZHANG H K, GUO C D, GAO G B, et al. Processing technology study of Crataegi Fructus charcoal based on pilot-scale level and multi-component quantification by UPLC [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2017, 34(10): 1413-1417.
[8] LIU L, CHENG L Q, ZHOU S Y, et al. Content determination of ginsenoside Rg1,ginsenoside Re and ginsenoside Rb1in RadixPanax Quinque FoliumL. [J]. Her Med(医药导报), 2011, 30(9): 1208-1209.
[9] BI F J, ZHONG S H, GU L H. Comparison between RRLC and HPLC for determination of ginsenoside Rg1, Re and Rb1in Radix et Rhizoma Ginseng Rubra and Radix Panacis Quinuefolii [J]. Chin J Pharm Anal(药物分析杂志), 2010, 30(9): 1720-1724.
[10] 杨立伟, 郑传奇, 蒋忠军, 等. 超高效液相色谱法测定西洋参中人参皂苷Rg1、Re、Rb1的含量[J]. 中药材, 2008, 31(1): 55-57.
[11] YOKOZAWA T, LIU Z W, DONG E. A study of ginsenoside-Rd in a renal ischemia-reperfusion model[J]. Nephron, 1998, 78(2): 201-206.
[12] ZHAO Y, HU D J, ZHANG X, et al.In vitroeffects of ginsenoside Rd on proliferation and expression of TGF-β1 in human mesangial cells induced by high glucose [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2014, 31(7): 786-789.
Simultaneous Determination of Four Constituents in ImportedPanax QuinquefoliumL. by UHPLC
LU Jingxian, SHI Bei, DONG Ting, CHEN Bilian, MA Linke, ZHU Ming*
(Zhejiang Institute for Food and Drug Control, Hangzhou 310000, China)
ABSTRACT:OBJECTIVETo establish a UHPLC method for simultaneous determination of four active components (ginsenoside Rg1, ginsenoside Re, ginsenoside Rb1and ginsenoside Rd) in importedPanax quinquefoliumL..METHODSAn Agilent Zorbax SB C18column(2.1 mm×100 mm, 1.8 μm) was used, with mobile phase of acetonitrile as mobile phase A and water as mobile phase B(gradient elution) at a flow rate of 0.5 mL·min-1, column temperature was 30 ℃ and detector wavelength was 203 nm.RESULTSThe four components showed good separation and linearity within the tested range. The mean recoveries were in the range of 95.7%-100.3% (RSD 1.4%-1.8%).CONCLUSIONIt provides a rapid and reliable UHPLC method which is suitable for the quality control ofPanax quinquefoliumL..
KEY WORDS:Panax quinquefoliumL.; UHPLC; ginsenoside Rg1; ginsenoside Re; ginsenoside Rb1; ginsenoside Rd
中图分类号:R917
文献标志码:B
文章编号:1007-7693(2018)10-1443-04
DOI:10.13748/j.cnki.issn1007-7693.2018.10.002
引用本文:陆静娴,施贝,董婷, 等. UHPLC同时测定进口西洋参4个化学成分的含量[J]. 中国现代应用药学, 2018, 35(10): 1443-1446.
收稿日期:2017-10-17
基金项目:浙江省中医药科技计划项目(2016ZB081)
作者简介:陆静娴,女,硕士,主管中药师 Tel: (0571)86459414 E-mail: lujingxian1984@126.com
*通信作者:祝明,女,主任中药师 Tel: (0571)86454617 E-mail: zhumingd@hotmail.com
(本文责编:李艳芳)




