
图1 对照品、复方鱼腥草片和阴性样品的HPLC色谱图
关潇滢1,2,陈雪莲3,王淑红1,2,肖丽和1,2,王铁杰1,2*
(1.深圳市药品检验研究院,广东深圳518057;2.深圳药品质量标准研究重点实验室,广东深圳518057;3.暨南大学,广州510632)
摘要:目的 建立HPLC同时测定复方鱼腥草片中绿原酸、连翘酯苷A、槲皮苷和黄芩苷含量的方法。方法 采用CAPCELL PAK MG(4.6 mm×250 mm,5μm)色谱柱,流动相为乙腈(A)-0.1%磷酸溶液(B),梯度洗脱(0~12 min,9%A;12~15 min,9%→15%A;15~32 min,15%A;32~48 min,15%→29%A;48~60 min,29%A),流速1.0 mL·min-1,柱温35 ℃,检测波长:330 nm。结果 绿原酸、槲皮苷浓度在2~100 μg·mL-1内,连翘酯苷A浓度在4~200 μg·mL-1内,黄芩苷浓度在12~600 μg·mL-1内,与峰面积均呈良好的线性关系(r=0.999 9);平均回收率(n=6)分别为98.0%,99.8%,99.1%和98.3%,RSD均<2.0%。结论 建立的HPLC可实现同时测定绿原酸、连翘酯苷A、槲皮苷和黄芩苷4种有效成分,方法快速、简便、结果准确,可为复方鱼腥草片提供更全面、可靠的质量控制方法。
关键词:复方鱼腥草片;绿原酸;连翘酯苷A;槲皮苷;黄芩苷;质量控制;高效液相色谱法
复方鱼腥草片收载于中国药典2015年版一部[1],由鱼腥草、黄芩、板蓝根、连翘、金银花5味药组成,现行质量标准规定了性状、鉴别、检查和黄芩苷的含量测定项目。目前,该制剂的质量控制方法已有一些报道,李长新等[2]采用HPLC测定复方鱼腥草片中黄芩苷的含量;黎小伟等[3]采用HPLC测定复方鱼腥草片中绿原酸的含量;金永新等[4]采用HPLC同时测定复方鱼腥草片中绿原酸、连翘苷、黄芩苷的含量。本实验以方中金银花有效成分绿原酸、连翘有效成分连翘酯苷A、鱼腥草有效成分槲皮苷和黄芩有效成分黄芩苷为指标,采用HPLC同时检测这4个有效成分,与文献报道的复方鱼腥草片含量测定方法相比,具有操作简便、可同时检测多个有效成分以及专属性强的优势。
1.1 仪器
SHIMADZU LC-20AD高效液相色谱仪,DAD检测器(日本岛津公司);XS205电子天平(瑞士梅特勒-托利多公司);SCIENTZ SB-25-12DT超声波清洗仪(宁波新芝生物);纯水器(美国Millipore公司)。
1.2 试药
乙腈(色谱纯,德国MERCK公司);甲醇、磷酸 (分析纯,广州化学试剂厂);水为超纯水;对照品:绿原酸(批号:110753-201314,纯度:96.6%)、连翘酯苷A(批号:111810-201405,纯度:94.1%)、槲皮苷(批号:111538- 200403,纯度:100%)、黄芩苷(批号110715-201318,纯度:93.3%),均购于中国食品药品检定研究院;20批不同生产企业复方鱼腥草片样品为全国范围抽样得到。
2.1 色谱条件
采用CAPCELL PAK MG(4.6 mm×250 mm,5 μm)色谱柱,以乙腈(A)-0.1%磷酸溶液(B)为流动相,梯度洗脱(0~12 min,9%A;12~15 min,9%→15%A;15~32 min,15%A;32~48 min,15%→29%A;48~60 min,29%A),流速1.0 mL·min-1,柱温35 ℃,检测波长为330 nm,进样量10 μL。
2.2 溶液的制备
2.2.1 对照品储备液的制备 取绿原酸和槲皮苷对照品各约10 mg,精密称定,分别置50 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得;取连翘酯苷A和黄芩苷对照品各约10 mg,精密称定,分别置25 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得。
2.2.2 混合对照品溶液的制备 精密吸取绿原酸、槲皮苷的对照品储备液各2 mL,连翘酯苷A的对照品储备溶液3 mL,黄芩苷的对照品储备液10 mL,置同一20 mL量瓶中,加甲醇稀释至刻度,摇匀,即得。
2.2.3 供试品溶液的制备 取本品20片,除去包衣(糖衣/薄膜衣片),精密称定,研细,取约1.0 g,精密称定,精密加入70%甲醇50 ml,称定质量,超声处理(功率500 W,频率40 kHz)1 h,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.2.4 阴性供试品溶液的制备 按复方鱼腥草片的处方及制法,分别制成不含鱼腥草、黄芩、连翘和金银花的阴性样品,按“2.2.3”项下方法操作,分别制得阴性样品溶液。
2.3 系统适用性试验
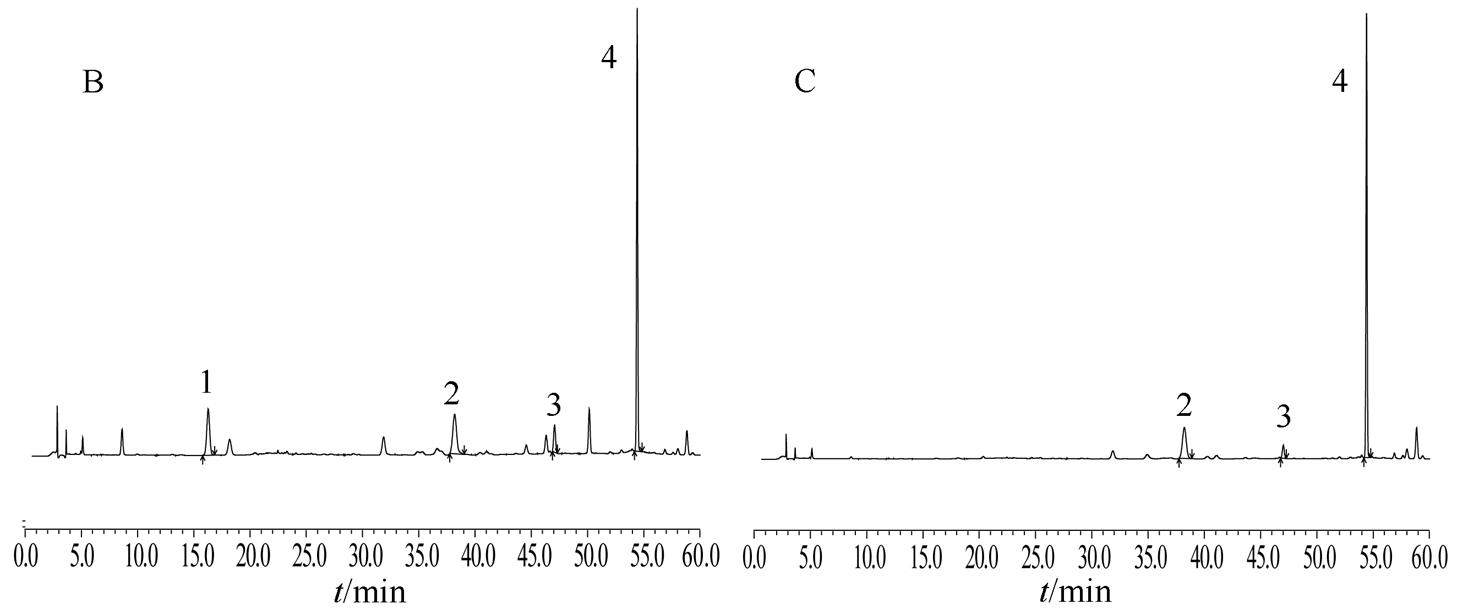
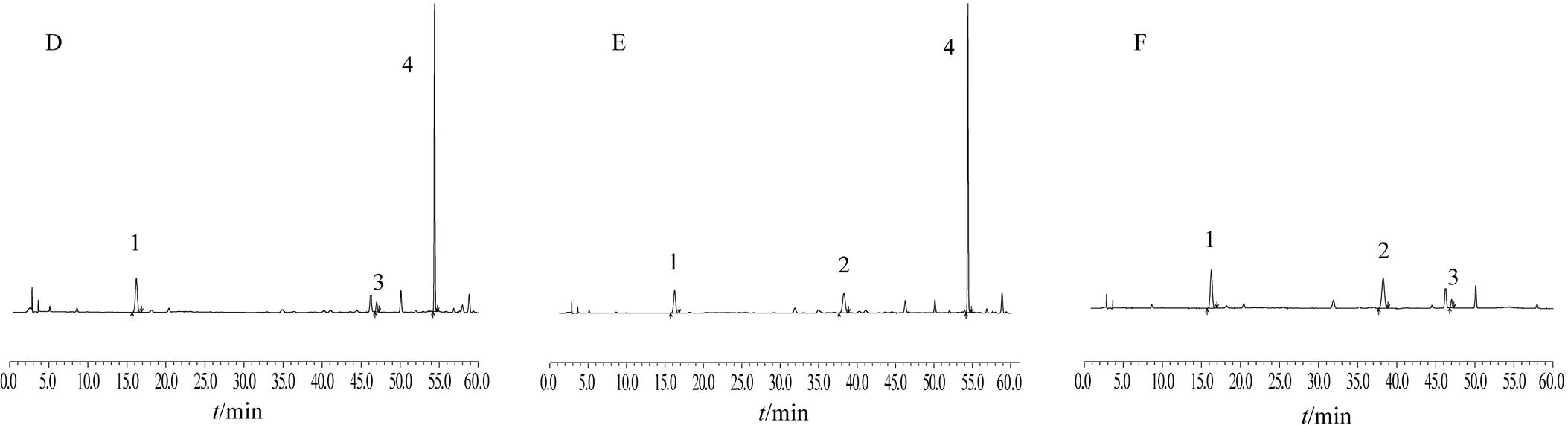
取混合对照品溶液、供试品溶液及阴性样品溶液各10 μL,按“2.1”项下色谱条件进行测定,记录色谱图,见图1。结果阴性样品的色谱图中,在与对照品色谱图相同的保留时间位置上未见色谱峰,说明阴性无干扰。理论板数按绿原酸、连翘酯苷A、槲皮苷、黄芩苷峰计算,均≥8 000;各色谱峰峰形对称,分离度良好;阴性样品无干扰。



图1 对照品、复方鱼腥草片和阴性样品的HPLC色谱图
A-对照品;B-样品;C-缺金银花阴性样品;D-缺连翘阴性样品;E-缺鱼腥草阴性样品;F-缺黄芩阴性样品;1-绿原酸;2-连翘酯苷A;3-槲皮苷;4-黄芩苷。
Fig. 1 HPLC chromatograms of reference substances, Fufang Yuxingcao tablets and negative samples
A-reference substances; B-sample; C-negative sample without Lonicerae Japonicae Flos; D-negative sample without Forsythiae Fructus; E-negative sample without Houttuyniae Herba; F-negative sample without Scutellariae Radix; 1-chlorogenic acid; 2-forsythoside A; 3-quercitroside; 4-baicalin.
2.4 线性关系考察
取绿原酸、槲皮苷对照品各约10 mg,精密称定,置同一50 ml量瓶中,加甲醇溶解并稀释至刻度,摇匀,作为绿原酸、槲皮苷混合对照品溶液;取连翘酯苷A对照品约10 mg、黄芩苷对照品约30 mg,精密称定,置同一50 mL量瓶中,精密加入上述绿原酸、槲皮苷混合对照品溶液25 mL,加甲醇溶解并稀释至刻度,摇匀,精密量取1,2,5,10,25 ml分别置50 mL量瓶中,加甲醇稀释至刻度,摇匀,按“2.1”项下色谱条件进行测定,以对照品的浓度X(μg·mL-1)为横坐标,测得的峰面积Y为纵坐标,绘制标准曲线,得绿原酸、连翘酯苷A、槲皮苷、黄芩苷的回归方程分别为:Y=3.10×104X+3.54×102,r=0.999 9;Y=3.39×104X+2.63×102,r=0.999 9;Y=1.70×104X+ 8.66×102,r=0.999 9;Y=9.55×104X+1.99×103,r=0.999 9。结果表明,绿原酸、槲皮苷浓度在2~ 100 μg·mL-1内,连翘酯苷A浓度在4~200 μg·mL-1内,黄芩苷浓度在12~600 μg·mL-1内均与其峰面积呈良好的线性关系。
2.5 仪器精密度试验
取混合对照品溶液,按“2.1”项下色谱条件连续进样6次,测定峰面积,计算绿原酸、连翘酯苷A、槲皮苷、黄芩苷峰面积的RSD分别为0.5%,0.2%,0.3%,0.3%,结果表明该方法仪器精密度良好。
2.6 稳定性试验
取同一份复方鱼腥草片供试品溶液,分别于0,1,2,4,8,12 h进样测定,测得的绿原酸、连翘酯苷A、槲皮苷、黄芩苷峰面积的RSD分别为0.6%,0.5%,0.4%,0.3%。结果表明溶液自制备后12 h内基本稳定。
2.7 重复性试验
取同一批复方鱼腥草片(序号01,平均片重0.295 6 g)6份,按“2.2.3”项下方法制备供试品溶液,进样测定,测得绿原酸、连翘酯苷A、槲皮苷、黄芩苷含量平均值及其RSD分别为1.22 mg·g-1(0.3%),3.54 mg·g-1(0.7%),1.11 mg·g-1(0.5%),21.39 mg·g-1(0.4% ),结果表明该方法的重复性良好。
2.8 加样回收率试验
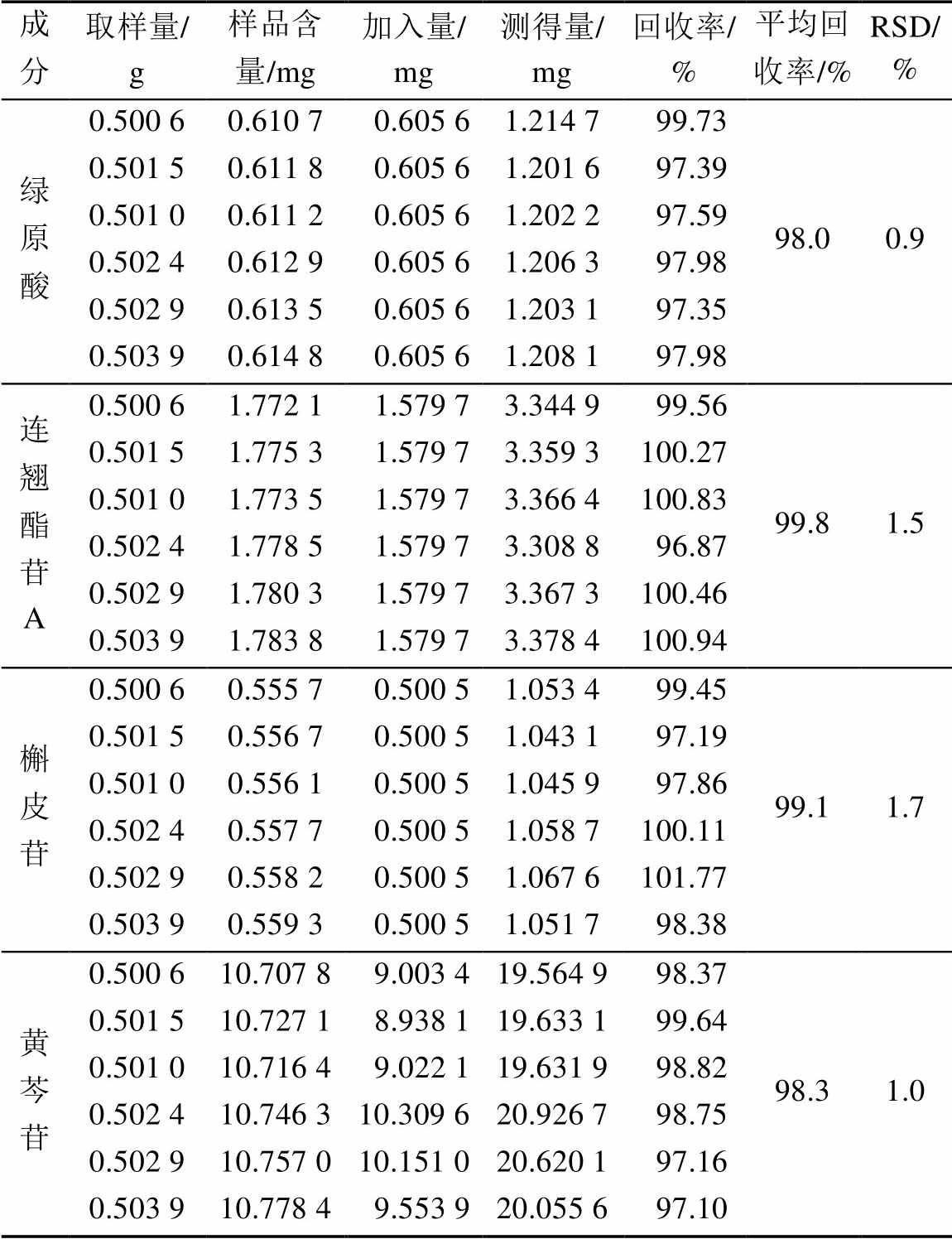
精密称取同一批已知含量(序号01)的复方鱼腥草片粉末约0.5 g,共6份,根据复方鱼腥草片中绿原酸、连翘酯苷A、槲皮苷、黄芩苷的含量,按表1分别精密加入绿原酸、连翘酯苷A、槲皮苷和黄芩苷对照品,按“2.2.3”项下方法制备供试品溶液,进样测定,计算绿原酸、连翘酯苷A、槲皮苷、黄芩苷的平均回收率(n=6)分别为98.0%(RSD=0.9%),99.8%(RSD=1.5%),99.1% (RSD=1.7%),98.3%(RSD=1.0%)。
表1 加样回收率测定结果(n=6)
Tab. 1 Recoveries of 4 effective components in samples (n=6)
2.9 样品的测定
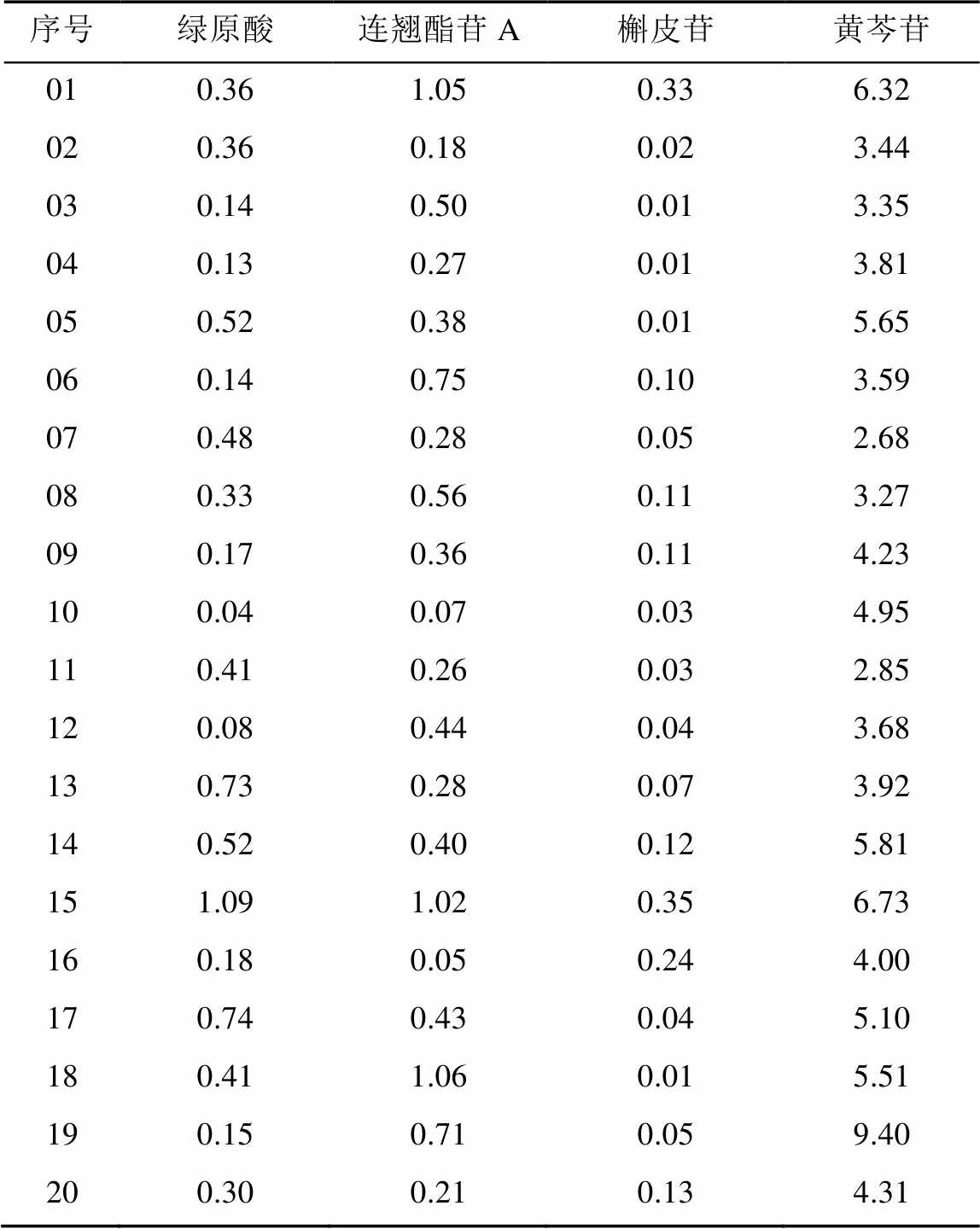
取不同生产企业复方鱼腥草片20批,分别按“2.2.3”项下方法制备供试品溶液,进样测定,以外标法计算绿原酸、连翘酯苷A、槲皮苷、黄芩苷的含量,结果见表2。
3.1 测定成分的选择
复方鱼腥草片的功能主治为清热解毒,而此次测定的金银花中的绿原酸、连翘中的连翘酯苷A、鱼腥草中的槲皮苷和黄芩中的黄芩苷,4个成分均具有抗炎、抗病毒[5-9]的药理作用,与复方鱼腥草片的功能主治相符合,故同时测定此4个成分的含量进而控制中成药的质量优劣是具有重要意义的。
表2 样品含量测定结果(n=2)
Tab. 2 Results of content tests(n=2) mg
3.2 提取溶剂及提取方式的选择
为保证绿原酸、连翘酯苷A、槲皮苷、黄芩苷4种成分都可提取完全,作者考察了甲醇、70%甲醇、乙醇、70%乙醇4种提取溶剂,0.5,1,1.5 h 3个提取时间,超声、回流2种提取方式,最终确定提取方式为70%甲醇超声提取1 h,4个成分的提取效率最高。
3.3 检测波长的选择
分别取绿原酸、连翘酯苷A、槲皮苷、黄芩苷对照品储备溶液,在200~400 nm内进行扫描,绿原酸、连翘酯苷A均在330 nm有最大吸收、槲皮苷和黄芩苷在此波长也有较大吸收,故最终确定以330 nm作为检测波长。
3.4 流动相的选择
比较了乙腈-0.1%磷酸溶液和乙腈-6 mmol·L-1磷酸二氢钾溶液2个系统,结果乙腈-0.1%磷酸溶液梯度洗脱条件下4个成分的分离效果更好,出峰时间更适宜。
3.5 阴性溶液的制备
绿原酸为金银花的指标成分之一,但有文献[10]报道鱼腥草中也含有绿原酸,故同时制备了金银花阴性和金银花、鱼腥草双阴性溶液,分析显示金银花阴性样品色谱图中仅有一峰面积极小的绿原酸峰,含量极微,表明复方鱼腥草片中的绿原酸主要来源于金银花药材。
3.6 含量测定结果
实验从全国范围抽取的样品中,随机选取了不同厂家的20批复方鱼腥草片进行含量测定,结果可见,除现行质量标准中已控制的黄芩苷的测定结果较稳定外,其余3个指标成分含量差异较大,故增加此3个指标成分的含量测定方法,以更全面地监控复方鱼腥草片的质量。
本实验建立了HPLC同时测定复方鱼腥草片中绿原酸、连翘酯苷A、槲皮苷和黄芩苷的含量,经方法学验证,所建立的测定方法符合定量分析要求,且实现同时对方中金银花、连翘、鱼腥草和黄芩的质量控制,为更全面提升该品种质量标准、保障产品质量,提供了一种可靠的检测方法。
[1] 中国药典. 一部[S]. 2015: 1234-1235
[2] LI C X, QI X P. Determination of baicalia content in Compound Houttuynia Herb tablets HPLC [J]. Heilongjiang Med J(黑龙江医药), 2005, 18(5): 320-321.
[3] LI X W, YE X Q. Determination of chlorogenic acid content in Compound Houttuynia Herb tablets by HPLC [J]. Chin Tradit Pat Med(中成药), 2003, 25(1): 66-67.
[4] JIN Y X, YAO L Q. Determination of chlorogenic acid, phillyrin and baicalin in Compound Houttuynia Herb tablets by RP-HPLC [J]. China Pharm(中国药师), 2004, 7(7): 524-526.
[5] LIUY, GUO M Y, BAI G B. Research progress of chlorogenic acid [J]. J Chin Med Mater(中成药), 2012, 35(7): 1180-1185.
[6] XING L N, ZHOU M M, LI Y, et al. Recent progress of potential effects and mechanisms of chlorogenic acid and its intestinal metabolites on central nervous system diseases [J]. China J Chin Mater Med(中国中药杂志), 2015, 40(6): 1044-1047.
[7] FU P L, WANG D Q, LI Z J. Research progress of forsythoside [J]. J Changchun Univ Tradit Chin Med(长春中医药大学学报), 2011, 27(12): 1062-1063.
[8] YANG L. Research development of pharmacology activities of quercitroside [J]. Asia-Pacific Tradit Med(亚太传统医药), 2016, 11(6): 61-63.
[9] WEN M, LI X, FU S T. New Research progress in pharmacological activities of baicalin [J]. J Shenyang Pharm Univ(沈阳药科大学学报), 2008, 25(2): 158-162.
[10] HE B, LIU Y, et al. Simultaneous determination of six active constituent in different parts of Houttuyniae Herba by quantitative analysis of multi-components by single marker [J]. Chin Tradit Herb Drags(中草药), 2013, 43(15): 2160-2164.
(本文责编:曹粤锋)
GUAN Xiaoying1,2, CHEN Xuelian3, WANG Shuhong1,2, XIAO Lihe1,2, WANG Tiejie1,2*
(1.Shenzhen Institute for Drug Control, Shenzhen 518057, China; 2.Shenzhen Key Laboratory of Drug Quality Standard Research, Shenzhen 518057, China; 3.Jinan University, Guangzhou 510632, China)
ABSTRACT:OBJECTIVE To establish an HPLC method for simultaneous determination of chlorogenic acid, forsythoside A, quercitroside and baicalin in Fufang Yuxingcao tablets. METHODS The samples were separated on a CAPCELL PAK MG (4.6 mm×250 mm, 5 μm) column, by a gradient elution using acetonitrile(A) and 0.1% phosphoric acid(B) (0-12 min, 9%A; 12-15 min, 9%→15%A; 15-32 min, 15%A; 32-48 min, 15%→29%A; 48-60 min, 29%A) as mobile phase at a flow rate of 1.0 mL·min-1. The column temperature was set at 35 ℃. The wavelength was set on 330 nm. RESULTS The linear ranges of chlorogenic acid, quercitroside, forsythoside A and baicalin were 2-100 μg·mL-1, 2-100 μg·mL-1, 4-200 μg·mL-1and 12-600 μg·mL-1(r=0.999 9), the average recoveries(n=6) were 98.0%, 99.8%, 99.1% and 98.3%, respectively, and RSDs were < 2.0%. CONCLUSION A rapid, simple, accurate HPLC method is successfully established for simultaneous determine 4 effective components in Fufang Yuxingcao tablets. The method herein described is helpful for the quality control of Fufang Yuxingcao tablets.
KEY WORDS:Fufang Yuxingcao tablets; chlorogenic acid; forsythoside A; quercitroside; baicalin; quality control; HPLC
中图分类号:R917.101
文献标志码:B
文章编号:1007-7693(2017)09-1300-04
DOI:10.13748/j.cnki.issn1007-7693.2017.09.018
引用本文:关潇滢, 陈雪莲, 王淑红, 等. HPLC同时测定复方鱼腥草片中4个有效成分的含量[J]. 中国现代应用药学, 2017, 34(9): 1300-1303.
作者简介:关潇滢,女,硕士,主管中药师 Tel: (0755)26031745 E-mail:guanxy1213@163.com
*通信作者:王铁杰,女,博士,主任药师 Tel: (0755)26031728 E-mail: wangtj88@163.com
收稿日期:2017-01-11