表1 流动相比例变化
Tab. 1 The proportion of mobile phase changes

李好
(温州市人民医院,浙江温州 325000)
摘要:目的 建立超高效液相色谱-串联质谱(UPLC-MS/MS)测定大鼠血浆中盐酸美沙酮及其代谢产物乙二胺二甲基次磷酸(2-ethylidene-1,5-dimethyl-3,3-diphenylpyrrolidine,EDDP)的含量。方法 以地西泮为内标,大鼠血浆用乙腈沉淀蛋白,运用UPLC-MS/MS检测大鼠灌胃盐酸美沙酮6 mg·kg-1后血浆中美沙酮和EDDP的血药浓度,并对数据进行分析。结果 大鼠血浆中盐酸美沙酮和EDDP的定量限均为0.5 ng·mL-1;线性相关系数r>0.999;日内精密度和日间精密度的RSD均<15%;绝对回收率均>85%,相对回收率在90%~110%之间;基质效应在92.80%~97.71%之间。主要药动学参数:美沙酮、EDDP在大鼠血浆中的消除半衰期(t1/2)为(1.479±0.839),(2.590±0.760) h;最高血药浓度(Cmax)为(48.562±10.501),(25.542±3.706)mg·L-1;平均滞留时间(MRT0-t)为(3.476±0.310),(3.883±0.514) h;曲线下面积(AUC0-t)为(204.036±61.145),(86.031±15.287)mg·h·L-1;清除率(CL)为(32.338±14.343)、(70.137±10.786) L·h-1·kg-1,各项药动学参数比较差异均有统计学意义。结论 该法专属性强、分离完全、快速灵敏,适用于大鼠血浆中盐酸美沙酮及其代谢产物EDDP的含量测定和药动学研究。
关键词:超高效液相色谱串联质谱法;美沙酮;乙二胺二甲基次磷酸;血药浓度
盐酸美沙酮(以下简称美沙酮)是一类μ阿片受体激动剂,具有镇痛作用,被用于海洛因依赖脱毒和替代维持治疗[1]。因其脂溶性高、半衰期(t1/2)长,且费用低,常被用于慢性疼痛的治疗[2]。作为长效镇痛阿片类药物,美沙酮具有血药浓度较稳定、成瘾性小等优点,其应用也越来越广泛[3]。但是,美沙酮为μ阿片受体激动剂,其药理作用和不良反应与吗啡类似,常见的不良反应有头晕、恶心、出汗、嗜睡、便秘等,也可因组织蓄积而产生药物过量中毒以及药物成瘾。美沙酮亦存在过量可导致致死性药物不良反应——呼吸抑制。美沙酮所致的呼吸抑制和呼吸衰竭在婴儿、儿童等群体中较为常见[4-5],此外还有心脏毒性和5-羟色胺综合征等比较严重的不良反应;且美沙酮个体差异较大、容易与其他药物发生相互作用[6],故监测其浓度在临床治疗、法医鉴定、戒毒等领域都有重要意义[7]。
美沙酮经肝脏代谢,乙二胺二甲基次磷酸(2-ethylidene-1,5-dimethyl-3,3-diphenylpyrrolidine,EDDP)是其主要的代谢产物,检测美沙酮及其代谢产物EDDP的浓度,有助于对其药动学进行研究。本研究采用UPLC-MS/MS联用技术,建立方法专属性强,分离完全,快速灵敏的检测方法,并通过口服灌胃给药测定大鼠血浆中药物浓度,对美沙酮及EDDP进行大鼠体内的药动学研究。其也可用于美沙酮与其他药物相互作用的研究,并为美沙酮在体内吸收和代谢研究提供参考。
1.1 仪器
Waters XEVO TQD超高效液相-质谱联用(美国Waters);AE 200-S电子天平(浙江省科学器材进出口有限责任公司);QL-901涡旋混合器(江苏海门其林贝尔仪器制造有限公司);Milli-Q Reference超纯水仪(美国Millipore)。
1.2 试药
盐酸美沙酮(美国 Mallinckrodt Inc,批号:P05077,纯度>99.5%);EDDP(加拿大Toronto Research Chemicals,批号:FN122109-01,纯度:99.5%);地西泮(南京苏耀建科技有限公司,批号:171225-200903,纯度>99.0%);乙腈(色谱纯,美国Merk&Co Inc);甲醇(色谱纯,美国Fisher Scientific);水为Millipore超纯水;其余常规化学试剂均为分析纯或优级纯(上海化学试剂公司)。
1.3 动物及给药方法
SD大鼠,♂,体质量(257±23)g,由温州医科大学动物实验中心提供,合格证号为SCXK(浙)2014-0001。饲养于清洁级条件下,动物房室温维持在24 ℃左右,湿度约为60%~70%。于实验前一晚8:00开始禁食,不禁水。
2.1 对照品溶液的配制
2.1.1 美沙酮对照品溶液的配制 精密称取美沙酮对照品2.50 mg,用甲醇溶解于10 mL量瓶中,得浓度为250 µg·mL-1美沙酮对照品储备溶液。
2.1.2 EDDP对照品溶液的配制 精密称取EDDP对照品10.00 mg,用甲醇溶解后转移至25 mL量瓶中,甲醇定容,得400 µg·mL-1EDDP对照品储备溶液。
2.1.3 地西泮内标溶液的配制 精确吸取2.5 mg·mL-1地西泮对照品溶液1 mL于25mL量瓶中,甲醇定容,得100 µg·mL-1地西泮对照品溶液;精确吸取1 mL 100 µg·mL-1地西泮甲醇溶液于100 mL量瓶中,甲醇定容,得1 µg·mL-1地西泮内标液。
2.2 色谱条件及系统适应性
2.2.1 色谱条件 色谱柱为Waters Acquity UPLC BEH C18色谱柱(2.1 mm×50 mm,1.7 μm),流动相为乙腈和0.1%甲酸(溶于超纯水中),采用梯度洗脱,流动相比例见表1。流速为0.4 mL·min-1,柱温为40 ℃,自动进样器内温度设置为4 ℃。
表1 流动相比例变化
Tab. 1 The proportion of mobile phase changes

2.2.2 质谱条件 Waters XEVO TQD质谱为电喷雾(ESI)质谱,本研究所用为正离子模式。去溶剂化气体为氮气,流速为1 000 L·h-1,温度为500 ℃。离子源温度为150 ℃。氩气为碰撞气体,流速为0.1 mL·min-1。毛细管电压为1 kV。各药物经调谐后的MRM信息见表2。
表2 美沙酮及其代谢产物和内标地西泮的MRM信息
Tab. 2 MRM information of methadone and its metabolites and diazepam in internal standard

2.3 血浆样品处理方法
将保存于-80 ℃冰箱的血浆取出,置于室温下解冻。涡旋混匀,取100 µL于1.5 mL EP管中,加入内标地西泮甲醇溶液(1 µg·mL-1)40 µL和200 µL乙腈沉淀蛋白,涡旋混匀2 min,13 000 r·min-1离心10 min,取上清液100 µL于0.5 mL EP管中,加入100 µL超纯水稀释,涡旋混匀,2 µL用于进样。
2.4 方法学验证
2.4.1 专属性试验 在“2.2.1”色谱条件下,分别取大鼠空白血浆、空白血浆加美沙酮、EDDP和内标溶液,以及大鼠给药30 min后的血浆样品,按“2.3”项下方法操作分析。空白血浆对美沙酮及其代谢产物的检测无明显干扰,见图1。美沙酮、EDDP和内标地西泮的出峰时间分别为1.67,1.58,1.78 min,且峰型良好。美沙酮及其代谢产物的质谱图见图2。虽然两者出峰时间相近,但是在其相应的离子通道里,各物质无相互干扰。
2.4.2 标准曲线的制备 分别用微量移液枪准确移取美沙酮、EDDP标准储备液200,125 µL于10 mL量瓶中,用甲醇定容,得到美沙酮、EDDP浓度为5 µg·mL-1的混合工作液I。将该混合工作液依次用甲醇稀释,配置成浓度为10,20,100,200,500,1 000,2 000,5 000 ng·mL-1的混合工作液组Ⅱ。准确移取混合工作液Ⅱ各5 µL,依次加入到8份100 µL的大鼠空白血浆中,得到终浓度分别为0.5,1,5,10,25,50,100,250 ng·mL-1。
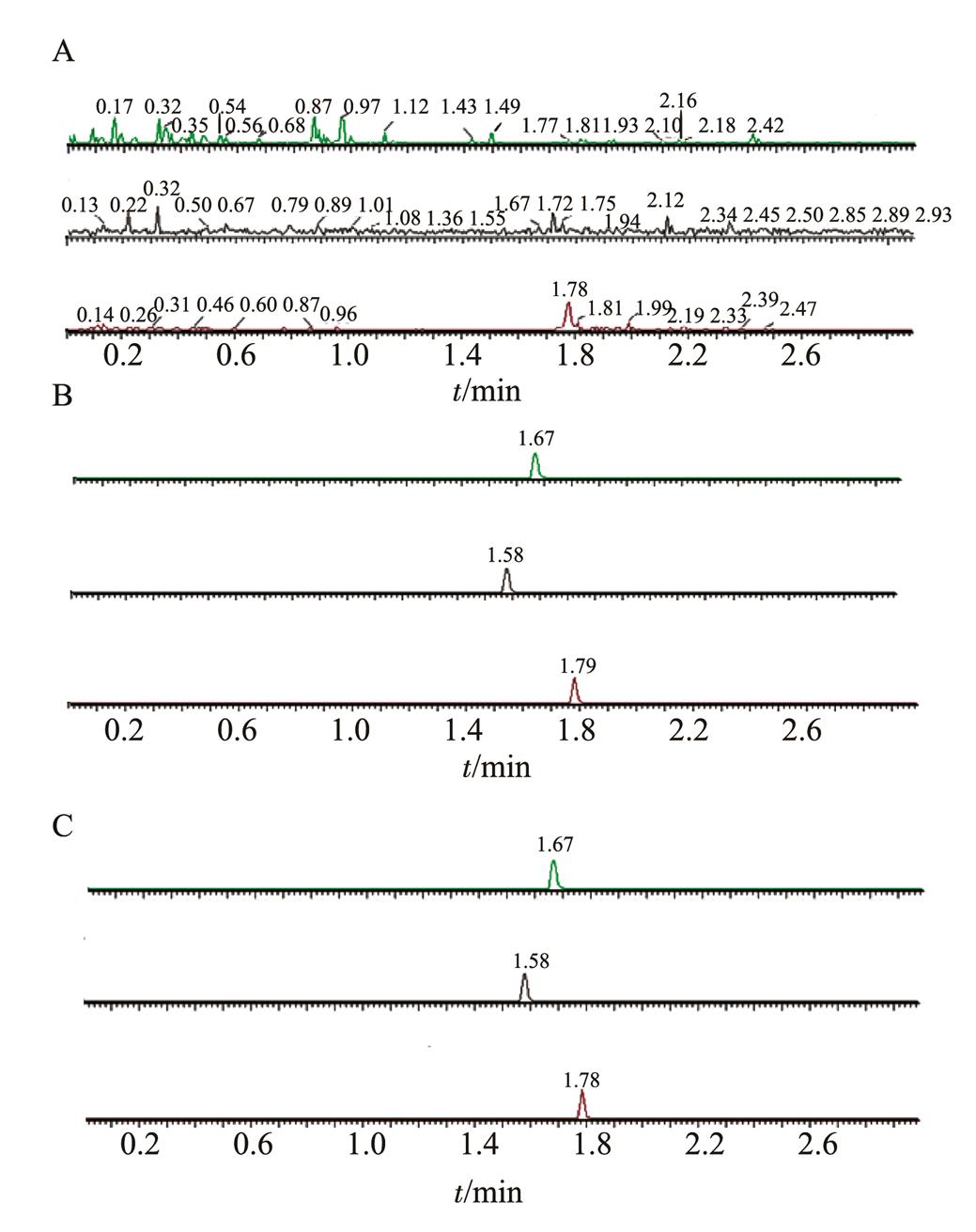
图1 色谱图
A-空白血浆;B-空白血浆加美沙酮、EDDP(0.5 ng·mL-1)和内标;C-血浆样品(灌胃给药后30 min)。
Fig. 1 HPLC chromatogram
A-blank plasma; B-blank plasma with methadone and EDDP (0.5 ng·mL-1) and internal standard; C-a plasma sample collected at 30 min after oral administration.
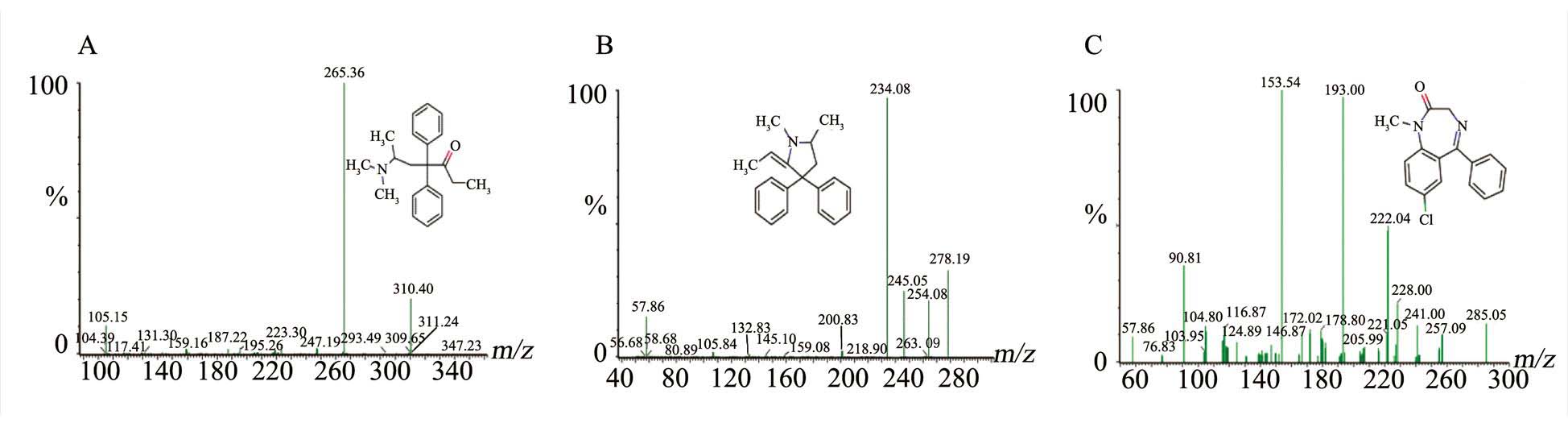
图2 质谱图
A-美沙酮;B-EDDP;C-内标地西泮。
Fig. 2 Mass spectrum
A-methadone; B-EDDP; C-the internal standard diazepam.
按“2.3”项下方法对上述血浆标准品进行处理并检测。以血浆中待测物浓度为横坐标x,待测物与内标的峰面积比值为纵坐标y,用加权(1/C2)最小二乘法进行回归运算,得在0.5~250 ng·mL-1范围的美沙酮、EDDP的标准曲线方程为美沙酮:y=0.006 5x+0.012 3(r=0.999 7);EDDP:y=0.013 8x+ 0.039 9(r=0.999 2)。美沙酮、EDDP在相应的浓度范围内线性关系良好(r>0.999)。美沙酮、EDDP的定量下限均为0.5 ng·mL-1(信噪比S/N>10)。
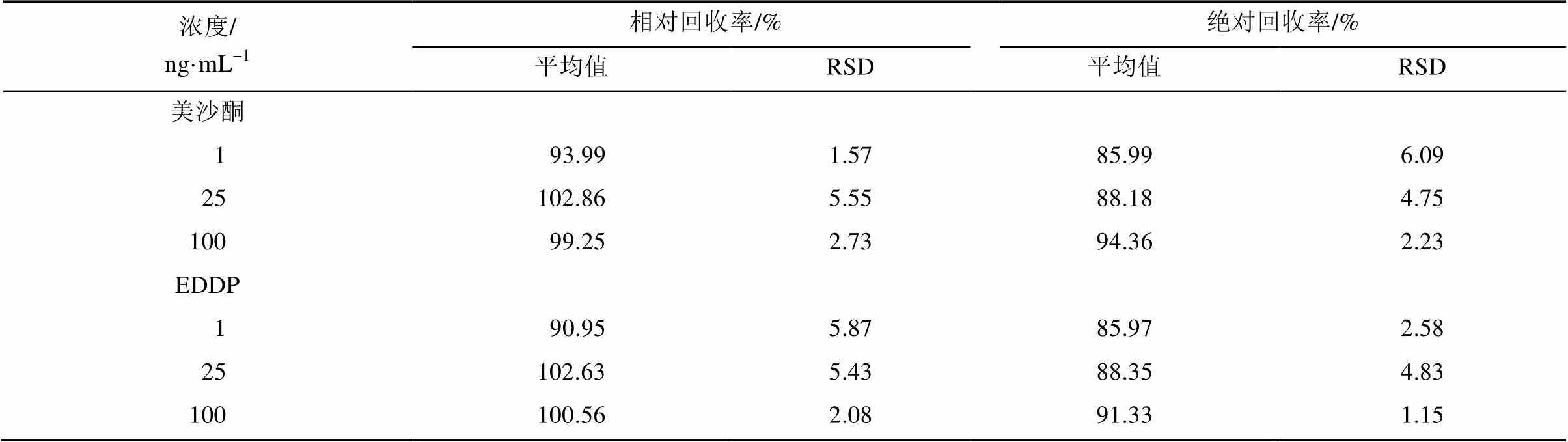
2.4.3 回收率实验 按“2.4.2”项下分别配制美沙酮和EDDP低、中、高浓度均为1,25,100 ng·mL-1的血浆样品溶液,每个浓度取6份,按“2.3”项下所描述的方法处理后检测峰面积,依据标准曲线计算检测浓度,计算相对回收率。同上取美沙酮和EDDP低、中、高浓度均为1,25,100 ng·mL-1的血浆样品溶液各6份,经过血浆样本处理后进样测定,进样分析得峰面积A1与另取大鼠空白血浆样品经处理后,加入对应的低、中、高浓度的系列对照品溶液和内标溶液,进样分析得峰面积A2,计算绝对回收率。
美沙酮、EDDP的相对回收率在90%~110%之间,绝对回收率均>85%,符合方法学要求,结果见表3。
表3 大鼠血浆中美沙酮、EDDP的相对回收率和绝对回收率(n=6)
Tab. 3 The relative recovery and absolute recovery of methadone and EDDP in rat plasma(n=6)
2.4.4 精密度实验 按“2.4.2”项下方法分别配制美沙酮和EDDP低、中、高浓度均为1,25,100 ng·mL-1的血浆样品溶液,每个浓度平行配制6份,按“2.3”项下方法处理,进样测定,并分别在1 d内和连续3 d内进样,依法测定。计算方法的日内精密度和日间精密度。
美沙酮、EDDP的日内、日间精密度的RSD均<15%,符合方法学要求,结果见表4。
表4 大鼠血浆中的美沙酮、EDDP的日内、日间精密度(n=6)
Tab. 4 The intra-day and inter-day precision of methadone and EDDP in rat plasma (n=6)

2.4.5 基质效应 取大鼠空白血浆按照“2.4.2”项下所描述的方法处理后得到上清液,分别加入美沙酮、EDDP和内标溶液,制成含内标溶液的低、中、高浓度均为1,25,100 ng·mL-1的血浆样品溶液,进样分析,得到的色谱峰面积与相应浓度的标准溶液直接进样获得的峰面积进行比较,计算本方法基质效应。
美沙酮、EDDP的基质效应在92.80%~97.71%之间,可见,大鼠血浆基质效应不影响各药物的检测。
2.4.6 稳定性考察 按照“2.4.2”的方法分别配制美沙酮、EDDP大鼠血浆低、中、高浓度均为1,25,100 ng·mL-1的血浆样品各3份,分别于室温(放置0,4,12 h)、自动进样器内(4 ℃放置0,4,12 h)、长期冻存(-80 ℃冰箱中放置1周、2周和4周)和冻融循环3次后处理样品并进行检测,考察样品稳定性。结果表明,血浆样品放置在上述条件下,美沙酮和EDDP的RSD均<10%。采集的样品可保存于-80 ℃冰箱内,样品处理后放置于进样器内并于12 h内检测完所得的数据也是可信的。
2.5 药动学试验
准备SD大鼠8只,♂,体质量(257±23)g,实验采用单次灌胃给药方式,给药剂量为盐酸美沙酮6 mg·kg-1。灌胃前采集空白血0.5 mL,再分别于灌胃后5,10,15,30,45 min和1,1.5,2,3,4,6,8,10,12,24 h经尾部静脉采血0.5 mL于加有肝素的1.5 mL的EP管中。采集的血样于3 000 r·min-1条件下离心10 min,取血浆于1.5 mL EP管中,置于-80 ℃冷冻保存。
实验测得的主要药动学参数经DAS 3.0软件进行处理分析,得到相应药物的药动学参数。美沙酮和EDDP在大鼠血浆中的浓度-时间曲线见图3,测得的主要药动学参数见表5。
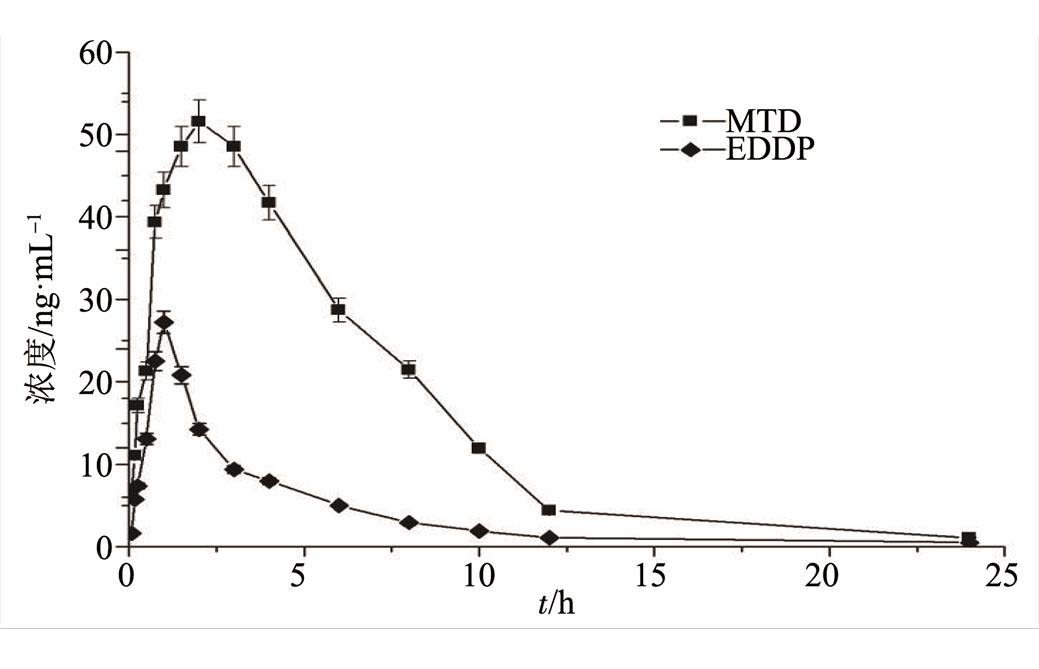
图3 大鼠血浆中美沙酮、EDDP的平均血药浓度-时间曲线
Fig. 3 Mean blood concentration-time curve of methadone and EDDP of rat plasma
表5 大鼠灌胃给予6 mg·kg-1美沙酮后美沙酮和EDDP的药动学参数(n=8,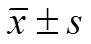 )
)
Tab. 5 Pharmacokinetic parameters of methadone and EDDP after 6 mg·kg-1of methadone to rat(n=8,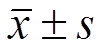 )
)

美沙酮目前主要用于海洛因依赖脱毒和替代维持治疗[8],因其脂溶性高、半衰期长[9],还用于慢性疼痛的治疗[2]。在治疗过程中,使美沙酮血药浓度达到最佳浓度是至关重要的[10]。虽然美沙酮半衰期较长,血药浓度较稳定[11],但是不同个体之间的药物浓度及给药剂量却相差很大,检测其血药浓度至关重要[12]。
中国药典2015年版(二部)规定采用HPLC测定盐酸美沙酮口服溶液中盐酸美沙酮的含量[13]。曾以乙腈-水为流动相,考察了不同配比,但峰形拖尾严重。梯度洗脱中流动相的水相可加入酸改变拖尾现象,本实验改加入0.1%甲酸后,峰形得到改善,减少了拖尾现象,并且增加了检测的灵敏度和精密度,提高了分离能力[14-15]。实验采用地西泮甲醇溶液作为内标物,进一步减少了检测干扰和系统误差。
本研究建立了一种UPLC-MS/MS测定盐酸美沙酮及其代谢产物EDDP含量的方法,专属性高,分离完全,检测时间快,并研究了其在大鼠体内的药动学,可以进一步为临床血药浓度监测和人体药动学试验提供依据。
[1] MARIENFELD C, ROSENHECK R A. Psychiatric services and prescription fills among veterans with serious mental illness in methadone maintenance treatment [J]. J Dual Diagn, 2015, 11(2): 128-135.
[2] MACEY T A, WEIMER M B, GRIMALDI E M, et al. Patterns of care and side effects for patients prescribed methadone for treatment of chronic pain [J]. J Opioid Manag, 2013, 9(5): 325-333.
[3] SULLIVAN S G, WU Z, CAO X, et al. Continued drug use during methadone treatment in China: a retrospective analysis of 19, 026 service users [J]. J Subst Abuse Treat, 2014, 47(1): 86-92.
[4] SWENSON O. Accidental methadone intoxication masquerading as asthma exacerbation with respiratory arrest in a six-year-old boy [J]. Del Med J, 2015, 87(5): 147-149.
[5] GHARIB B, FARSHADMOGHADAM H, HOSSEINI F, et al. Be careful of lies: a six-year-old boy with respiratory distress and decreased level of consciousness [J]. Acta Med Iran, 2014, 52(6): 481-483.
[6] PAD J R. Methadone drug interactions [J]. J Mainten Add, 2008, 2(3): 69-74.
[7] LIU X M, LI C Y, WANG M S. A study of safe dosage of methadone in drug abuse treatment [J]. Chin J Drug Abuse Pre Treat(中国药物滥用防治杂志), 2009, 15(6): 324-326.
[8] FAGGIANO F, VIGNA F. Methadone maintenance at different dosages for opioid dependence [J]. Cochrane Database Syst Rev, 2003(3): CD002208.
[9] LISTED N. Torsades de pointes with methadone [J]. Prescrire Int, 2005, 14(76): 61-62.
[10] GALLAGHER R. Management of painful wounds in advanced disease [J]. Can Fam Physician, 2010, 56(9): 883-885.
[11] WANG J, FU C X, WU W M, et al. Determination of plasma concentrations of methadone hydrochloride by HPLC [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2011, 28(4): 347-350.
[12] XU B S, SHUAI Y L, WANG Z Q, et al. The observation of clinical effects of methadone maintenance treatment [J]. Chin J Drug Abuse Prev Treat(中过药物滥用防治杂志), 2005, 11(2): 72-75.
[13] 中国药典. 二部[S]. 2015: 附录1045.
[14] SHAKLEYA D M, JANSSON L M, HUESTIS M A. Validation of a LC-APCI-MS/MS method for quantification of methadone,2-ethylidene-1, 5- dimethyl-3, 3-diphenylpyrrolidine(EDDP) and 2-ethyl-5- methyl-3, 3- diphenylpyraline (EMDP) in infant plasma following protein precipitation [J]. J Chromatogr B Anal Technol Biomed Life Sci, 2007, 856(1/2): 267-272.
[15] KISS B, BOGDAN C, POP A, et al. A rapid UPLC-MS/MS method for simultaneous determination of flunitrazepam, 7-aminoflunitrazepam, methadone and EDDP in human, rat and rabbit plasma [J]. Talanta, 2012, 99(18): 649-659.
(本文责编:李艳芳)
LI Hao
(Wenzhou People’s Hospital, Wenzhou 325000, China)
ABSTRACT:OBJECTIVE To propose a UPLC-MS/MS method for the determination of methadone hydrochloride and its metabolites 2-ethylidene-1,5-dimethyl-3,3-diphenylpyrrolidine(EDDP) in rat plasma. METHODS Diazepam was used as internal standard, rat plasma was precipitated with acetonitrile, the concentration of methadone hydrochloride and EDDP in the plasma of rats after intragastric administration methadone 6 mg·kg-1, determined by UPLC-MS/MS, and the data were analyzed. RESULTS The limit of quantitation was 0.5 ng·mL-1for both methadone hydrochloride and EDDP in rat plasma; the linear correlation coefficientr>0.999; the intra-day and inter-day RSDs were all < 15%; Absolute recovery rates were above 85%. The relative recoveries ranged from 90% to 110%; the matrix effect ranged from 92.80% to 97.71%. The main pharmacokinetic parameters of methadone and EDDP were as follow:t1/2of methadone and EDDP were (1.479±0.839), (2.590±0.760) h;Cmaxwere (48.562±10.501), (25.542±3.706)mg·L-1; MRT0-twere (3.476±0.310), (3.883±0.514) h; AUC0-twere (204.036±61.145), (86.031±15.287)mg·h·L-1;CLwere (32.338±14.343), (70.137±10.786) L·h-1·kg-1, respectively, and there were significant differences in the parameters between the rats before and after being administrated with methadone and EDDP. CONCLUSION The method is proved to be highly sensitive, selective, and has been successfully applied to the determination of methadone hydrochloride and its metabolite EDDP, and can be used for pharmacokinetic studies in rats.
KEY WORDS:UPLC-MS/MS; methadone; EDDP; plasma concetration
中图分类号:R917
文献标志码:B
文章编号:1007-7693(2017)09-1277-05
DOI:10.13748/j.cnki.issn1007-7693.2017.09.013
引用本文:李好. UPLC-MS/MS快速测定大鼠血浆中盐酸美沙酮及其代谢产物含量[J]. 中国现代应用药学, 2017, 34(9): 1277-1281.
基金项目:2016年浙江省温州市科技计划项目(Y20160543)
作者简介:李好,女,硕士,主管药师 Tel: (0577)88059580 E-mail: lh1804@163.com
收稿日期:2017-01-11