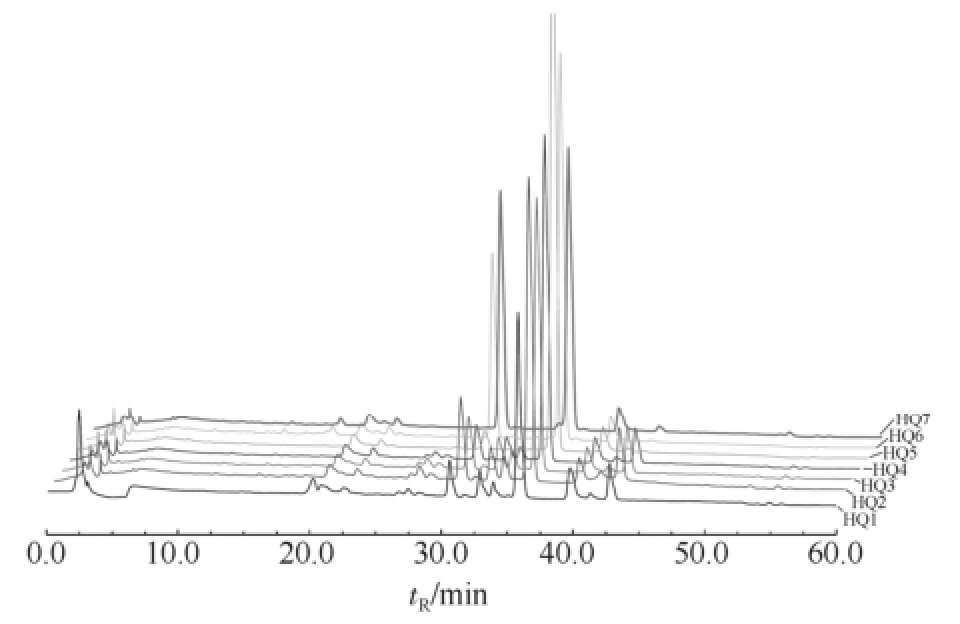
图1 不同样品的高效液相色谱图
Fig.1 HPLC chromatograms of different samples
余立雁 1,潘荣华 2,王倩倩 1,郑立忠 2,马忠俊 1*(1.浙江大学海洋学院,浙江 舟山 316021;2.浙江三禾生物工程股份有限公司,浙江 江山 324123)
摘要:目的 建立基于LC-TOF/MS技术的分析方法,检测功能性红曲中非法添加非红曲来源的洛伐他汀。方法 红曲样品的甲醇提取物经Zorbax SB-C 18(4.6 mm×150 mm,5 μm)色谱柱,以0.05%甲酸水溶液-乙腈为流动相梯度洗脱(0~40 min,40%~100%乙腈),正离子扫描检测。结果 非法添加非红曲来源的洛伐他汀的功能性红曲存在天然功能性红曲没有的特征杂质离子峰,可以区分非法添加非红曲来源的洛伐他汀的功能性红曲和天然功能性红曲。结论 本方法可用于天然功能性红曲是否非法添加非红曲来源的洛伐他汀的鉴别。
关键词:红曲;非法添加;洛伐他汀;杂质
红曲是以大米为原料,利用真菌红曲霉(Monascus spp.)经固态发酵而成的天然产品,它因具有良好的降血脂功能而备受国内外消费者的青睐 [1]。经研究,红曲作为一种功能性食品,其降血脂的功效成分主要为他汀类化合物 [2],其主要代谢产物洛伐他汀(lovastatin,又名Monacolin K),能够抑制胆固醇合成过程中的限速酶3-羟基-3-甲基戊二酰辅酶A(HMG-CoA)还原酶,从而调节脂肪代谢 [3]。作为红曲中含量最高,且降血脂作用明确的代谢产物,洛伐他汀含量是评价红曲质量行业标准的主要指标。国家食品药品监督管理局“国食药监许[2010]2号文件”规定红曲产品中洛伐他汀应当来源于红曲,然而,针对非法添加人工洛伐他汀的行为,目前还没有任何有效的检测方法可以评价功能性红曲中是否非法添加了非红曲来源的洛伐他汀 [3-5]。本研究针对上述问题,探讨了基于人工洛伐他汀的杂质成分,分别采用HPLC和LC-TOF/MS检测红曲中人工洛伐他汀的可能性,结果表明,所建立的LC-TOF/MS能较好地区别天然红曲和非法添加洛伐他汀的红曲。
Thermo DIONEX Ultimate 3000高效液相色谱仪(美国赛默飞)及Sepax C 18-H色谱柱(250 mm× 4.6 mm,5 µm);Agilent TOF 6230 LC/MS高效液相色谱质谱联用仪(美国Agilent)及Zorbax SB-C 18(150 mm×4.6 mm,5 µm)色谱柱;DS5510DTH超声波清洗器(上海生析超声仪器有限公司);SHIMADZU AUW120D电子分析天平(日本岛津)。
甲醇、甲酸(分析纯,国药集团);乙腈(色谱纯,百灵威);三氟乙酸(分析纯,美国Sigma);水为超纯水;洛伐他汀对照品(美国Sigma,批号:0749-9404,含量:98%);7种功能性红曲(HQ1~HQ7)由浙江三禾生物工程股份有限公司提供,标示的洛伐他汀含量分别为1.5%,3%,3%,3%,5%,5%,5%,其中HQ1~HQ3为未添加洛伐他汀的天然红曲,HQ4非法添加了1.5%的人工洛伐他汀,HQ5、HQ6为国内添加人工洛伐他汀的样品,HQ7为比利时添加人工洛伐他汀的样品。
2.1 溶液制备
2.1.1 对照品溶液的制备 取洛伐他汀对照品适量,精密称定,加甲醇制成10 mg·mL -1的对照品溶液。
2.1.2 供试品溶液的制备 取不同来源功能红曲适量,以30 mg·mL -1比例加入甲醇,超声10 min,滤过,即得。
2.2 HPLC的鉴别
2.2.1 分析方法 流动相:乙腈-水(含0.05%三氟乙酸);梯度洗脱程序:0~50 min,20%→100%乙腈;流速:1 mL·min -1;检测波长:230 nm;柱温:40 ℃;进样量:10 μL。
2.2.2 分析结果 7个红曲供试品的HPLC图见图1,其中洛伐他汀的保留时间t R为36.05 min。除洛伐他汀外,洛伐他汀对照品还显示了9个杂质色谱峰,保留时间t R分别为20.92,27.28,28.74,33.66,34.58,37.31,38.15,39.89,42.94 min,7个供试红曲样品杂质色谱峰的检测结果汇总如表1,结果显示,可检测的杂质色谱峰并不能有效区分7个供试样品。

图1 不同样品的高效液相色谱图
Fig.1 HPLC chromatograms of different samples
表1 红曲样品与人工洛伐他汀杂质峰比较分析
Tab.1 Comparison analysis of lovastatin and RYRs

注:+表示有相应的色谱峰。
Note: +means detectable peaks.
2.3 LC-TOF/MS鉴别
2.3.1 高效液相色谱条件 流动相:0.05%甲酸水溶液-乙腈;梯度洗脱程序:0~40 min,40%~100%乙腈;流速:0.6 mL·min -1;检测波长:230 nm;柱温:40 ℃;进样量:10 μL。
2.3.2 质谱条件 电喷雾离子源(ESI);正离子扫描;毛细管温度:300 ℃;脱溶剂管温度:250 ℃;加热块温度:400 ℃;雾化气流量:3.0 L·min -1;干燥气流量:12.0 L·min -1;加热气流量:12.0 L·min -1;喷雾电压:+4.5 kV。
2.3.3 定性分析结果 对人工洛伐他汀的总离子流图(TIC)进行分析,共从中获得38个较为明显的离子峰信号,根据出峰时间先后分别如下:m/z 477.2,491.2,461.2,507.2,461.2,441.2,475.2,536.3,459.2,475.2,611.3,475.2,491.2,443.2,274.3,318.3,443.2,459.2,489.2,459.2,443.2,427.2,302.3,520.3,441.2,443.2,459.2,330.3,374.3,413.2,429.2,425.2,442.4,427.2,358.3,506.3,429.2,409.2。根据从洛伐他汀所获得的杂质离子信号,分别从7个供试品中提取相应的分离子流图(EIC),经对比分析,发现6个离子信号m/z 536.3,358.3,491.2,475.2,429.2,611.3存在于不同的功能红曲样品中,比较结果见表2。红曲样品HQ1、HQ2、HQ3均不含上述杂质离子,而红曲样品HQ4、HQ5、HQ6、HQ7不同程度地含有上述杂质离子,因此,初步推断HQ1、HQ2、HQ3为未非法添加洛伐他汀的天然红曲,HQ4极有可能非法添加了洛伐他汀,HQ5、HQ6、HQ7非法添加了洛伐他汀,HQ1~HQ3的分析结果与实际一致。
表2 红曲样品与人工洛伐他汀杂质峰比较分析
Tab.2 ESI comparison analysis results of lovastatin and RYRs
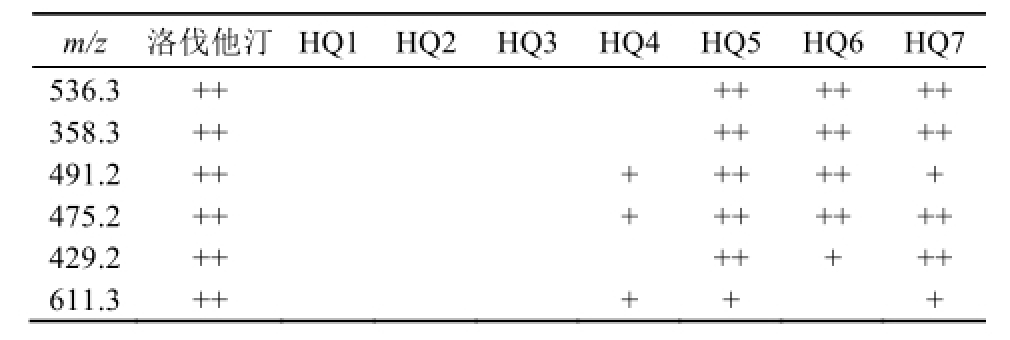
注:+表示有相应的离子信号;++表示有较强的离子信号。
Note: + means weak ion signals; ++ means obvious ion signals.
2.3.4 初步定量分析结果 定性分析获得的6个离子可以区别不同红曲样品的离子信号m/z 536.3,358.3,491.2,475.2,429.2,611.3对应的EIC色谱图积分,对信噪比>3的色谱峰进行比对分析。以洛伐他汀标准品1 μg的离子信号响应值为基准,不同供试红曲中等量洛伐他汀含有的杂质离子信号的响应值汇总见图2。定量分析结果结合实际杂质添加情况,保留时间t R为10.62 min(m/z 536.3)、11.76 min(m/z 536.3)、12.44 min(m/z 536.3)、13.45 min(m/z 536.3)、8.69 min(m/z 491.2)和8.69 min(m/z 475.2)的离子信号,能很好区分天然红曲和非法添加了洛伐他汀的红曲,可以作为添加洛伐他汀的特征杂质离子。尽管所用的质谱不能精确定量,但为区别杂质信号和初步定量提供了必要的信息。

图2 不同红曲样品中洛伐他汀杂质信号的相对响应值
Fig.2 Relative signal strength of impurity ions of different samples
本研究分别探讨了基于HPLC和LC-TOF/MS技术鉴别天然功能红曲是否非法添加外源洛伐他汀的可能性。结果表明,HPLC杂质色谱峰比较分析并不能区别不同程度添加洛伐他汀的红曲。由于人工洛伐他汀通常来源于微生物发酵,因此,HPLC可检测的杂质色谱峰,极有可能是洛伐他汀生物合成过程中的同系物或降解产物,因此和红曲中色谱峰相似,而其它可能存在的特征杂质,由于HPLC检测限的原因,并不能在HPLC比较分析中得到体现。本研究所建立的基于LC-TOF/MS技术的分析方法 [6],通过定性比较分析所得的6个特征杂质离子的EIC图,可以较好地判断功能红曲中是否非法添加了非红曲来源的洛伐他汀,进一步定量分析比较,获得的6个离子,通过离子信号强度,可以精确地判断功能红曲中是否非法添加了非红曲来源的洛伐他汀,验证了LC-MS用于检测功能红曲中人工洛伐他汀的可能性。由于不确定本实验所用的洛伐他汀对照品和供试红曲中非法添加的洛伐他汀是否相同,不能确定两者所含的杂质含量是否相同,所以本实验只能依据红曲中杂质信号与洛伐他汀中的信号强度粗略地估算红曲中添加洛伐他汀的量,未能精确定量供试品中非法添加的非红曲来源的洛伐他汀的含量,如果所用的人工洛伐他汀对照品和供试红曲中非法添加的洛伐他汀一致,结合定量LC-MS分析仪器,本研究所建立的检测方法可以初步定量分析非功能红曲来源的洛伐他汀的添加量。此外,非功能红曲来源的杂质信号代表的化合物需要进一步的提取分离并进行NMR等测试后才能确定其结构,这些化合物有可能成为鉴别添加了非功能红曲来源的洛伐他汀的功能红曲产品的标志性成分。
REFERENCES
[1] KASLIWAL R R, BANSAL M, GUPTA R, et al. ESSENS dyslipidemia: A placebo-controlled, randomized study of a nutritional supplement containing red yeast rice in subjects with newly diagnosed dyslipidemia [J]. Nutrition, 2016, 32(7/8): 767-776.
[2] PATEL S. Functional food red yeast rice (RYR) for metabolic syndrome amelioration: a review on pros and cons [J]. World J Microbiol Biotechnol, 2016, 32(5): 87. doi: 10.1007/s11274-016-2035-2. Epub 2016 Apr 2.
[3] LI M, TAI X S, FENG J L, et al. Research progress on the microbial lovastatin [J]. Sci Technol Food Indust(食品科技), 2011, 32(8): 457-460.
[4] LU Z J, QI W W, X Y. Analysis of the red fermented rice from different manufacturers by HPLC [J]. Food Nut China(中国食品与营养), 2014, 20(9): 38-41.
[5] YANG Y, ZHENG R J, HUA Y Y, et al. High performance liquid chromatographic analysis of lovastatin (lactone) and lovastatin acid in red yeast rice [J]. Chin J Health Lab Tec(中国卫生检验杂志), 2014, 24(12): 1714-1717.
[6] SHEN H L, PENG Y W, YANG M Z. Study on detection method of chemical drugs illegally added in Shuimianbao Capsules [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2015, 32(6): 724-727.
Adulteration Detection of Lovastatin in Red Yeast Rice by LC-TOF/MS
YU Liyan 1, PAN Ronghua 2, WANG Qianqian 1, ZHENG Lizhong 2, MA Zhongjun 1*(1.Ocean College, Zhejiang University, Zhoushan 316021, China; 2.Zhejiang Sanhe Bio-tech Co., Ltd., Jiangshan 324123, China)
ABSTRACT:OBJECTIVE To establish an analysis method to detect the adulteration of lovastatin in red yeast rice by LC-TOF/MS. METHODS Methanol extract of red yeast rice was subject to LC-MS analysis by applying Zorbax SB-C 18(4.6 mm×150 mm, 5 μm) column, eluted using water supplied with 0.05% formic acid-acetonitrile with gradient elucidation (0~40 min, 40%~100% acetonitrile), and scanned in positive ion mode . RESULTS Comparison analysis led to the finding of typical ions could specifically distinguish adulterated lovastatin in red yeast rice. CONCLUSION The established LC-MS analysis method can be applied for adulteration detection of lovastatin in red yeast rice.
KEY WORDS:red yeast rice; adulteration; lovastatin; impurities
中图分类号:R917.101
文献标志码:B
文章编号:1007-7693(2017)02-0266-03
DOI:10.13748/j.cnki.issn1007-7693.2017.02.024
收稿日期:2016-08-03
作者简介:余立雁,女,博士 Tel: 13588702160 E-mail: yuliyan2160@126.com *
通信作者:马忠俊,男,博士,教授 Tel: 13588090752 E-mail: mazj@zju.edu.cn