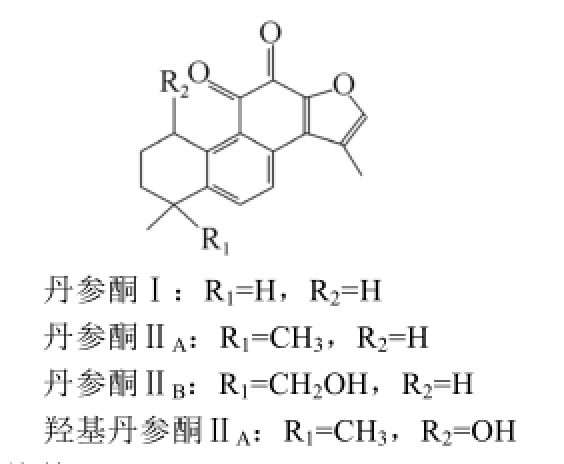
图1 丹参酮结构
Fig.1 Structures of tanshinones
章 靓,严国鸿,江 川 *,刘智勇,郭晓芳,陈成辉,何丽君(福建中医药大学附属人民医院药学部,福州 350004)
摘要:目的 利用反向分子对接方法预测丹参酮抗血小板可能的作用靶点及作用机制。方法 以丹参酮Ⅱ B为代表,采用Autodock Vina软件,把丹参酮Ⅱ B与抗血小板的靶蛋白进行反向对接。利用Discovery Studio Visualizer 4 软件对丹参酮Ⅱ B与靶蛋白的作用模式进行分析。结果 丹参酮Ⅱ B能与GP Ⅱb/Ⅲa很好地结合,且丹参酮Ⅱ B的结合能明显优于原有配体RUC-2(IC 50为96 nmol·L -1)。结论 GPⅡb/Ⅲa可能是丹参酮Ⅱ B抗血小板的潜在靶标。
关键词:丹参酮;抗血小板;分子反向对接
在血栓形成过程中血小板聚集发挥着关键作用。血小板活化所引起的动脉粥样硬化斑块破裂,血小板聚集及血栓形成是急性冠脉综合征、急性心肌梗死的病理生理学共性,也是直接经皮冠脉介入治疗患者突发远端血管阻塞的主要原因 [1]。目前抗血小板药如阿司匹林、氯吡格雷、双嘧达莫、奥扎格雷钠、替罗非班等主要通过6条途径抑制血小板的功能和聚集而发挥抗凝血作用,但也潜在出血等不良反应。
丹参及其复方制剂或提取物作为活血化瘀药物,在临床上广泛运用于心血管疾病特别是抗血栓的治疗。现代药理学研究表明,丹参及其制剂可以有效抑制血小板活化、聚集,具有防止血栓形成、抗凝、抗动脉粥样硬化的作用 [2],同时安全性高、出血的不良反应少。丹参的主要有效成分为丹参酮、丹参多酚酸和丹参素等 [3],其中以丹参酮类抗血小板作用最明显。
尽管目前已对丹参酮抗血小板的临床疗效做了较深入的观察,但丹参酮的作用靶标及分子药理机制依然不清楚。在药物研发过程中,为弥补传统药物研发手段的盲目性及高成本,计算机分子模拟研究已经广泛地应用于中药有效成分的确定和作用机制的研究 [4]。其中,以小分子化合物为探针,在已知结构的靶点数据库内寻找与之结合的生物大分子,并通过空间和能量匹配相互识别形成分子复合物,从而预测药物潜在作用靶点的反向分子对接技术,在探索小分子的药理作用及机制等方面得到了广泛的认可,该技术可以用来寻找药物可能的作用靶标及作用机制,也可用于药物的不良反应分析 [5-6]。
本研究拟通过反向分子对接技术,把丹参酮与已知的抗血小板靶蛋白进行反向对接,确定丹参酮的可能作用靶标,以期从分子相互作用的角度探讨丹参酮抗血小板聚集的作用机制,为丹参的药理作用提供进一步的理论依据,同时也为后续的新药发现及改造提供基础。
1.1 丹参酮分子的构建
丹参酮具有4个亚型 [2],分别为丹参酮Ⅰ,丹参酮ⅡA,丹参酮Ⅱ B和羟基丹参酮,具体结构见图1。由于这4个结构都比较类似,为了简化计算和分析处理,本研究以丹参酮Ⅱ B为例,进行探讨。丹参酮Ⅱ B的立体结构使用分子模拟图形界面软件Discovery Studio Visualizer 4(DSV4)进行绘制,并利用Dreiding-like力场对丹参酮Ⅱ B的结构进行优化。

图1 丹参酮结构
Fig.1 Structures of tanshinones
1.2 靶点收集与准备
从蛋白数据库(protein data bank, PDB)(http: //www.rcsb.org/)中搜索具有抗血小板作用的靶点:对于含有多个晶体结构的靶点,只保留含有复合物的、且分辨率最高的靶点(表1)。靶蛋白晶体结构从PDB数据库获得,导入到DSV4(http:// accelrys.com/),去除自带配体,进行整体分析、加氢及修正不完整的残基等处理。
表1 抗血小板作用靶点
Tab.1 Potential targets of antiplatelet

1.3 反向分子对接
采用Autodock Vina V 1.1.2为对接软件 [7],以靶蛋白原配体的中心作为活性位点的中心,同时设定Grid box盒范围大小设定为10,作为靶蛋白的活性位点,其他参数采用默认值。在对接过程中,只改变配体的构象,而保持蛋白构象不变。利用Autodock Vina软件,计算得到丹参酮Ⅱ B与靶蛋白的结合能。在结果处理过程中,只保留与丹参酮Ⅱ B结合能最低的一个。同时根据公式K i=exp[(ΔG×1 000)/(Rcal×T)],其中ΔG单位为kcal·mol -1,T=300 K,Rcal=1.987 19 cal·mol -1·K -1,计算得到丹参酮Ⅱ B对靶蛋白的抑制常数(K i)。
1.4 对接结果显示及相互作用分析
分子对接的结果显示及相互作用的分析都是基于DSV4软件进行的。
2.1 对接方法的检验
为了检验对接方法的可靠性,选择4个晶体结构(PDB编号分别为3LN1,4NTJ,1Q4G,3T3M),将原有配体重新对接到其对应的空受体中,然后比较配体对接后的预测构象与晶体中构象的差异。4个晶体结构中,配体在对接后的预测结合构象与原先在晶体结构中的构象可以基本重合,仅有较小的差异(2个构象间的均方根偏差RMSD都<0.5,见表2),结果见图2。以上结果表明,分子对接能够较好地重现晶体结构中的结合构象,表明其具有较强的预测能力,能够用于丹参酮的反向对接研究。
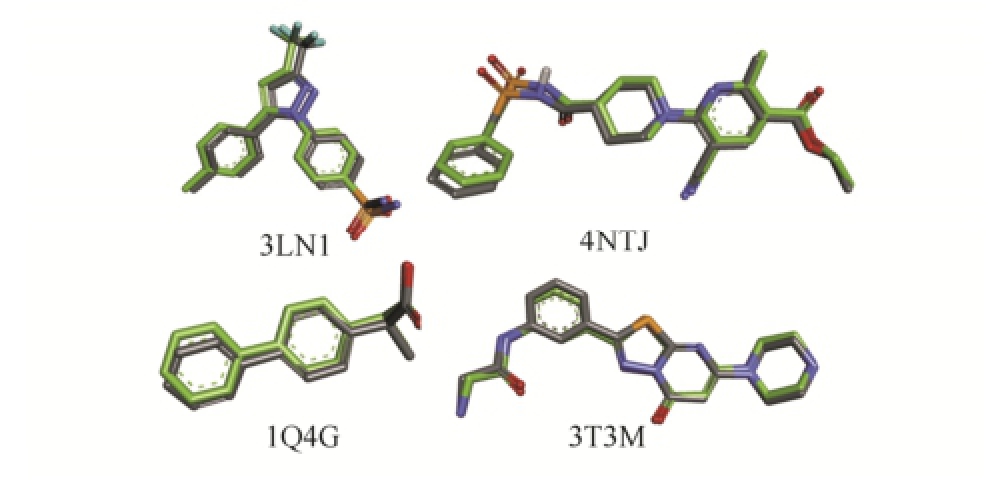
图2 配体对接构象与其晶体中构象的比较
Fig.2 The docked poses compared with their co-crystal structures
表2 配体对接的打分值以及其与晶体结构构象的均方根偏差(RMSD)
Tab.2 The docking scores and RMSD between the docked poses and their co-crystal structures

2.2 丹参酮反向对接
利用分子对接软件AutoDock Vina,考察丹参酮Ⅱ B与具有抗血小板作用的各靶点间结合能的好坏和潜在的相互作用模式。Vina评价小分子与蛋白质结合的好坏主要通过结合能(Affinity)来表示,即计算后拟合得到的ΔG值,值越小表示结合能越高,药物越容易与受体结合。丹参酮Ⅱ B与磷酸二酯酶、环氧化酶1/2以及GP Ⅱb/Ⅲa 都能够较好地结合,结果见表3。这可能与这些靶点都含有一个较深且疏水性强的结合位点有关,由于丹参酮为二萜化合物,含有一个较大的疏水性杂环,因此对接打分时都能得到较好的结果。
表3 反向对接的筛选结果
Tab.3 The results of reverse docking

然而,不同靶点间亲和力的大小并无可比性。当药物与受体的结合能小于内源性配体时,药物将难以竞争过内源性配体而跟受体结合;当药物与受体的结合能高于内源性配体时,即使药物在该靶点的结合能比在其他靶点低,药物也能很好地竞争结合到受体上。因此,在比较对接结果时,并不能简单地以结合能进行比较,还应考虑靶点本身与其内源性配体或有效药物间的亲和力大小,以评估化合物是否具有竞争优势。为此,本研究比较了丹参酮Ⅱ B与蛋白结晶自带配体的结合能及抑制常数K i。通过比较发现,在磷酸二酯酶及环氧化酶1/2中,丹参酮Ⅱ B的抑制常数比内源性配体小得多,不具备竞争优势。而对于GP Ⅱb/Ⅲa,丹参酮Ⅱ B的结合能明显优于原有配体RUC-2(IC 5096 nmol·L -1),表明GP Ⅱb/Ⅲa极有可能是丹参酮Ⅱ B的靶点。
2.3 丹参酮Ⅱ B与GP Ⅱb/Ⅲa相互作用分析
为了从分子层次上揭示丹参酮Ⅱ B抗血小板作用的机制,本研究对丹参酮Ⅱ B与GP Ⅱb/Ⅲa的结合构象和作用模式进行了分析。从GP Ⅱb/Ⅲa与药物RUC-2复合物的晶体结构3T3M可以看到,药物与蛋白的结合位点位于蛋白C链和D链结合交界处的上方口袋中。丹参酮Ⅱ B上的醇羟基作为氢键供体,与GP Ⅱb/Ⅲa C链中苯丙氨酸(C:PHE160)骨架上的羰基形成了一个氢键相互作用;此外二酮结构能够与D链丙氨酸(D:ALA218)骨架上的氨基形成一个较弱的氢键,结果见图3。但与丹参酮Ⅱ B相互作用最明显的要属C链上的190位酪氨酸(C:TYR190),由于它靠近丹参酮的骨架芳环且几近平行,能够与多环结构上的3个芳香环形成明显的π-π相互作用。除此之外,丹参酮Ⅱ B的结合位点周围有多个疏水性残基,如C:TYR190,C:PHE160,C:Leu192,C:PHE231,D:PRO219这些残基形成一个疏水性口袋,与丹参酮形成多个疏水相互作用,进一步加强丹参酮Ⅱ B结合的稳定性。
与Zhu等 [8]发现的GP Ⅱb/Ⅲa高活性抑制剂(IC 5096 nmol·L -1)RUC-2的相互作用进行比较,二者之间有些类似:RUC-2与靶点最明显的相互作用为C:TYR190与RUC-2上的2个芳香环(苯环和吡啶并噻二唑环)形成较强的π-π相互作用;RUC-2与靶点也有多个氢键相互作用(C:Asp224,D:Glu220,D:Asn215);此外,RUC-2与靶点残基存在诸多疏水相互作用,见图4。
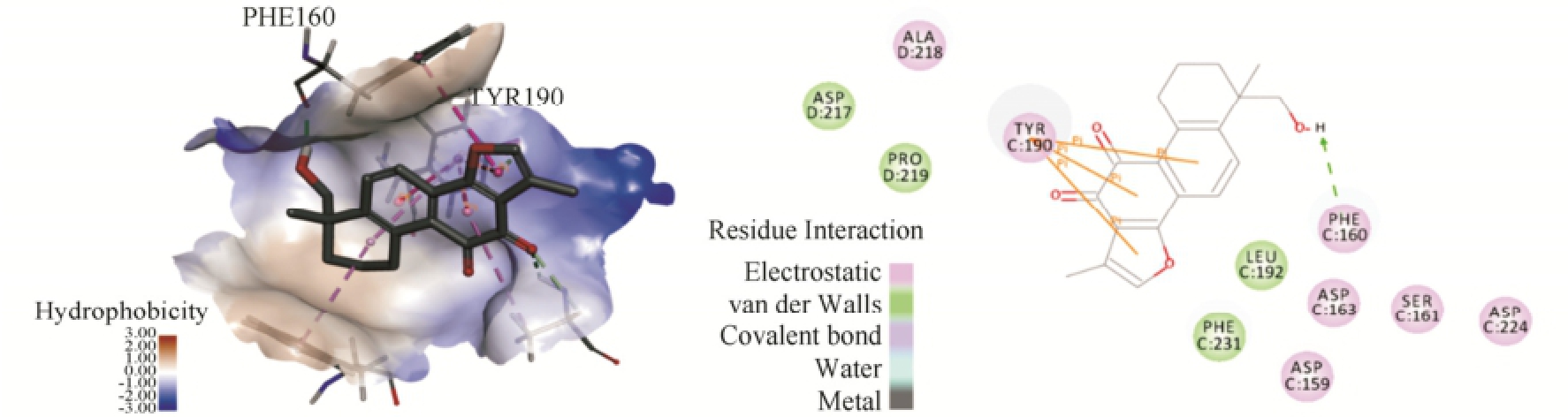
图3 丹参酮Ⅱ
B与GPⅡb/Ⅲa的相互作用
Fig.3 The interactions between tanshinone ⅡB and GP Ⅱb/Ⅲa
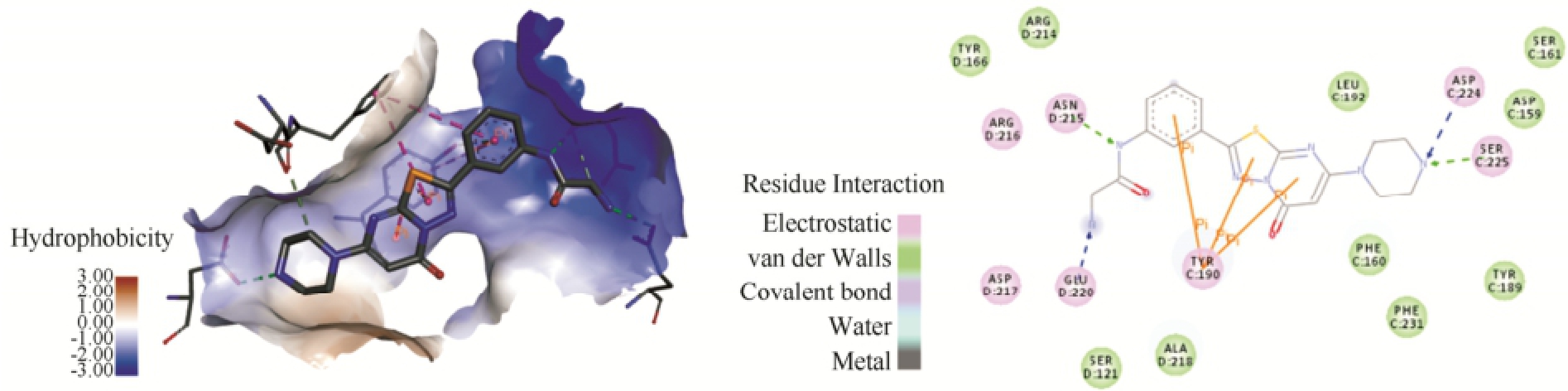
图4 GPⅡb/Ⅲa与其高活性配体RUC-2的相互作用
Fig.4 The interactions between GPⅡb/Ⅲa and its high-affinity ligand RUC-2
通过分子对接研究,发现丹参酮Ⅱ B能够较好地与GPⅡb/Ⅲa相结合,且亲和力高于GPⅡb/Ⅲa的高活性配体RUC-2,说明丹参酮Ⅱ B的抗凝血作用极有可能是通过结合于GPⅡb/Ⅲa,抑制GPⅡb/Ⅲa活性而起作用的。
2.4 丹参酮对血小板膜粘附分子的表达影响
在血栓形成过程中,GPⅡb/Ⅲa起着极其重要的作用。它经“由内到外”的信号激活后,与纤维蛋白原的亲和力显著增加,引起血小板聚集,是血小板聚集和血栓形成的一个关键因子 [9]。GP Ⅱb/Ⅲa与纤维蛋白原的结合是ADP、凝血酶、胶原、肾上腺素等多种血小板激活剂诱导血小板聚集过程中的最后共同途径,结果见图5。CD41是GPⅡb/Ⅲa受体的亚基,GPⅡb/Ⅲa是凝血因子I受体,只有当血小板被活化时,凝血因子I才能与血小板结合,同时GPⅡb/Ⅲa与血浆或组织中的一些黏附蛋白结合,介导血小板聚集,这一控制功能是通过GPⅡb/Ⅲa的功能状态得以实现。CD62P也称P选择素或血小板α颗粒膜蛋白(GMP-140),介导活化血小板与中性粒细胞和单核细胞的黏附,活化的血小板通过表达CD62P与白细胞特意黏附,使白细胞停留在血管破损或血栓形成处。

图5 抗血小板药物的作用机制
Fig.5 The mechanism of antiplatelet drugs
孙学刚等 [10]研究表明,丹参酮能减少大鼠CD41和CD62P的表达(P<0.05),减少心律失常大鼠的死亡率。余雅婷 [11]对90例不稳定型心绞痛患者使用复方丹参滴丸的临床疗效及血小板活化功能进行观察,结果表明复方丹参滴丸组的CD62P、GMP-140均明显低于对照组(P<0.05)。这与本课题组预测的丹参酮Ⅱ B的抗凝血作用极有可能是通过结合于GPⅡb/Ⅲa,抑制GP Ⅱb/Ⅲa活性而起作用相一致。
本研究采用反向分子对接原理,使用Autodock Vina对丹参酮Ⅱ B抗血小板的潜在靶蛋白进行了分析。分析结果表明丹参酮Ⅱ B能够较好地与抗血小板聚集关键靶标GPⅡb/Ⅲa进行结合,说明GPⅡb/Ⅲa可能是丹参酮类抗血小板作用的靶点。
虽然反向分子对接技术在提高药物研发成功率、降低研发成本、缩短研发周期等方面具有优势,但理论计算始终不能替代药理实验数据,本研究为丹参酮类药物开发提供理论参考,为分子机制研究提供方向,但最终还需要药理药效学实验进行验证。
REFERENCES
[1] WANG M, GUZILINUER T. Clinical efficacy of yinxingdamo injection combined with antithrombotic therapy for treating the patients with acute coronary syndrome [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2011, 28(S1): 1379-1381
[2] XIONG J H, YANG J Z, YE H, et al. Effects of TanshinoneⅡA on the pharmacokinetics of theophylline in rats [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2015, 32(8): 966-970.
[3] WANG Y, CHEN T, PANN L, et al. Application of liquid chromatography coupled with mass spectrometry technique in component analysis of Salvia miltiorrhiza [J]. Chin Tradit Herb Drugs(中草药), 2014, 45(23): 3494-3502.
[4] ZHU W, YAO L M. Virtual screening for small molecule inhibitors of tumor necrosis factor-α based on database of traditional Chinese medicine [J]. Chin J Exp Tradit Med Form(中国实验方剂学杂志), 2010, 16(13): 199-202.
[5] ZHANG M B, LI L, SUN Y T, et al. Study on antitumor mechanism of quercetin based on molecular reverse docking method [J]. Chin J Exp Tradit Med Form(中国实验方剂学杂志), 2012,18(23):145-148
[6] ZHU Z Y, ZHANG Y, LI Z, et al. Progress in receptor protein & drug molecule docking approaches [J]. Chin J Clin Pharmacol Ther(中国临床药理学与治疗学), 2009, 14(11): 1308-1313.
[7] TROTT O, OLSON A J. Autodock vina: Improving the speed and accuracy of docking with a new scoring function,efficient optimization, and multithreading [J]. J Comput Chem, 31(2): 455-461.
[8] ZHU J Q, CHOI W S, MCCOY J G, et al. Structure-guided design of a high-affinity platelet integrin α Ⅱbβ 3receptor antagonist that disrupts Mg 2+binding to the MIDAS [J]. Sci Transl Med, 2012, 4(125): 125ra32. Doi: 10.1126/ scitranslmed.3003576.
[9] ZHANG L, CHEN W, PANG W S, et al. Mechanism of thrombosis and IIb/IIIa receptor antagonist: platelet glycoprotein: a research progress [J]. J Int Pharm Res, 2009, 36(4): 268-271.
[10] 孙学刚, 贾钰华, 陈育尧. 定心方及丹参酮对血小板膜粘附分子表达的影响[J]. 山东中医药大学学报, 2001, 25(1): 61-63.
[11] YU Y T. The influce of Compound Danshen Dripping pills on platelet activation function in patients with unstable angina [J]. China Med Pharm(中国医药科学), 2014, 4(6): 91-92.
Study of Prediction Antiplatelet Potential Targets of TanshinoneⅡ Bby Reverse Molecule Docking
ZHANG Jing, YAN Guohong, JIANG Chuan *, LIU Zhiyong, GUO Xiaofang, CHEN Chenghui, HE Lijun (Department of Pharmacy, People’s Hospital Affiliated to Fujian University of Traditional Chinese Medicine, Fuzhou 350004, China)
ABSTRACT:OBJECTIVE To predict the potential targets and the mechanism of tanshinones against platelet activation by reverse docking. METHODS The reverse docking was performed based on Autodock Vina, where tanshinone II B(Tan II B) was screened against several targets that may be activated in platelet aggregation. The interactions between targeted proteins and ligands were analyzed using Discovery Studio Visualizer 4 software. RESULTS Tan Ⅱ Bcan be well docked into GP Ⅱb/Ⅲa with a better predicted affinity than the original ligand RUC-2 (IC 50=96 nmol·L -1). CONCLUSION GP Ⅱb/Ⅲa is the most possible target for the Tan Ⅱ B.
KEY WORDS:tanshinones; antiplatelet; reverse docking
中图分类号:R914.2
文献标志码:A
文章编号:1007-7693(2017)02-0221-04
DOI:10.13748/j.cnki.issn1007-7693.2017.02.015
收稿日期:2016-06-28
作者简介:章靓,女,硕士,主管药师 Tel: (0591)83947134 E-mail: smxls522@126.com *
通信作者:江川,男,副主任药师 Tel: (0591)83947179 E-mail: 442556540@qq.com