图1 当归的TLC色谱图
1~3-复方制剂;4-阿魏酸;5-当归对照药材;6-阴性对照。
Fig. 1 TLC graph of Angelicae Sinensis Radix
1~3-compound preparation; 4-ferulic acid; 5-reference of Angelicae Sinensis Radix; 6-negative sample.
余晓晖1,2,樊秦1,2,赵磊1,2,王永刚1,杨蕊菁1,宋娇娇1
(1.甘肃中医药大学,兰州 730000;2.甘肃省高校中(藏)药化学与质量省级重点实验室,兰州 730000)
摘要:目的 建立复方当归妇炎微灌肠剂的质量控制方法。方法 根据处方组成,采用TLC对制剂中的当归、赤芍、延胡索进行定性鉴别。以HPLC测定当归中阿魏酸、赤芍中芍药苷的含量:采用Extend-C18(4.6 mm×250 mm,5 μm)色谱柱;以乙腈-0.1%磷酸(15∶85)为流动相等度洗脱;柱温25 ℃;流速1 mL·min-1;检测波长320,234 nm。结果 阿魏酸和芍药苷分别在 0.002 4~0.011 9 mg·mL-1(r=0.999 4),0.036 4~0.081 9 mg·mL-1(r=0.999 2)内呈良好的线性关系;平均加样回收率分别为100.3%,98.9%,RSD分别为1.08%,0.68%。结论 该方法简便、准确、稳定性好,可用于该制剂的质量控制。
关键词:微灌肠剂;质量标准;当归;赤芍;延胡索
复方当归妇炎微灌肠剂原处方由当归、赤芍、延胡索、大血藤、鸡血藤等10味中药组成,为嘉峪关市胜利社区医院的院内制剂,已有长期的临床疗效,主要用于慢性盆腔炎[1]。此制剂本为普通灌肠剂,经剂型改造将其改进为微型灌肠剂。该制剂中当归补血活血,调经止痛,润肠通便,赤芍清热凉血,活血散瘀,这 2味药材均为方中君药。为有效控制该制剂质量,本实验采用TLC对方中君药当归、赤芍,臣药延胡索进行定性鉴别。采用 HPLC建立方中君药当归中阿魏酸、赤芍中芍药苷含量测定方法,为该制剂的进一步开发提供依据。
Agilent 1100高效液相色谱仪系列(美国Agilent公司,二元梯度泵,自动进样器,恒温进样器,柱温箱,二极管阵列检测器);Extend-C18(4.6 mm×250 mm,5 μm)色谱柱;SK3300H 数控超声波清洗器(昆山市超声仪器有限公司);BT125D电子天平(梅特勒-托利多,十万分之一);WB0830026电子天平(梅特勒-托利多,万分之一);AL104电子天平(梅特勒-托利多仪器上海有限公司);BPI105 电子分析天平(德国 Sartorius);KQ-250超声波清洗仪器(昆山市超声仪器有限公司)。
复方当归妇炎微灌肠剂(由实验小组制备)。
中药材:赤芍、当归、延胡索(元胡)、鸡血藤、大血藤、薏米仁、败酱草、小茴香,购于黄河药市,由甘肃中医药大学药学院晋玲教授鉴定,均符合中国药典2015年版一部标准。
对照品:芍药苷(成都克洛玛生物科技有限公司,批号:CHB161227,纯度:98.9%)、阿魏酸(成都克洛玛生物科技有限公司,批号:CHB160913,纯度:98.1%)、延胡索乙素 (上海源叶生物科技有限公司,批号:Y21S7Y17091,纯度:98.6%)。对照药材:赤芍(批号:121093-201303)、当归(批号:120927-201516)、延胡索(元胡,批号:120928-201208),均购于中国食品药品检定研究院。硅胶G(青岛海洋化工有限公司);水为超纯水;甲醇、乙腈均为色谱纯;其余试剂均为分析纯。
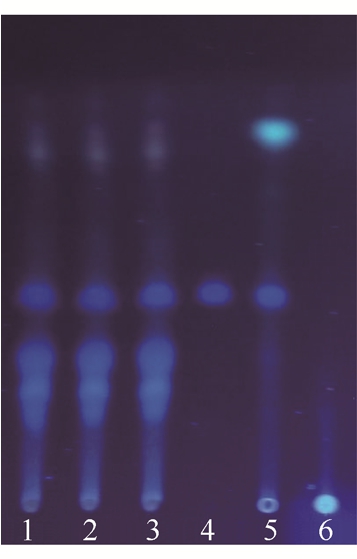
2.1.1 当归的TLC鉴别[2-3]精密称取制剂10 g,加甲醇40 mL,回流2 h,抽滤,挥去甲醇,得残渣,加蒸馏水10 mL,转移至分液漏斗,用10%稀硫酸调pH至2,乙醚萃取,取乙醚层,挥去乙醚,加甲醇1~2 mL,得复方制剂供试品溶液。同法制取阴性对照溶液。精密称取当归对照药材0.05 g,加甲醇20 mL,超声提取30 min,过滤,挥去甲醇,得残渣,加蒸馏水10 mL,转移至分液漏斗,用 10%稀硫酸调 pH 至 2,乙醚萃取 2次(每次10 mL),取乙醚层,挥去乙醚,加甲醇1~2 mL,得当归对照药材供试品溶液。按照TLC法(中国药典 2015年版,四部通则 0502),吸取阿魏酸对照品溶液5.0 μL,其余3种溶液10.0 μL,点样,以环己烷-二氯甲烷-乙酸乙酯-甲酸(12∶3∶9∶0.4)为展开剂,展开,晾干,置于紫外光灯365 nm下检视。在与阿魏酸对照品、当归对照药材色谱相应的位置上,复方制剂供试品色谱显相同颜色的斑点,且阴性对照色谱中无干扰,结果见图1。
2.1.2 赤芍的 TLC鉴别[3-5]精密称取制剂10 g,加甲醇40 mL,回流2 h,抽滤,水浴挥至1~2 mL,得复方制剂供试品溶液。同法制取剂阴性对照溶液。精密称取赤芍对照药材0.05 g,加甲醇20 mL,超声提取30 min,抽滤,滤液挥至1~2 mL,得对照药材供试品溶液。按照 TLC法(中国药典 2015年版,四部通则 0502),吸取芍药苷对照品溶液5.0 μL,其余 3种溶液 10.0 μL,点样,以氯仿-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)展开,晾干,5%香草醛-浓硫酸乙醇溶液显色,加热烘至斑点清晰,取出。在与芍药苷对照品、赤芍对照药材色谱相应的位置上,复方制剂供试品色谱显相同颜色的斑点,且阴性对照色谱中无干扰,结果见图2。

图1 当归的TLC色谱图
1~3-复方制剂;4-阿魏酸;5-当归对照药材;6-阴性对照。
Fig. 1 TLC graph of Angelicae Sinensis Radix
1~3-compound preparation; 4-ferulic acid; 5-reference of Angelicae Sinensis Radix; 6-negative sample.
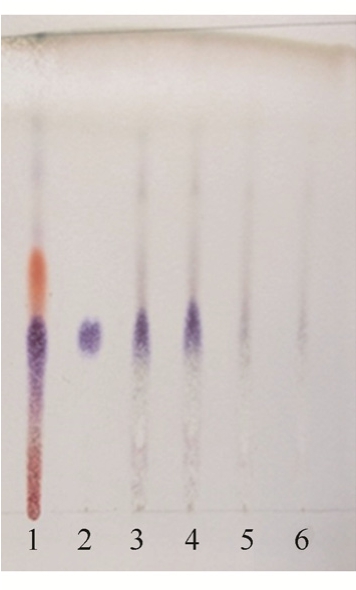
图2 赤芍的TLC色谱图
1-赤芍对照药材;2-芍药苷;3~4-复方制剂;5~6-阴性对照。
Fig. 2 TLC graph of Paeoniae Radix Rubra
1-reference Paeoniae Radix Rubra; 2-paeoniflorin; 3-4-compound preparation; 5-6-negative sample.
2.1.3 延胡索的TLC鉴别[6]精密称取制剂10 g,加甲醇40 mL,回流2 h,抽滤,挥去甲醇,得残渣,加蒸馏水10 mL,转移至分液漏斗,用浓氨水调pH至9,正己烷萃取,取正己烷层,挥去正己烷,加甲醇1~2 mL,得复方制剂供试品溶液。同法制取剂阴性对照溶液。精密称取延胡索对照药材0.05 g,加甲醇20 mL,超声提取30 min,过滤,挥去甲醇,得残渣,同复方制剂供试品溶液的制备。按照TLC法(中国药典2015年版,四部通则0502),吸取上述对照品溶液5.0 μL,其余3种溶液 10.0 μL,点样。先以正己烷-氯仿-甲醇(15∶8∶0.6)为展开剂一次展开,溶剂前沿约12 cm,取出,晾干;再以环己烷-丙酮为展开剂(14∶6)二次展开,取出,晾干;用碘单质显色,365 nm紫外灯下检视。在与延胡索乙素对照品、延胡索对照药材色谱相应的位置上,复方制剂供试品色谱显相同颜色的斑点,且制剂阴性对照色谱中无干扰,结果见图3。
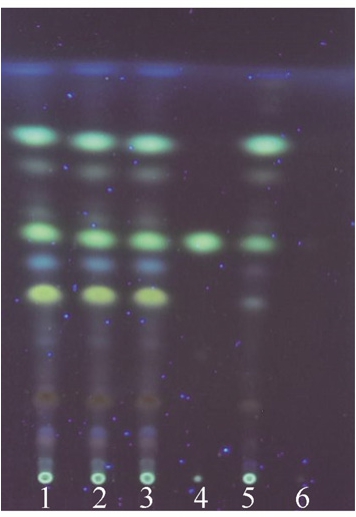
图3 延胡索的TLC色谱图
1~3-复方制剂;4-延胡索乙素对照品;5-延胡索对照药材;6-阴性对照。
Fig. 3 TLC graph of Corydalis Rhizoma
1-3-compound preparation; 4-tetrahydropalmatine; 5-reference Corydalis Rhizoma; 6-negative sample.
2.2.1 色谱条件 色谱柱 Extend-C18(4.6 mm×250 mm,5 μm);流动相:乙腈-0.1%磷酸(15∶85);柱温:25 ℃;DAD检测器;检测波长:阿魏酸320 nm,芍药苷234 nm;流速:1 mL·min-1;进样量:10 μL。
2.2.2 溶液的制备 ①对照品溶液的制备:精密称取阿魏酸对照品 0.04 mg,芍药苷对照品0.27 mg,至5 mL量瓶中,以甲醇溶解,配制成阿魏酸浓度为 0.008 mg·mL-1,芍药苷浓度为0.054 mg·mL-1的混合对照品溶液,放入冰箱贮存,备用。②供试品溶液的制备:精密称取样品制剂约1 g,置25 mL量瓶中,加入甲醇定容至刻度,超声提取 10 min,作为供试品溶液。③阴性供试品溶液的制备:分别称取缺少当归、赤芍的阴性制剂,按照②方法制备阴性供试品溶液。
2.2.3 系统适用性试验 分别精密吸取对照品、供试品和阴性供试品溶液各10 μL,按“2.2.1”项下色谱条件进样。理论板数按芍药苷峰计算≥5 000。样品色谱图中,在与对照品色谱图相应保留时间有相同色谱峰,阴性样品无干扰,见图4。
精密称取阿魏酸对照品 2.98 mg,定容至50 mL;精密称取芍药苷对照品5.69 mg,定容至25 mL。精密吸取阿魏酸、芍药苷对照品溶液,配制成阿魏酸浓度为 0.002 4,0.004 8,0.007 2,0.009 5,0.011 9 mg·mL-1,芍药苷浓度为 0.036 4,0.045 5,0.054 6,0.063 7,0.072 8,0.081 9 mg·mL-1的混合对照品溶液,按“2.2.1”项下色谱条件进样 10 μL,记录色谱峰面积。以浓度(mg·mL-1)为横坐标,峰面积为纵坐标,绘制标准曲线。阿魏酸的回归方程为:Y=31 662X-19.715(r=0.999 4),芍药苷的回归方程为:Y=11 142X-15.736(r=0.999 2),表明阿魏酸在 0.002 4~0.011 9 mg·mL-1,芍药苷在0.036 4~0.081 9 mg·mL-1内线性关系良好。

图4 高效液相色谱图
A-对照品;B-样品;C-阴性对照;1-阿魏酸;2-芍药苷。
Fig. 4 HPLC chromatograms
A-reference substance; B-sample; 1-ferulic acid; 2-paeoniflorin.
取同一供试品溶液,连续进样6次,阿魏酸、芍药苷的RSD分别为2.23%(n=6),1.56%(n=6),结果表明仪器精密度良好。
取同一供试品溶液,室温下静置,分别于0,2,4,8,12,24 h,按“2.2.1”项下色谱条件测定,阿魏酸、芍药苷的RSD分别为1.83%(n=6),1.74%(n=6),结果表明供试品溶液在24 h内稳定。
取同一批样品 6份,按“2.2.2”项下供试品溶液制备的方法平行制备供试品溶液 6份,按“2.2.1”项下色谱条件测定,计算阿魏酸、芍药苷的RSD分别为1.58%(n=6),0.81%(n=6),结果表明本方法重复性良好。
精密称取已知含量的同一批样品 9份,分别按样品含量的 50%,100%,150%(低、中、高)3个浓度加入浓度为0.073 2 mg·mL-1的阿魏酸对照品溶液0.4,0.8,1.2 mL,浓度为0.135 8 mg·mL-1的芍药苷对照品溶液2.7,5.4,8.1 mL,各3份分别加甲醇溶解定容至25 mL量瓶,按照“2.2.2”②项下方法制备,按“2.2.1”项色谱条件测定,结果见表1。
表1 加样回收实验结果(n=6)
Tab. 1 Results of recovery tests (n=6)
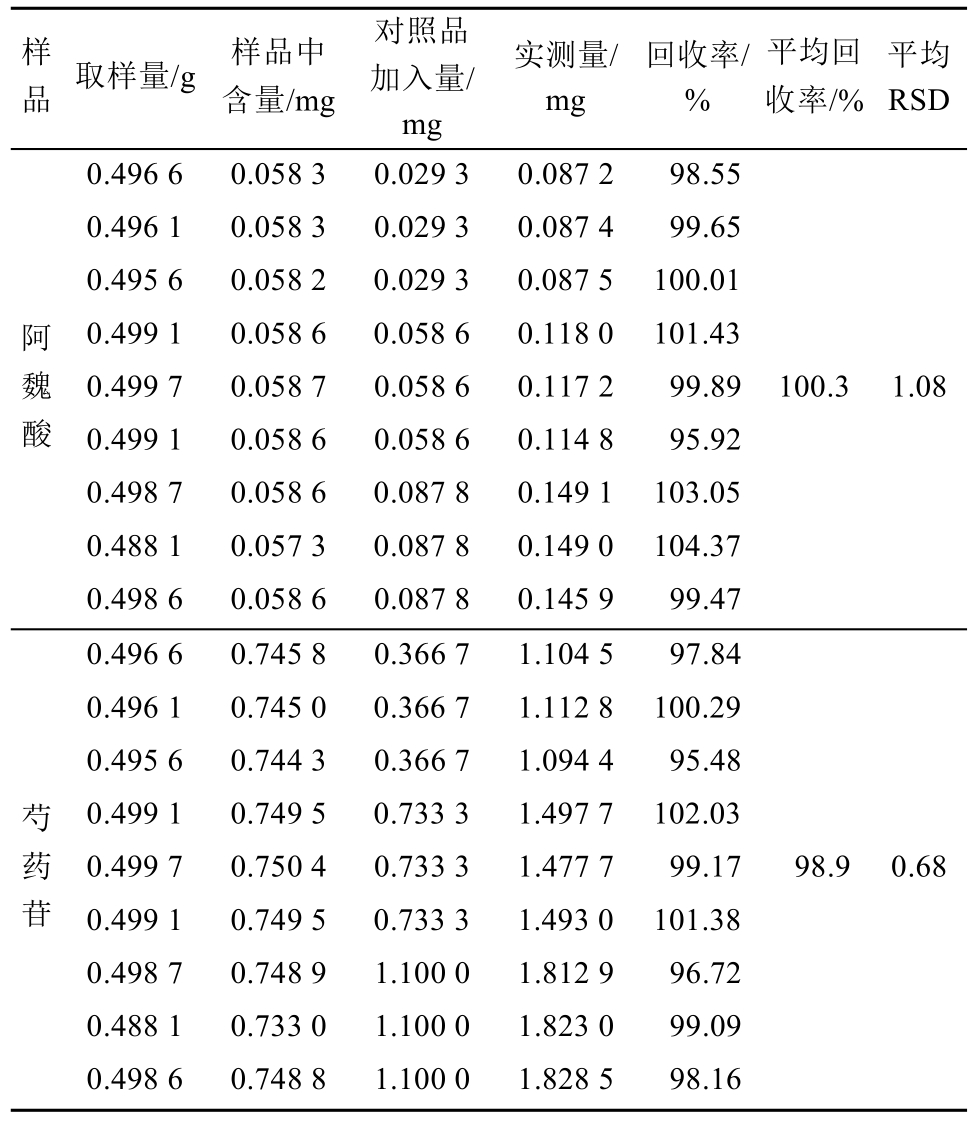
取 3批样品,平行取样 3份,按“2.2.2”②项下方法制备供试品溶液,按“2.2.1”项下色谱条件测定,记录色谱峰面积,按外标法计算样品中阿魏酸、芍药苷的含量,结果185 g生药所制备的 92.5 g制剂中含阿魏酸含量为 0.122 2 mg·g-1,RSD=1.38%;芍药苷为1.487 1 mg·g-1,RSD=0.76%。
复方当归妇炎微灌肠剂为复方制剂,方剂组成的药味多,分离难,干扰大,质量标准建立难。本实验对方中多味药进行了鉴别,最后根据药材的主要成分和新药审批标准选择君药当归、赤芍、延胡索定性鉴别。该鉴别方法专属性强,且阴性对照无干扰,可作为该制剂专属鉴别,以更好地控制产品质量。
根据中国药典2015年版阿魏酸检测波长选定为320 nm。采用芍药苷的最大吸收波长(230 nm)时,其杂质的吸收过大,影响了芍药苷的峰型,通过对其3D图谱观察,在234 nm的波长下,其对芍药苷的吸收影响不大,但对杂质的吸收减弱。因此,本实验结合药典、文献选择芍药苷的检测波长为234 nm[5,7-8]。
在流动相的选择上,根据阿魏酸和芍药苷的化学性质,本实验首先采用甲醇-0.085%磷酸(15∶85)洗脱,分离效果及峰型欠佳;更换为乙腈-0.1%磷酸梯度洗脱,出现较大基线漂移;故将流动相再次更换为乙腈-0.1%磷酸(15∶85)等度洗脱[5,8-9]。结果表明,此流动相对2种成分进行测定的分离效果和对称性都很好,且该制剂其他组分没有影响。本实验为建立复方当归妇炎微灌肠剂质量控制标准提供了理论依据。
[1] ZHAO P X, WANG Y Z, YU X H. Clinical observation of 100 cases of pelvic inflammatory disease treated by Compound Angelica Fuyan Enema [J]. Clin J Chin Med(中医临床研究),2015, 7(6): 67-69.
[2] 谢仲德, 方应权, 李文烈, 等. 当归调经胶囊的薄层鉴别与阿魏酸、芍药苷的测定[J]. 中成药, 2013, 35(2): 427-430.
[3] LU J X, TAN C M, CHEN B L, et al. Improvement of the quality control standard for Mingmu Shangqing pills [J]. Chin J Pharm Anal(药物分析杂志), 2016, 36(11): 2051-2058.
[4] YANG F. Study on TLC identification and general methods of Yuanhuzhitong series varieties [J]. Chongqing J Res Chin Drug Herb(重庆中草药研究), 2014(1): 7-9.
[5] LIU Y Q, MA Y, YANG B W, et al. Determination of bioactive components in paeonia lactiflora roots cultivated in various areas by UHPLC [J]. J Chin Med Mater(中药材), 2016,39(5): 980-985.
[6] YANG M, LI C, FENG W H, et al. Simultaneous determination of eleven major alkaloids in Corydalis Rhizoma by RP-HPLC [J]. Chin J Exp Tradit Med Form(中国实验方剂学杂志), 2016, 22(6): 22-25.
[7] HE L L. Determination of perlic acid in Angelica Nourishing pills by HPLC [J]. Chin Med Her(中国医药导报), 2011, 8(3):60-62.
[8] 中国药典. 一部[S]. 2015: 80-81.
[9] CHEN Y H. Fast determination of Aifu Nuangong pills by HPLC [J]. Strait Pharm J(海峡药学), 2014, 26(12): 55-57.
Study of Quality Control on Compound Angelica Fuyan Micro Enema
YU Xiaohui1,2, FAN Qin1,2, ZHAO Lei1,2, WANG Yonggang1, YANG Ruijing1, SONG Jiaojiao1
(1.Gansu University of Chinese Medicine, Lanzhou 730000, China; 2.Provincial Key Laboratory of Chinese (Tibetan) Medicine Chemistry and Quality in Universities in Gansu Province, Lanzhou 730000, China)
ABSTRACT:OBJECTIVE To establish a method of quality control for Compound Angelica Fuyan Micro Enema.METHODS According to the composition of prescription, the qualitative identification of Angelicac Sinensis Radix, Paeoniae Radix Rubra and Corydalis Rhizoma in Compound Angelica Fuyan Micro Enema was performed by TLC. The content of ferulic acid and paeoniflorin in Compound Angelica Fuyan Micro Enema was determined by HPLC: using Extend-C18(4.6 mm×250 mm, 5 μm) column; acetonitrile-0.1% phosphoric acid (15∶85) was as the flow equality. Column temperature was 25 ; ℃flow velocity 1 mL·min-1; the detection wavelength was 320, 234 nm. RESULTS Ferulic acid and paeoniflorin had good linear relationship within 0.002 4-0.011 9 mg·mL-1(r=0.999 4), 0.036 4-0.081 9 mg·mL-1(r=0.999 2). The average recovery rate was 100.3%, 98.9% and the RSD was 1.08%, 0.68% respectively. CONCLUSION The established method is simple, accurate and stable well, and can be used for the quality control of the preparation.
KEY WORDS:micro enema; qualitative standard; Angelicac Sinensis Radix; Paeoniae Radix Rubra; Corydalis Rhizoma
REFERENCES
中图分类号:R284.1
文献标志码:B
文章编号:1007-7693(2017)12-1703-04
DOI:10.13748/j.cnki.issn1007-7693.2017.12.013
引用本文:余晓晖, 樊秦, 赵磊, 等. 复方当归妇炎微灌肠剂质量控制研究[J]. 中国现代应用药学, 2017, 34(12): 1703-1706.
基金项目:2014年兰州市科技局重点项目(2014-1-145);2015年甘肃省高校中(藏)中药药理与毒理研究省级重点实验室开放基金项目(ZDSYS-KJ-2015-006)
作者简介:余晓晖,女,正高级工程师 Tel: (0931)8765394 E-mail: yxhg123@sina.com
收稿日期:2017-06-28
(本文责编:李艳芳)