益生菌四联对比铋剂四联疗法补救根除幽门螺杆菌感染的Meta分析
周本刚1,冯秋曲1,李仕宇2,张海1,王宏志1*
[鄂东医疗集团黄石市中心医院(湖北理工学院附属医院)消化内科,湖北 黄石 435000;2.遵义市第一人民医院(遵义医学院第三附属医院)消化内科,贵州 遵义 563000]
摘要:目的 系统评价益生菌四联疗法(PQT)对比铋剂四联疗法(BQT)补救根除幽门螺杆菌(Helicobacter pylori,Hp)感染的疗效和安全性。方法 检索关于PQT对比BQT补救根除Hp感染的临床试验,检索时限均为建库至2016年10月。由2名评价员,根据纳入与排除标准筛选文献、提取资料,依据改良Jadad量表评价纳入研究的方法学质量,采用RevMan 5.3软件进行meta分析。结果 最终纳入9个临床试验,共875例患者,结果显示:补救治疗中PQT的Hp根除率高于BQT,但差异无统计学意义(RR=1.03,95%CI:0.97~1.10,P=0.36);按PP分析,PQT与BQT的Hp根除率相当,但差异无统计学意义(RR=1.00,95%CI:0.94~1.07,P=0.90)。PQT的不良反应发生率明显低于 BQT,且差异有统计学意义(RR=0.31,95%CI:0.23~0.41,p<0.000 01)。结论 与BQT相比,补救治疗中PQT的不良反应发生率更低,但Hp的根除率无差异,该结论有待大样本高质量的研究验证。
关键词:幽门螺杆菌;益生菌;铋剂;Meta分析;系统评价
幽门螺杆菌(Helicobacter pylori,Hp)感染是十分普遍的公共卫生问题,全球Hp感染率约为50%,某些发展中国家高达 80%~90%,我国成人中 Hp感染率高达40%~60%[1-2]。目前研究认为,Hp感染与许多消化系统疾病及非消化系统疾病相关[3],因此根除 Hp临床意义重大。2015年发表的《幽门螺杆菌胃炎京都全球共识报告》[4]将Hp胃炎定义为一种感染性疾病,对Hp的根除提出了更高的要求。然而,近年来随着抗菌药物的广泛使用,Hp耐药性不断提高,Hp根除失败是临床医师必须面对的难题。Hp首次根除失败后,其再次根除失败的可能性较大[2,5],故补救根除方案的选择尤为重要。铋剂四联疗法、左氧氟沙星三联疗法、伴同疗法等是目前临床上推荐的补救治疗方案[5],然而均有不同程度的胃肠道反应导致根除治疗失败,因此探究新的补救治疗方案成为研究热点。近年来诸多研究发现益生菌具有抑制 Hp生长的作用,而且能降低根除治疗过程的不良反应[6]。目前已有多项益生菌联合三联疗法对比铋剂四联疗法补救治疗 Hp感染的临床试验,但结果仍有争议。为此,本研究对上述 2种方案的临床试验进行meta分析,为临床实践提供循证医学依据。
1 研究方法
1.1 检索策略
计算机检索 PubMed、Embase、the Cochrane library(2016年第 10期)、中国生物医学文献数据库(CBM)、中国知网(CNKI)、万方数据库(Wanfang)、维普(VIP)数据库,收集关于益生菌联合三联疗法对比铋剂四联疗法补救治疗 Hp感染的随机对照试验。中文检索词:幽门螺杆菌、有益菌种、益生菌、乳酸菌、乳球菌、双歧杆菌、酵母菌、酪酸菌、芽孢杆菌、微生态制剂、铋;英文检索词:Helicobacter pylori、H.pylori、Hp、Campylobacter pyloridis、probiotics、probiotic、lactobacillus、lactococcus、bifidobacterium、yeast、yogurt、saccharomyces、streptococcus、enterococcus、Bacillus subtilis、 Bacillus clausii、 clostridium butyrium、bismuth。此外,追溯已纳入文献和相关综述的参考文献,检索时间均从建库至2016年10月,无语种限制。
1.2 纳入标准与排除标准
纳入标准:①研究设计类型:随机对照试验或临床对照试验。②研究对象:所有受试者均为经常规疗法初次或多次治疗后 Hp仍阳性者;Hp感染需经以下任意一种方法证实:尿素呼气试验、快速尿素酶试验、组织学检测或 Hp粪便抗原检测。③干预措施:试验组益生菌+三联疗法;对照组铋剂+三联疗法;三联疗法为PPI+2种抗菌药物;试验组与对照组的标准三联方案组成及用法完全一致。④结局指标:按意向治疗(intention-to-treat,ITT)分析的Hp根除率;符合方案集(per protocol,PP)分析的Hp根除率;Hp根除标准:至少停药4周采用公认的Hp检测方法复查,阴性为Hp根除;不良反应(恶心、呕吐、腹泻、腹胀等)的发生率。⑤排除标准:综述、会议摘要、重复发表文献;研究对象为Hp感染初次治疗的患者。
1.3 文献筛选、资料提取
由 2名评价员分别独立进行文献筛选及资料提取,对部分多臂试验的随机对照试验,只提取符合干预措施的数据,数据提取完成后进行交叉核对,有争议时通过与第三方讨论解决。资料提取主要包括:第一作者姓名、发表时间及研究地区、研究对象的基线资料,试验组与对照组的具体细节、结局指标及质量评价的关键要素等。
1.4 文献质量评价
采用改良 Jadad量表对纳入文献进行质量评价,评分标准包括以下 4项:①随机化序列的产生(0~2 分);②分配隐藏(0~2 分);③盲法(0~2 分);④撤出或失访(0~1分)。前3项评分方法如下:采用方法“恰当”评为2分,“不清楚”评为1分;“不恰当”评为0分;“撤出或失访”描述评为1分,未描述评为0分,分值为0~7分。质量评价由 2名评价员独立进行,如有争议通过讨论或咨询第三方解决,总分≤3分为低质量文献[7]。
1.5 统计分析
采用RevMan 5.3软件进行meta分析。本研究的结局指标为二分类变量,采用相对危险度(RR)及其95%CI为效应指标。异质性检验采用χ2检验(检验水准为 α=0.1)及 I2,各研究间无统计学异质性(I2≤50%,P≥0.1),采用固定效应模型(FEM)进行分析;如异质性检验结果显示各研究间存在统计学异质性(I2>50%,p<0.1),若无明显的临床异质性,采用随机效应模型(REM)进行合并分析。采用敏感性分析检测结果的稳定性,运用RevMan 5.3倒漏斗图检测发表偏倚。
2 研究结果
2.1 文献检索及筛选结果
共检索到文献327篇(中文197篇,英文130篇),运用软件EndNoteX7去重后剩余151篇,依次阅读题目、摘要、全文进行筛选,剔除不符合纳入与排除标准的文献142篇,最终纳入9个临床试验[8-16],均为中文文献。
2.2 纳入研究基本特征与文献质量评价
本研究共纳入2011—2016年间我国6个省份和2个直辖市的9个临床试验(共875例患者),其中试验组439例,对照组436例。研究对象均为成人,各研究均报告基线具有可比性。各研究所用的益生菌不尽一致,有2个研究[8-9]使用乐托尔(乳酸菌LB散),1个研究[10]使用复方嗜酸乳杆菌,1个研究[14]使用培菲康,5个研究[11-13,15-16]使用金双歧。采用改良Jadad量表对其进行质量评价,有7个研究[8-13,15]提及“随机”字样,但2个研究[13,15]提及“计算机随机”方法;1个研究[14]按“药物治疗不同”分组,1个研究[16]按“入院顺序”分组;有6个研究[8-9,12-15]描述了具体的失访/退出情况;有1个研究[9]为开放试验,其余所有研究的盲法均未作描述。基本特征及质量评价评分见表1。
2.3 Meta分析结果
2.3.1 按ITT分析Hp的根除率 纳入的 9个研究[8-16]均报告了Hp的根除率,按ITT分析处理数据,研究结果间无统计学异质性(I2=0%,P=0.82),采用FEM进行meta分析,益生菌四联组的Hp根除率高于铋剂四联组,但差异无统计学意义(RR=1.03,95%CI:0.97~1.10,P=0.36),结果见图 1。
2.3.2 按PP分析Hp的根除率 试验组7例,对照组18例在研究中失访或退出。按PP分析处理数据,研究结果间无统计学异质性(I2=0%,P=0.99),采用FEM进行meta分析,益生菌四联组与铋剂四联组的Hp根除率相当,差异无统计学意义(RR=1.00,95%CI:0.94~1.07,P=0.90),结果见图2。
2.3.3 不良反应发生率 纳入的 9个研究均对服药后的不良反应进行了报告,纳入研究间无统计学异质性(I2=0,P=0.49),采用FEM进行meta分析,结果显示益生菌四联组的不良反应发生率明显低于铋剂四联组,且差异有统计学意义(RR=0.31,95%CI:0.23~0.41,P<0.000 01),结果见图3。
2.3.4 敏感性分析与发表偏倚 对于 Hp的根除率及不良反应的发生率,采用逐一剔除单项研究合并剩下研究的方法进行敏感性分析,结果均显示无明显改变,表明其结果较为稳健。采用RevMan 5.3绘制倒漏斗图,漏斗图基本对称,提示无明显发表偏倚。结果见图4。
表1 纳入研究基本特征
Tab. 1 Basic characteristic of included studies
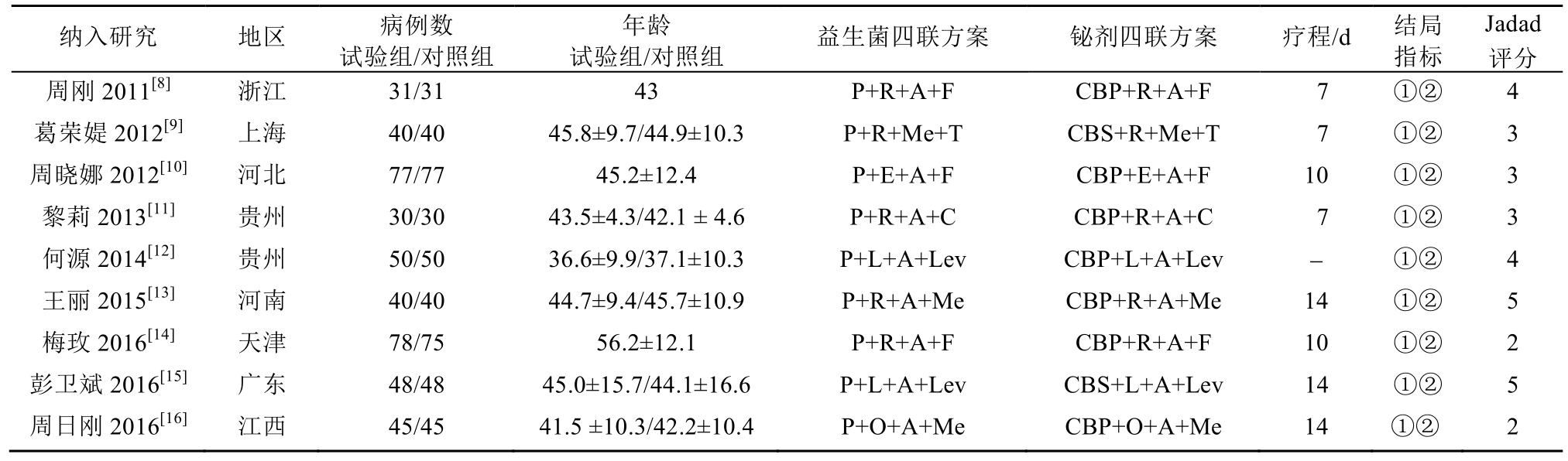
注:P-益生菌;R-雷贝拉唑;L-兰索拉唑;E-埃索美拉唑;O-奥美拉唑;CBP-胶体果胶铋;CBS-胶体次枸橼酸铋;A-阿莫西林;C-克拉霉素;F-呋喃唑酮;Me-甲硝唑;T-四环素;Lev-左氧氟沙星;①Hp的根除率;②不良反应的发生率。
Note: P-probiotics; R-rabeprazole; L-lansoprazole; E-esomeprazole; O-omeprazole; CBP-colloidal bismuth pectin; CBS-collodial bismuth subcitrate;A-amoxicillin; C-clarithromycin; F-furazolidone; Me-metronidazole; T-tetracycline; Lev-levofloxacin; ①-the eradication rate of Hp; ②-incidence of adverse reactions.
纳入研究 地区 病例数试验组/对照组 试验组/对照组 益生菌四联方案 铋剂四联方案 疗程/d 结局指标年龄Jadad评分周刚2011[8]浙江 31/31 43 P+R+A+F CBP+R+A+F 7 ①② 4葛荣媞2012[9]上海 40/40 45.8±9.7/44.9±10.3 P+R+Me+T CBS+R+Me+T 7 ①② 3周晓娜2012[10]河北 77/77 45.2±12.4 P+E+A+F CBP+E+A+F 10 ①② 3黎莉2013[11]贵州 30/30 43.5±4.3/42.1 ± 4.6 P+R+A+C CBP+R+A+C 7 ①② 3何源2014[12]贵州 50/50 36.6±9.9/37.1±10.3 P+L+A+Lev CBP+L+A+Lev - ①② 4王丽2015[13]河南 40/40 44.7±9.4/45.7±10.9 P+R+A+Me CBP+R+A+Me 14 ①② 5梅玫2016[14]天津 78/75 56.2±12.1 P+R+A+F CBP+R+A+F 10 ①② 2彭卫斌2016[15]广东 48/48 45.0±15.7/44.1±16.6 P+L+A+Lev CBS+L+A+Lev 14 ①② 5周日刚2016[16]江西 45/45 41.5 ±10.3/42.2±10.4 P+O+A+Me CBP+O+A+Me 14 ①② 2
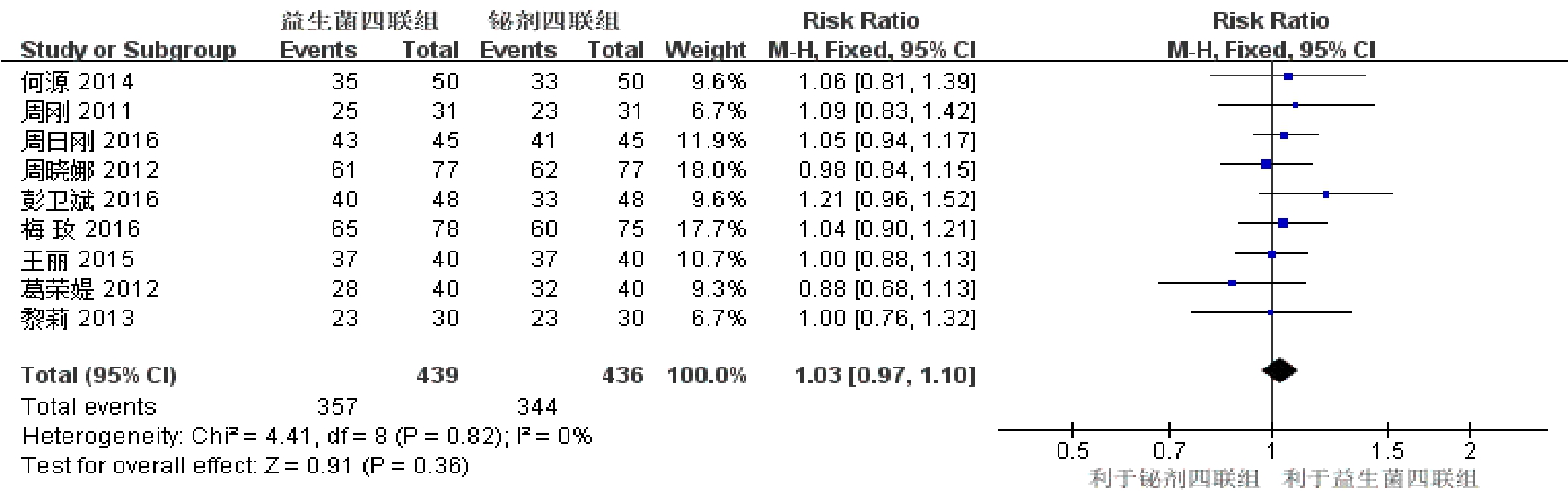
图1 补救治疗中试验组及对照组Hp根除率比较的森林图(ITT分析)
Fig. 1 Forest plot for comparison of the eradication rate of Hp between the experimental group and the control group in rescue regimen(ITT analysis)
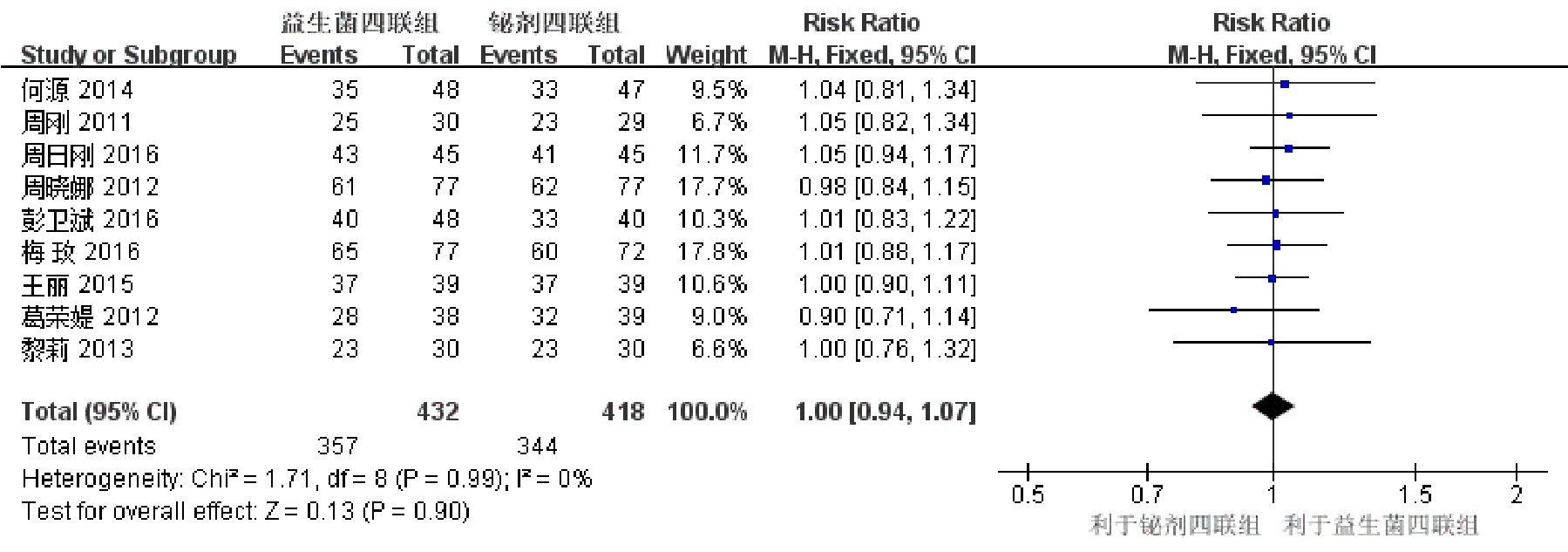
图2 补救治疗中试验组及对照组 Hp 根除率比较的森林图(PP分析)
Fig. 2 Forest plot for comparison of the eradication rate of Hp between the experimental group and the control group in rescue regimen (PP analysis)
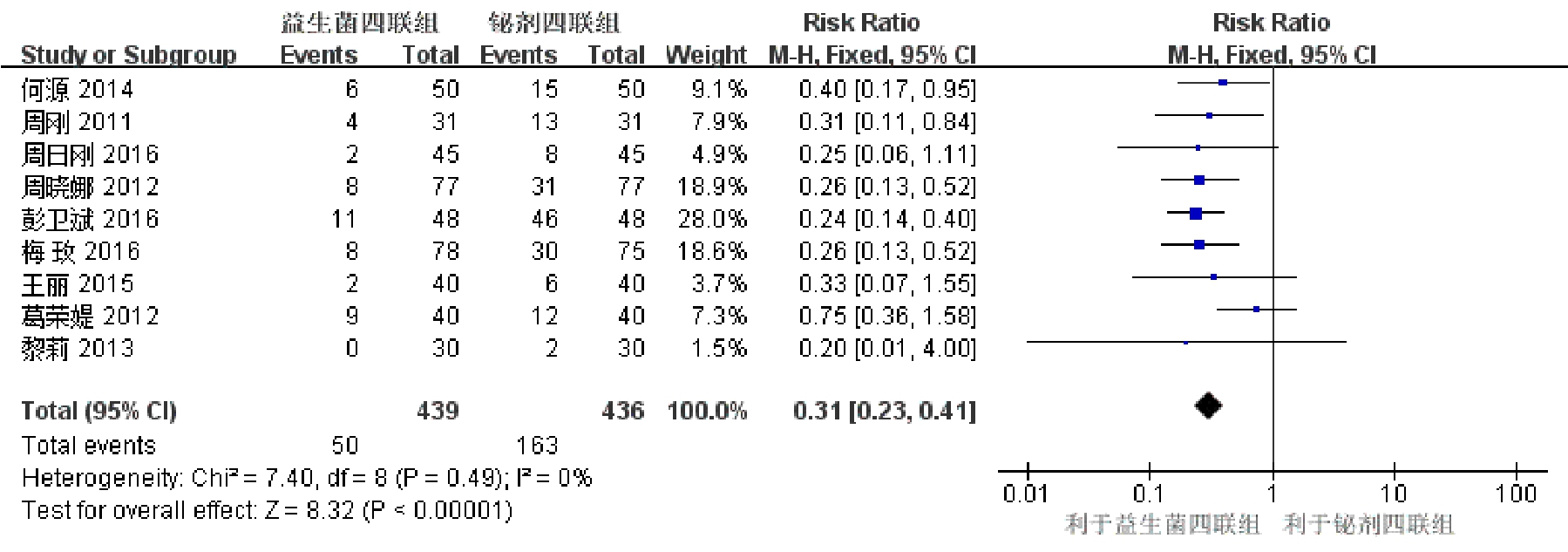
图3 补救治疗中试验组及对照组不良反应发生率比较的森林图
Fig. 3 Forest plot for comparison of the incidence rates of adverse reactions between the experimental group and the control group in rescue regimen

图4 Hp根除率和不良反应发生率的漏斗图
Fig. 4 Funnel plot based on Hp eradication rate and the incidence rates of adverse reactions
3 讨论
3.1 纳入文献质量分析
本研究纳入9个临床试验,有5个研究质量≤3分(低质量文献),平均分为3.4分,纳入研究整体质量不高,文献普遍存在随机序列产生、分配隐藏及盲法未作具体描述等问题,在一定程度上降低了结果的可靠性。因此,建议未来的研究应严格规范设计,鼓励进行注册,试验实施时采用严格的质量控制,论文报告时采用随机对照试验报告标准规范(CONSORT 2010),从而保证试验的透明化和质量的提升,以便于得出更高质量的证据。
3.2 益生菌四联疗法补救根除Hp的疗效分析
本研究纳入我国2011—2016年间9个临床试验共875例患者,meta分析结果显示,不论按ITT分析还是按PP分析,补救疗法中益生菌四联疗法与铋剂四联疗法的Hp根除率均无统计学意义,表明2组疗法的Hp根除率相当。然而在不良反应发生率上,益生菌四联组的不良反应发生率明显低于铋剂四联组,提示益生菌联合三联疗法可明显降低抗菌药物相关性不良反应的发生。益生菌菌株种类繁多,可分为乳酸菌属、双歧杆菌属、酵母菌属、梭菌属等[17],本研究纳入的文献中益生菌主要以乳酸杆菌、双歧杆菌与乳酸杆菌的混合制剂为主。乳酸杆菌是目前临床和动物试验最常用的益生菌,其抗 Hp的机制可能通过产生抑制Hp生长的物质,抑制Hp的定植,抑制Smad7、核转录因子κB(NF-κB)通路活化,调节免疫反应,从而减弱Hp引起的胃黏膜炎症反应[6]。双歧杆菌也是人体胃肠道正常菌群的一部分,且更为安全,主要通过抑制 Hp的活性、抑制 Hp刺激产生的IL-8,从而抑制炎症反应[18]。此外,益生菌可平衡常规根除方案所致的肠道菌群紊乱,降低抗菌药物的不良反应,从而提高患者的依从性[19],可间接提高Hp的根除率。
3.3 本研究的局限性
本研究采用逐一剔除单项研究合并剩下的研究的方法进行敏感性分析,结果无明显改变,且发表偏倚检测提示无明显发表偏倚,说明本研究结果较为稳健、可靠。然而本研究存在一定局限性:①原始研究质量普遍低下,降低了结果的可靠性;②纳入研究在药物种类、剂量、疗程及先前的Hp根除方案等方面存在一定的差异,可能会影响结果的真实性;③纳入人群均为国内人群,因地区、种族的差异,结论不一定适用于其他人群。
3.4 结论与展望
当前证据显示,补救治疗中,益生菌四联疗法与铋剂四联疗法相比,Hp根除率相当,但益生菌四联疗法不良反应发生率更低。由于Hp首次根除失败后再次根除,其失败的可能性较大,且抗Hp的抗菌药物选择有限,部分患者对铋剂不能耐受或有禁忌,因此益生菌四联疗法可作为铋剂四联疗法补救根除Hp感染一种补充。但由于纳入研究的数量有限,质量不高,同时,益生菌抗Hp的作用机制尚未完全阐明,益生菌的菌株选择、剂量、添加时机等诸多问题尚未达成共识,因此临床医师应谨慎使用。未来需进一步开展大样本、高质量的研究来验证益生菌四联疗法补救根除Hp感染的有效性及安全性。
[1] 牛占岳, 宋志强, 周丽雅. 中国大陆地区成人幽门螺杆菌耐药情况及变迁[J]. 中华内科杂志, 2016, 55(9): 734-736.
[2] 刘文忠, 谢勇, 成虹, 等. 第四次全国幽门螺杆菌感染处理共识报告[J]. 中华内科杂志, 2012, 51(10): 832-837.
[3] MALFERTHEINER P, MEGRAUD F, O'MORAIN C A, et al.European Helicobacter and Microbiota Study Group and Consensus panel. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report [J]. Gut,2017, 66(1): 6-30.
[4] SUGANO K, TACK J, KUIPERS E J, et al. Kyoto global consensus reporton Helicobacter pylori gastritis [J]. Gut, 2015,64(9): 1353-1367.
[5] LIU W Z, XIAO S D. Interpretation of new international consensuses on Helicobacter pylori [J]. Chin J Gastroenterol(胃肠病学), 2012, 17(1): 1-4.
[6] HOMAN M, OREL R. Are probiotics useful in Helicobacter pylori eradication [J]. World J Gastroenterol, 2015, 21(37):10644-10653.
[7] LI S, DING B J, YANG Y, et al. Meta-analysis: the effect of probiotics supplement on standard triple therapy for Helicobacter pylori eradication [J]. Chin J Microecol(中国微生态学杂志), 2012, 24(4): 334-338.
[8] ZHOU G, LI Z Y, WANG Z L, et al. Effect of quadruple therapy containing microecologics on Helicobacter pylori infection after first treatment failure in 31 cases [J]. China Pharm(中国药业), 2011, 20(9): 58-59.
[9] GE R T. Rabeprazole-based quadruple therapy as the rescue regimen after failure to Helicobacter pylori eradication [D].Shanghai: Shanghai JiaoTong University, 2012: 4-16.
[10] ZHOU X N, CHANG L L, WU Y M. Effect of probiotics with triple therapy on Helicobacter pylori eradication [J]. Chin J Clin Ration Drug Use(临床合理用药), 2012, 5(3B): 15-16.
[11] LI L, YANG W W, YANG J L, et al. Radical curative efficacy of quadruple therapy containing probiotics on persistent Helicobacter pylori infection: an efficacy observation [J]. Chin J Microecol(中国微生态学杂志), 2013, 25(6): 673-675.
[12] 何源, 尘坚, 李岚, 等. 双歧杆菌乳杆菌三联活菌片在幽门螺杆菌根除失败后补救疗法中的观察[J]. 医药前沿,2014(34): 180-181.
[13] WANG L. Pharmacological analysis of intestinal probiotics and medication safety investigation in adjuvant treatment of intractable Hp infection [J]. Chin J Mod Drug Appl(中国现代药物应用), 2015, 9(2): 1-3.
[14] 梅玫, 陆伟, 罗雁, 等. 培菲康联合补救三联方案对复治幽门螺杆菌的临床观察[J]. 吉林医学, 2016, 37(9): 2257-2258.
[15] PENG W B, RONG H Y, SHA W H, et al. Efficacy of levofloxacin-based triple therapy combined with probiotics as a rescue therapy for Helicobacter pylori re-eradication [J].Chin J Gastroenterol(胃肠病学), 2016, 21(4): 211-214.
[16] 周日刚. 肠道微生态制剂的药理作用与辅助治疗顽固性幽门螺杆菌感染的用药安全性分析[J]. 临床合理用药, 2016,9(8C): 62-63.
[17] GUARNER F, KHAN A G, GARISCH J, et al. World Gastroenterology Organisation Global Guidelines: probiotics and prebiotics October 2011 [J]. J Clin Gastroenterol, 2012,46(6): 468-481.
[18] 曾冉冉, 吴丽丽, 张晓梅, 等. 微生态制剂对幽门螺杆菌感染的治疗作用[J]. 中华医学杂志, 2015, 95(16): 1266-1267.
[19] CHEN Y H, WANG C L, XIE Y. Progress of research into the pathogenic mechanism of Helicobacter pylori and the preventive role of probiotics in H. pylori infection [J]. World Chin J Digestol(世 界 华 人 消 化 杂 志 ), 2007, 15(25):2690-2697.
Probiotics-containing Quadruple Therapy Versus Bismuth Quadruple Therapy as a Rescue Regimen for the Eradication of Helicobacter Pylori Infection: A Meta-analysis
ZHOU Bengang1, FENG Qiuqu1, LI Shiyu2, ZHANG Hai1, WANG Hongzhi1*
(1.Department of Gastroenterology,Huangshi Central Hospital of Edong Healthcare Group, Affiliated Hospital of Hubei Polytechnic University, Huangshi 435000,China; 2.Department of Gastroenterology, The First People’s Hospital of Zunyi, The Third Affiliated Hospital of Zunyi Medical College, Zunyi 563000, China)
ABSTRACT:OBJECTIVE To systematically review the efficacy and safety of probiotics containing quadruple therapy(PQT)as a rescue regimen for the eradication of Helicobacter pylori (Hp) infection. METHODS To search clinical trials about PQT versus bismuth quadruple therapy(BQT) as a rescue regimen for the eradication of Hp infection from inception to October 2016.Two reviewers independently screened literature, extracted data, and assessed the methodological quality of included studies by revised Jadad scale. The meta-analysis was performed by RevMan5.3 software. RESULTS A total of 9 clinical trials containing 875 patients were finally included. The results of meta-analysis showed that: according to ITT analysis, the Hp eradication rate of PQT as a rescue regimen was higher than that of BQT, but the difference was not statistically significant(RR=1.03, 95%CI: 0.97-1.10, P=0.36); according to PP analysis, the Hp eradication rate of PQT versus BQT was considerable,but the difference was not statistically significant (RR=1.00, 95%CI: 0.94-1.07, P=0.90). The incidence of adverse reactions of PQT was significantly lower than that of the control group, and the difference was statistically significant (RR=0.31, 95%CI:0.23-0.41,p<0.000 01). CONCLUSION Compared with BQT, the incidence of adverse reactions of PQT is lower, but there is no significant difference in Hp eradication rate between the two therapies. More large-scale and high-quality studies are needed to confirm the above conclusions.
KEY WORDS:Helicobacter pylori; probiotics; bismuth; meta-analysis; systematic review
REFERENCES
中图分类号:R969.4
文献标志码:B
文章编号:1007-7693(2017)12-1751-05
DOI:10.13748/j.cnki.issn1007-7693.2017.12.024
引用本文:周本刚, 冯秋曲, 李仕宇, 等. 益生菌四联对比铋剂四联疗法补救根除幽门螺杆菌感染的Meta分析[J]. 中国现代应用药学, 2017, 34(12): 1751-1755.
作者简介:周本刚,男,硕士,医师 Tel: 13687185761 E-mail: zhoubengang198903@126.com*
通信作者:王宏志,男,硕士,副主任医师 Tel: 15826989592 E-mail: whz109@163.com
收稿日期:2017-06-11
(本文责编:蔡珊珊)




