“桂枝与白芍”药对入血成分UPLC-Q/TOF-MS分析
陈永财1,钱江辉2,3,王彬辉4,沙先谊2,3*
(1.温州市中医院药剂科,浙江 温州 325000;2.复旦大学药学院药剂学教研室,上海201203;3.复旦大学中西医结合研究院,上海 201203;4.台州学院医学院附属市立医院药剂科,浙江 台州 318002)
摘要:目的 对“桂枝与白芍”药对中的入血成分进行定性分析与鉴定。方法 采用UPLC,选择C18反相色谱柱,以乙腈-0.1%冰醋酸水为流动相,梯度洗脱进行分离;联用电喷雾飞行时间质谱(ESI-TOF-MS/MS)分别在正离子与负离子模式下获得入血各成分的精确分子量和分子式;通过各成分裂解碎片信息,结合文献对药对中的入血成分进行鉴定。结果 由MS和MS/MS结果鉴定出12个入血成分,主要包括没食子酸、原儿茶酸等4种有机酸,芍药苷、芍药内酯苷等6种芍药总苷单萜类化合物及香豆素类成分。结论 血中移行成分的分析为明确“桂枝与白芍”药对体内药效物质基础提供了科学依据。
关键词:桂枝;白芍;药对;UPLC-Q/TOF-MS;入血成分
“桂枝与白芍”为典型的相制配伍,源于《伤寒论》之桂枝汤,在桂枝汤、桂枝加芍药汤、桂枝加桂汤等方剂中都用到了桂枝和白芍的配伍,桂枝透达营卫,解肌发表,外散风寒;白芍益阴敛营,二药配伍,一收一散,一寒一温,相互制约,既有收调营卫、和气血,又有启发心阳、益阴止汗之功,为临床常用的调和营卫、温通止痛药对[1-2]。现代研究证明,桂枝中桂皮醛、肉桂酸等成分,白芍中芍药苷、芍药内酯苷等成分具有明显药理活性[3-4]。但其体内作用成分及代谢过程研究报道较少,药效物质基础尚不明确,通过分析中药口服给药后血清中成分,确定其中药的体内直接作用物质,将成为快速、正确地研究确定中药药效物质基础的有效途径[5],可见全面分析核心“桂枝与白芍”药对血中移行成分尤为关键。
本实验采用血清药物化学研究方法,通过UHPLC-Q/TOF-MS指纹图谱技术观察“桂枝与白芍”药对经口服后的体内动态过程,确定“桂枝与白芍”药对血中移行成分,为最终确定“桂枝与白芍”药对药效物质成分奠定基础。
1 仪器与材料
1.1 仪器与试剂
Agilent 1290超高液相色谱仪(美国Agilent);AB 5600+Q-TOF高分辨质谱仪(美国 Applied Biosystems);Analyst®TF1.6用于采集数据、Peak View 2.0用于数据分析处理;YMC-Triart C18色谱柱(100 mm×2.1 mm,1.9 µm);BT 25S分析天平、BT 210S天平(北京赛多利斯);TGL-16G高速离心机(上海安亭科学仪器厂);XW-80A旋涡振荡仪(海门市其林贝尔仪器制造有限公司);SK2510HP超声波清洗器(上海超导超声仪器有限公司);0.45 µm微孔滤膜(津腾);FL-1型可调式封闭电炉(北京市永光明医疗仪器有限公司);RE-2000A旋转蒸发器(上海亚荣生化仪器)。
乙腈(色谱纯,批号:AS1122-801)、甲醇(色谱纯,批号:MS1922-801)购自Tedia;乙酸(分析纯,国药集团化学试剂总公司,批号:20131016);水为超纯水。芍药苷对照品(批号:110736-201438,纯度:99.5%)、桂皮醛对照品(批号:110710-201418,纯度:99.4%)均购自中国食品药品检定研究院;儿茶素、没食子酸、原儿茶酸、没食子酸甲酯、芍药苷内酯、没食子酸乙酯、丁香醛、香豆素、肉桂酸、丹皮酚对照品(批号分别为 15082731,15033122,15090235,15051322,15010332,15072821,15012321,15072141,15051935,15072836,纯度均为98%)购自上海同田制药。桂枝、白芍中药饮片购自浙江华宇中药饮片有限公司(批号分别为1503190,1505100),经浙江中医药大学张水利教授鉴定桂枝为樟科植物肉桂(Cinnamomum cassia Presl)的干燥嫩枝,白芍为毛茛科植物芍药(Paeonia lactiflora Pall)的干燥根。
1.2 动物及饲料
SPF级SD大鼠,♂,体质量220~250 g,由复旦大学实验动物中心供应,实验动物许可证号:SYXK(沪)2010-0099。
2 方法与结果
2.1 分析条件
色谱条件:Agilent 1290 UPLC,YMC-Triart C18色谱柱(100 mm×2.1 mm,1.9 µm),流动相:乙腈(A)-0.1%冰醋酸水溶液(B),梯度洗脱程序[6-7]为 0~5 min,13%A;5~25 min,13%→35%A;25~30 min,35%→65%A;30~33 min,65%A。温度:30 ℃;检测波长:254 nm;流速:0.3 mL·min-1;进样量:5 µL。
质谱条件:电喷雾(ESI)源,正负离子模式;雾化气(Gas1):50 psi;辅助加热气(Gas2):50 psi;气帘气(Curtain Gas):30 psi;离子源温度:550 ℃;正负电压:5 500 V/-4 500 V;去簇电压(DP):±80 V;碰撞电压(CE):±40 V;一级MS扫描范围:50~1 000;二级 MS/MS扫描范围:50~1 000。
2.2 混合对照品溶液制备
分别精密称取芍药苷、桂皮醛、儿茶素、没食子酸、原儿茶酸、没食子酸甲酯、芍药苷内酯、没食子酸乙酯、丁香醛、香豆素、肉桂酸、丹皮酚12种对照品10 mg,用甲醇配成1 mg·mL-1母液。取上述各对照品母液200 µL,用甲醇定容至10 mL量瓶中,配成混合对照品溶液。
2.3 供试品溶液制备
2.3.1 “桂枝与白芍”药对水煎液提取物制备 按“桂枝与白芍”药对(1∶1)取桂枝90 g、白芍90 g,采用伤寒论中“桂枝汤”煎煮方法[2],按正交优选条件[8]加水量10倍、浸泡60 min、煮沸后微火煎煮60 min,合并2次提取液,过滤,减压浓缩并调整至相当生药 6 g·g-1的稠浸膏备用,精密称100 mg浸膏,加 50%乙腈水溶液 10 mL,涡旋1 min,超声 5 min,0.45 µm 微孔滤膜过滤,按“2.1”项下色谱条件测定。
2.3.2 桂枝和白芍单味水煎液提取物制备 称取桂枝90 g和白芍90 g分别单独煎煮,按“2.3.1”项下方法制备单味桂枝和单味白芍供试品。
2.3.3 血浆样品的采集与处理 取清洁级 SD大鼠,禁食过夜自由饮水,称取“桂枝与白芍”药对(1∶1)提取物3.5 g,加入3.5 mL纯水超声混合均匀,每只灌胃3 mL,空白组灌胃等体积的蒸馏水。给药后于30 min于眼眶静脉采血2 mL,置于预加肝素的试管中10 000 r·min-1离心10 min,取上层血浆,置于-20 ℃保存。将冻存血浆取出,室温融化,吸取500 µL血浆,加入2 mL甲醇蛋白沉淀,涡旋 1 min 后,10 000 r·min-1离心 10 min,取上清,用N2吹干后,加入100 µL甲醇充分涡旋溶解,10 000 r·min-1离心10 min取上清溶液进样UPLC-Q/TOF-MS分析,大鼠空白血浆同上述方法处理。
2.4 “桂枝与白芍”药对(1∶1)含药血清成分分析
根据大鼠灌胃给药桂枝与白芍(1∶1)共煎液30 min后血清样UPLC-Q/TOF-MS/MS提取总离子流图,与空白对照组比较,分析入血成分或代谢成分见图1。

图 1 “桂枝与白芍”药对(1∶1)体内外化学成分UPLC-Q/TOF-MS/MS总离子流色谱图A-“桂枝与白芍”药对(1∶1)体外成分ESI-;B-“桂枝与白芍”药对(1∶1)体内血浆成分ESI-;C-空白血浆ESI-。
Fig. 1 Total ion current chromatogram of chemical constituentsin vitroorin vivoby UPLC-Q/TOF-MS/MS from Ramulus Cinnamomi and Paeoniae Radix Alba drug pair(1∶1)
A-ESI-of chemical constituents of “Cinnamomum cassiaPresl and Paeoniae Radix” Alba drug pair(1∶1)in vitro; B-ESI-of chemical constituents of “Ramulus Cinnamomi and Paeoniae Radixin vivo; C-ESI-of blank plasma.
质谱分析软件Peak View®2.2的Formula finder和Master view 2种功能对主要出峰化合物进行鉴别。根据对照品的保留时间和质谱特征、化合物MS一级质谱和MS/MS二级质谱信息,进行成分确认;除此以外根据相关文献报道和体外成分分析结果[9],进一步比较质谱信息进行成分推测和确认,结果见表1。
tR为 1.43 min在 ESI-下得到一级质谱m/z为169.015 3[M-H]-,进行MS/MS特征碎片峰离子分析m/z125和m/z79,其与没食子酸对照品出峰时间和质谱行为一致。根据体外分析单味桂枝和单味白芍都含有没食子酸[10],推测以原型形式入血。体外成分分析中含有没食子酸芍药苷,体内却没有发现,因此推测部分没食子酸来自没食子酸芍药苷体内代谢产物。
tR为 2.40 min在 ESI-下得到一级质谱m/z为153.020 7[M-H]-,进行MS/MS特征碎片峰离子分析m/z109,其与原儿茶酸对照品出峰时间和质谱行为一致。根据体外分析单味桂枝和单味白芍都含有原儿茶酸[10],推测以原型形式入血。
tR为2.92 min在ESI-下得到准分子离子峰m/z为495.150 8 [M-H]-,并且进行MS/MS碎片峰离子分析,发现特征碎片离子峰m/z137为对羟基苯甲酸,m/z165为蒎烷基本骨架结构碎片;分子离子脱去一分子糖苷形成m/z333 [M-C6H10O5-H]-;分子离子脱去一分子甲醛形成m/z465[M-CH2O-H]-,推断该化合物为氧化芍药苷[11],并且体外共煎液中也发现该化合物,因此该化合物以原型入血。
表1 “桂枝与白芍”药对(1∶1)水煎液给药后大鼠体内入血成分分析
Tab. 1 Analysis of the components absorbed into plasma in rats after decoction of Ramulus Cinnamomi and Paeoniae Radix Alba drug pair(1∶1)
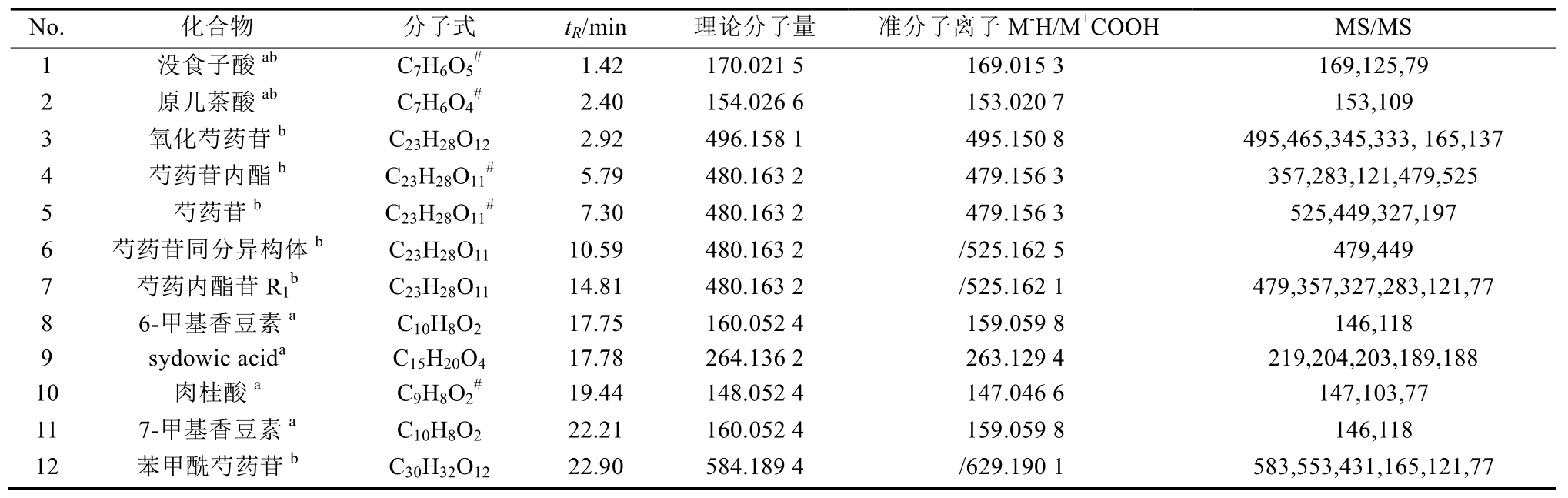
注:a-桂枝,b-白芍;#-通过对照品分析确认。
Note: a-Ramulus Cinnamomi, b-Paeoniae Radix Alba; #-confirmed through standard analysis.
No. 化合物 分子式tR/min 理论分子量 准分子离子M-H/M+COOH MS/MS 1 没食子酸abC7H6O5#1.42 170.021 5 169.015 3 169,125,79 2 原儿茶酸abC7H6O4#2.40 154.026 6 153.020 7 153,109 3 氧化芍药苷bC23H28O122.92 496.158 1 495.150 8 495,465,345,333, 165,137 4 芍药苷内酯bC23H28O11#5.79 480.163 2 479.156 3 357,283,121,479,525 5 芍药苷bC23H28O11#7.30 480.163 2 479.156 3 525,449,327,197 6 芍药苷同分异构体bC23H28O1110.59 480.163 2 /525.162 5 479,449 7 芍药内酯苷R1bC23H28O1114.81 480.163 2 /525.162 1 479,357,327,283,121,77 8 6-甲基香豆素aC10H8O217.75 160.052 4 159.059 8 146,118 9 sydowic acidaC15H20O417.78 264.136 2 263.129 4 219,204,203,189,188 10 肉桂酸aC9H8O2#19.44 148.052 4 147.046 6 147,103,77 11 7-甲基香豆素aC10H8O222.21 160.052 4 159.059 8 146,118 12 苯甲酰芍药苷bC30H32O1222.90 584.189 4 /629.190 1 583,553,431,165,121,77
tR为5.79 min和14.81 min的峰在ESI-模式下分别得到准分子离子峰 m/z为 525.161 8[M+COOH]-和 525.162 1 [M+COOH]-, 其 中5.79 min已经通过对照品确认为芍药苷內酯。通过对芍药苷内酯二级质谱MS/MS碎片峰离子分析,其质谱裂解规律跟芍药苷类似,不同的是存在特征离子峰m/z 283为[M-CO2-C7H5O2-H]-,其中CO2为内酯环断裂失去酯基。而14.81 min断裂方式与芍药苷内酯相同,根据文献报道存在同分异构体芍药内酯苷R1[12],因此推断为该化合物,两者都以原型形式入血。
tR为7.30 min和10.59 min在ESI-下分别得到准分子离子峰m/z为525.160 2 [M+COOH]-,其中7.30 min已经通过对照品确认为芍药苷。通过对芍药苷二级质谱MS/MS碎片峰离子分析,存在特征离子峰为苯甲酰m/z 121,蒎烷基本骨架m/z 165,苯环基本骨架m/z 165;分子离子脱去一分子甲醛形成m/z 449 [M-CH2O-H]-,再脱去一分子水形成m/z 431 [M-CH2O-H]-;分子脱去苯甲酰基形成m/z 357[M-C7H5O2-H]-;分子脱去一分子糖苷形成m/z 327[M-C6H12O5-H]-[11]。而14.81 min断裂方式与芍药苷相同,因此推断为芍药苷同分异构体。体外成分分析中含有没食子酸芍药苷,体内却没有发现,因此推测部分芍药苷来自没食子酸芍药苷体内代谢产物。
tR为 17.75 min在 ESI-下得到准分子离子峰m/z为159.059 8 [M-H]-,在体外正离子模式下得到准分子离子峰m/z为161.069 8 [M+H]+,存在特征离子峰为苯环 m/z 77;分子脱去一个甲基形成m/z 146 [M-CH3+H]+,再脱去一氧化碳形成m/z 118[M-CH3-CO+H]+[13],推断该化合物为甲基香豆素。负离子模式与正离子模式出峰时间一致,碎片离子相似并且在22.21 min发现相似化合物,二级质谱结构相似,推测为甲基香豆素同分异构体。根据出峰时间推断 17.75 min为 6-甲基香豆素,22.21 min为7-甲基香豆素,因此体内推测该化合物以原型入血。体外成分分析中含有香豆素成分,而体内却没有发现,这 2种化合物部分可能来源于香豆素羟基化代谢产物[14]。
tR为 17.78 min在 ESI-下得到准分子离子峰m/z为263.136 2 [M-H]-,并且进行MS/MS碎片峰离子分析,存在特征离子峰为m/z 119和m/z 136为分子断裂形成;分子脱去一分子 CO2形成 m/z 219 [M-CO2-H]-,再脱去一个甲基形成为m/z 204[M-CO2-CH3-H]-,再脱去一个甲基形成为m/z 189[M-CO2-2CH3-H]-。根据元素组成分析化合物分子式为C15H20O4,因此推断该化合物为sydowic acid。该成分以原型入血。
tR为 19.44 min 在 ESI-模式下得到147.046 6 [M-H]-,其与肉桂酸对照品出峰时间一致,进行 MS/MS碎片峰离子分析,m/z 103[M-COOH]-,m/z 77为苯环特征峰,因此确定此化合物为肉桂酸,该成分以原型入血。
tR为 22.90 min在 ESI-下得到准分子离子峰m/z为 629.186 5 [M+COOH]-,并且进行 MS/MS碎片峰离子分析,存在特征离子峰为苯甲酰 m/z 121,苯环特征峰 m/z 77和蒎烷骨架碎片峰m/z 165;分子脱去氢形成m/z 583 [M-H]-,再脱去一分子甲醛形成为m/z 553 [M-CH2O-H]-,再脱去一分子水形成为m/z 535 [M-CH2O-H2O-H]-[11]。根据元素组成分析化合物分子式为C30H32O12,因此推断该化合物为苯甲酰芍药苷,该成分以原型入血。
3 讨论
UPLC-Q-TOF/MS分析方法,具备高分离度,高分辨率、高质量精度和高灵敏度等特点,且可进行快速分析[15-16],一次进样,即可保证在复杂基质样品中能获得低浓度代谢物的高质量MS/MS,快速筛选分析中药复方用于代谢物的鉴定,成为中药复方体内外成分分析首选,运用血清药物化学研究方法,本实验前期建立“桂枝与白芍”药对化学成分 UPLC-Q-TOF/MS分析,明确了体外化学成分[9],在此基础上,对比和分析空白血浆、给药血浆和“桂枝与白芍”药对水煎液中获得对应化合物的提取总离子图,快速分离并初步鉴定“桂枝与白芍”药对(1∶1)水煎液主要以原型成分吸收12个入血成分,明确了各移行成分的中药归属。通过分析中药复方口服给药后血清中成分,确定其中药的体内直接作用物质,将成为快速、正确地研究确定中药药效物质基础的有效途径,得到广泛应用。
本实验结果可知,“桂枝与白芍”药对(1∶1)入血成分主要含有没食子酸、肉桂酸等 4种有机酸和芍药苷、芍药内酯苷及其同分异构体等 6种芍药总苷单萜类化合物及香豆素类成分。没食子酸有抑菌、抗炎、抗病毒、抗氧化、保护心血管作用[17];原儿茶酸有显著降低心肌耗氧量、提高心肌耐氧能力、减慢心率等作用[18];肉桂酸具有抗菌、升高白细胞、利胆等药理活性[19-20];芍药总苷具有镇痛、抗炎、免疫调节、改善血液流变学等作用[21],香豆素具有抗氧化、抗菌活性作用[22]。中药口服给药后只有被吸收入血的成分才能产生药效,可见“桂枝与白芍”药对(1∶1)中有机酸、芍药总苷单萜类化合物、香豆素类等化学成分为“桂枝与白芍”药对主要的药效物质基础。
实验中优选采用甲醇沉淀蛋白浓缩富集法入血成分数目最多,并且优化了取血时间为 30 min入血成分数目最多,为最佳取血时间。实验还优选色谱条件得出乙腈分离效果和洗脱能力都强于甲醇,且部分成分不出现拖尾现象,实验发现加入0.1%醋酸有利于改善色谱峰的分离度和出峰峰型。有机酸类和芍药苷类物质在 ESI-条件下响应更高,质谱结构分析以ESI-解析为主。
[1] 李贵海, 涂晓龙. 常用中药药对分析与应用[M]. 北京: 人民卫生出版社, 2009: 235-237.
[2] 李冀. 方剂学[M]. 北京: 中国中医药出版社, 2012: 27-28.
[3] 许源, 宿树兰, 王团结, 等. 桂枝的化学成分和药理研究[J]. 中药材, 2013, 36(4) : 674-678.
[4] LI W Y, HUANG S J, WANG R, et al. Advances in research on pharmacological actions and quality control of Paeoniae Radix Alba [J]. Pharm Care Res(药学服务与研究), 2012,12(2): 118-122.
[5] LI W X, TANG Y P, LIU L, et al. Research on Chinese medicine pairs()Ⅲ—their bio-active components [J]. China J Chin Mater Med(中国中药杂志), 2013, 38(24): 4196-4202.
[6] 王连芝, 董静艳. 桂枝与白芍配伍的 HPLC指纹图谱研究[J]. 中医药信息, 2010, 27(4): 32-34.
[7] PEI Y L, WU Z S, SHI X Y, et al. Study on drug pair of cassia twig and white peony root by HPLC/MS aualysis based on theory of “Xin-Gan Hua-Yang and Suan-Gan Huan-Yin” [J].World Sci Tech/Mod Tradit Chin Med Mater Med(世界科学技术-中医药现代化), 2014, 16(10): 2180-2184.
[8] CHEN Y C, WANG B H, LIN J. Optimization of decoction process of herbal pair of Ramulus Cinnamomi and Radix Paeoniae Alba by orthogonal test [J]. Pract Pharm Clin Rem(实用药物与临床), 2016, 19(12): 1530-1534.
[9] CHEN Y C, QIAN J H, WANG B H, et al. Chemical constituents analysis of the drug pair of “Cinnamomum cassia Presl and Paeoniae Radix Alba” by UPLC-Q/TOF-MS [J].China Med Herald(中国医药导报), 2017, 14(16): 12-15.
[10] CHEN Y C, QIAN J H, WANG B H, et al. Discussion on HPLC fingerprints for the different compatibility proportion Ramulus Cinnamomi and Radix Paeoniae Alba [J]. China Med Her(中国医药导报), 2017, 14(13): 29-33.
[11] ZHENG M X, CHEN Z, LIU P, et al. Analysis and identification of glycosides in paeonia lactiflora by UPLC-MS/MS [J]. China J Chin Mater Med(中国中药杂志),2011, 36(12): 1641-1643.
[12] REN J Q, LIU C M, WANG Y Q, et al. Determination of chemical compositions in extract of Radix Paeoniae Alba by liquid chromatography-electrospray ionization mass spectrometry [J]. Chin J Pharm Anal(药物分析杂志), 2014,34(10): 1375-1376.
[13] LI K P, GAO C K, LI W M. Analysis of coumarins in extract of cnidium monnieri by ultra performance liquid chromatographic coupled to electrospray ionization time of flightmass/Mass spectrometry [J]. Chin Tradit Patent Med(中成药), 2009, 31(4): 584-587.
[14] XU Q, XU G B. Metabolism research review of coumarin compounds [J]. Chin J Exp Tradit Med Form(中国实验方剂学杂志), 2014, 21(3): 222-225.
[15] SHEN L H, PENG Y W, CHEN G Q. Rapid detection of phenformin hydrochloride, glibenclamide and pioglitazone hydrochloride illegally mixed in traditional Chinese medicinal preparation for antidiabetics by UPLC-Q-TOF-MS [J]. Chin J Mod Appl Pharm(中 国 现 代 应 用 药 学 ), 2016, 33(9):1160-1165.
[16] ZOU Y H, ZHUNGE L. Determination illegal added diclofenac in slimming health care products by UPLC-Q-TOF-MS [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2016, 33(8): 1048-1051.
[17] GAO Y, LI H, WANG S W, et al. Research progress of pharmacological action and pharmacokinetics of gallic acid [J].Northwest Pharm J(西北药学杂志), 2014, 29(4): 435-438.
[18] 饶曼人, 刘广余, 高长忠, 等. 原儿茶酸对缺血区心肌代谢及心肌梗塞范围的影响[J]. 中国药理学报, 1988, 9(1):27-30.
[19] 柯铭清. 中草药有效成分理化与药理特性[M]. 长沙: 湖南科学技术出版社, 1982: 226.
[20] LIANG S N, DUAN Z F, FU L, et al. Comparative research on the antibacterial action of several types of cinnamic acid derivative and cinnamic acid [J]. Food Sci Tech(食品科技),2005, 9(22): 71-73.
[21] 蒋午峻, 王巧, 李小娜, 等. 白芍总苷的药理作用和质量控制方法研究进展[J]. 河北医科大学学报, 2006, 27(5):500-502.
[22] LI J Z, HUANG C S, LIU H X, et al. The study progress on relationship of pharmacological action to structure for natural coumarins [J]. J Guangxi Teach Edu Univ: Nat Sci Edit(广西师范学院学报: 自然科学版), 2007, 24(1): 93-98.
Analysis of Components Absorbed into Plasma of the Drug Pair of Ramulus Cinnamomi and Paeoniae Radix Alba by UPLC-Q/TOF-MS
CHEN Yongcai1, QIAN Jianghui2,3, WANG Binhui4, SHA Xianyi2,3*
(1.Department of Pharmaceutics, Wenzhou Hospital of TCM, Wenzhou 325000, China; 2.Department of Pharmaceutics, School of Pharmacy, Fudan University, Shanghai 201232, China; 3.Academy of Integrative Medicine, Fudan University, Shanghai 201232, China; 4.Department of Pharmaceutics,Affiliated Hospital of Taizhou Medical College, Taizhou 318002, China)
ABSTRACT:OBJECTIVE To set up a rapid analysis and characterization for the components absorbed into plasma of the drug pair of Ramulus Cinnamomi and Paeoniae Radix Alba in rats. METHODS The sampls was analyzed by UPLC with a reversed phase C18column using a eluent of acetonitrile and 0.1% acetic acid solution under gradient conditions. The ions of the components absorbed into plasma were observed by electrospray ionization (ESI) time of flight mass spectrometry(ESI-TOF-MS) under positive or negative mode, and the fragmentation behavior obtained by MS/MS, then the components were identified through the accurate molecular weight and molecular formula with literature review. RESULTS Tweleve components absorbed into plasma were qualitative identified by MS and MS/MS. These components included four kinds of organic acid such as gallic acid, protocatechuic acid, et al, six total paeoniflorin monoterpenes like paeoniflorin and albiflorin,and coumarins. CONCLUSION The analysis of the components absorbed into plasma provides cientific basis for the effective substances in the drug pair of Ramulus Cinnamomi and Paeoniae Radix Alba.
cientific basis for the effective substances in the drug pair of Ramulus Cinnamomi and Paeoniae Radix Alba.
KEY WORDS:Ramulus Cinnamomi; Paeoniae Radix Alba; drug pair; UPLC-Q/TOF-MS; components absorbed into plasma
REFERENCES
中图分类号:R284.1
文献标志码:B
文章编号:1007-7693(2017)12-1707-05
DOI:10.13748/j.cnki.issn1007-7693.2017.12.014
引用本文:陈永财, 钱江辉, 王彬辉, 等. “桂枝与白芍”药对入血成分UPLC-Q/TOF-MS分析[J]. 中国现代应用药学, 2017,34(12): 1707-1711.
基金项目:浙江省中医药资助项目(2015ZA195);温州市公益性科技计划项目(Y20140746)
作者简介:陈永财,男,副主任药师 Tel: (0577)56671566 E-mail: wzchycai@126.com*
通信作者:沙先谊,男,副教授,博导 Tel:(021)51980071 E-mail: shaxy@fudan.edu.cn
收稿日期:2017-05-22
(本文责编:李艳芳)


 cientific basis for the effective substances in the drug pair of Ramulus Cinnamomi and Paeoniae Radix Alba.
cientific basis for the effective substances in the drug pair of Ramulus Cinnamomi and Paeoniae Radix Alba.