HPLC测定拉坦前列素滴眼液复杂系统中的有关物质及含量
陈悦1,王玲2,高芳3,王建1*
(1.浙江省食品药品检验研究院,杭州 310052;2.浙江昌明药业有限公司,浙江 台州 317200;3.浙江工业大学,杭州 310014)
摘要:目的 建立HPLC测定拉坦前列素滴眼液复杂系统中的有关物质及含量的方法。方法 采用糖涂敷型手性色谱柱(4.6 mm×250 mm,5 µm),有关物质测定以0.005 mol·L-1磷酸二氢钠溶液(用磷酸调节pH值至2.7)-乙腈(56∶44)为流动相,含量测定以0.005 mol·L-1磷酸二氢钠溶液(用磷酸调节pH值至2.7)-乙腈(54∶46)为流动相,检测波长为200 nm,流速为0.5 mL·min-1。结果 有关物质测定中2个已知杂质与主峰之间的分离度良好,线性关系良好,5,6-反式-拉坦前列素和15S-拉坦前列素的平均回收率分别为101.5%和99.5%,拉坦前列素、5,6-反式拉坦前列素和15S-拉坦前列素的定量限(S/N≈10)分别为0.12,0.13和0.12 µg·mL-1;含量测定线性关系良好,重复性RSD=0.90%,拉坦前列素平均回收率为98.8%。结论 建立的方法准确可靠,可用于拉坦前列素滴眼液的质量控制。
关键词:拉坦前列素滴眼液;高效液相色谱法;有关物质;含量测定
拉坦前列素是一种新型苯基替代的丙基酯前列素F2a,为选择性F2a受体激动剂。它是一种无活性但能迅速渗透到角膜里的物质,在角膜和血浆中可水解为具有活性的游离酸。拉坦前列素滴眼液临床上用于降低开角型青光眼和高眼压症患者升高的眼压[1]。拉坦前列素滴眼液国内有成都恒瑞制药有限公司、鲁南贝特制药有限公司、北京紫竹药业有限公司和大连美罗大药厂4家药厂生产。另已有比利时辉瑞制药有限公司(适利达,进口药品注册标准编号:JX19980038)、印度太阳药业有限公司和联邦化学制药股份有限公司获得进口注册证。韩国Taejoon Pharm公司在申请进口注册中。
调研发现,拉坦前列素滴眼液的处方极复杂,各厂家的产品处方各不相同,生产中添加的防腐剂就有苯扎氯铵、苯扎溴铵和吐温80等多种,而这些不同的防腐剂在该药的含量测定或有关物质检查的色谱系统中会出现 2个或多个杂质峰,从而干扰该药活性成分的测定。查阅相关资料发现,该药在各国药典中均未见收载,现行的拉坦前列素滴眼液国内外质量标准和参考文献中,也没有一个合适的方法能适用所有厂家的产品[2-6]。但是,该药的主药成分拉坦前列素对热不稳定,需冷藏保存,再加之复杂的处方工艺,使得该药的有关物质相对也较复杂。为了进一步严格控制该药的产品质量,本研究考察了拉坦前列素的主要降解产物和实际存在的主要工艺杂质 15S-拉坦前列素和5,6-反式拉坦前列素,并对其进行了限度控制。
综合各厂家的产品处方,本研究考察了缓冲盐浓度、乙腈比例和柱温等因素对拉坦前列素、苯扎氯铵、吐温80和5,6-反式-拉坦前列素色谱行为的影响,在拉坦前列素滴眼液申请进口注册标准(韩国Taejoon Pharm Co., Ltd.公司)和进口注册标准JX19980038基础上,改进和优化了色谱条件,使各成分色谱峰间都得到了较好的分离。本实验所建立的 HPLC方法能适用所有厂家生产的拉坦前列素滴眼液的有关物质检查和含量测定。该方法通过对已知的特定杂质的控制,可以达到对该药质量的控制,为今后该药的质量控制提供技术支持。
1 仪器和试药
Agilent 1260液相色谱仪(包括在线真空脱气机,四元泵,自动进样系统等),拉坦前列素滴眼液(鲁南贝特制药有限公司,批号:60120503,60131001,60131002,60131003;北京紫竹药业有限公司,批号:74131024;成都恒瑞制药有限公司,批号:130401,130402,130403;比利时辉瑞制药有限公司,批号:Z0832);苯扎氯铵、苯扎溴铵、拉坦前列素酸(批号:LTWS1101,纯度:99.6%)、15S-拉坦前列素(批号:LT1M11001,纯度:99.8%)和5,6-反式-拉坦前列素对照品(批号:LT1M11201,纯度:99.8%)均由成都恒瑞制药有限公司提供。
2 方法和结果
2.1 色谱条件
多糖涂敷型手性色谱柱(Chiralcel OD-R,4.6 mm×250 mm,5 µm);流动相:0.005 mol·L-1磷酸二氢钠溶液(用磷酸调节 pH 值至 2.7)-乙腈(56∶44);检测波长:200 nm;柱温:25 ℃;流速:0.5 mL·min-1。
2.2 溶液配制
取 5,6-反式-拉坦前列素对照品和拉坦前列素滴眼液各适量,加流动相溶解并稀释制成每1 mL中分别约含0.5 μg和50 μg的溶液,作为系统适用性溶液;分别取苯扎氯铵、苯扎溴铵和辅料(吐温80、磷酸氢二钠、磷酸二氢钠和氯化钠)各适量,加流动相制成200 μg·mL-1的溶液,作为防腐剂辅料溶液。分别取拉坦前列素合成工艺的中间体、副产物 15S-拉坦前列素和 5,6-反式-拉坦前列素对照品及拉坦前列素各适量,加流动相制成2 μg·mL-1的溶液,作为各杂质的定位溶液。
精密称取拉坦前列素对照品适量,加流动相溶解并定量稀释制成每1 mL中约含0.5 μg的溶液,作为有关物质对照品溶液;取本品摇匀,取适量作为有关物质供试品溶液。精密称取拉坦前列素对照品约10 mg,置20 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀,精密量取1 mL,置20 mL量瓶中,加流动相10 mL,加水稀释至刻度,作为含量测定的对照品溶液。精密量取本品5 mL,置10 mL量瓶中,加流动相稀释至刻度,作为含量测定供试品溶液。2.3 样品测定
取上述系统适用性溶液、杂质定位溶液、防腐剂辅料溶液、对照品及供试品溶液各20 μL用于HPLC分析,记录色谱图。结果见图1,各批样品有关物质及含量测定结果见表1。结果表明,拉坦前列素峰与 5,6-反式-拉坦前列素峰的分离度为1.59,已实现良好分离,杂质 15S-拉坦前列素和5,6-反式-拉坦前列素也完全分离。苯扎氯铵、苯扎溴铵和辅料峰(吐温80、磷酸氢二钠、磷酸二氢钠和氯化钠)对主峰含量测定无干扰。
2.4 方法学试验
2.4.1 破坏试验 分别精密量取 5份拉坦前列素滴眼液样品2 mL,其中2份分别加入0.1 mol·L-1氢氧化钠溶液 0.5 mL和 0.1 mol·L-1盐酸溶液0.5 mL,放置24 h后中和,滤过;一份加30%过氧化氢溶液0.5 mL,放置4 h;另外2份分别在60 ℃下放置6 h和于强光下(4 500 lx)照射48 h,取上述处理后的溶液各20 μL进样分析,结果拉坦前列素对酸、碱、高温、氧化破坏均不稳定,有降解产物产生,拉坦前列素的主要降解产物为拉坦前列素酸,对杂质15S-拉坦前列素和5,6-反式-拉坦前列素的测定无干扰。
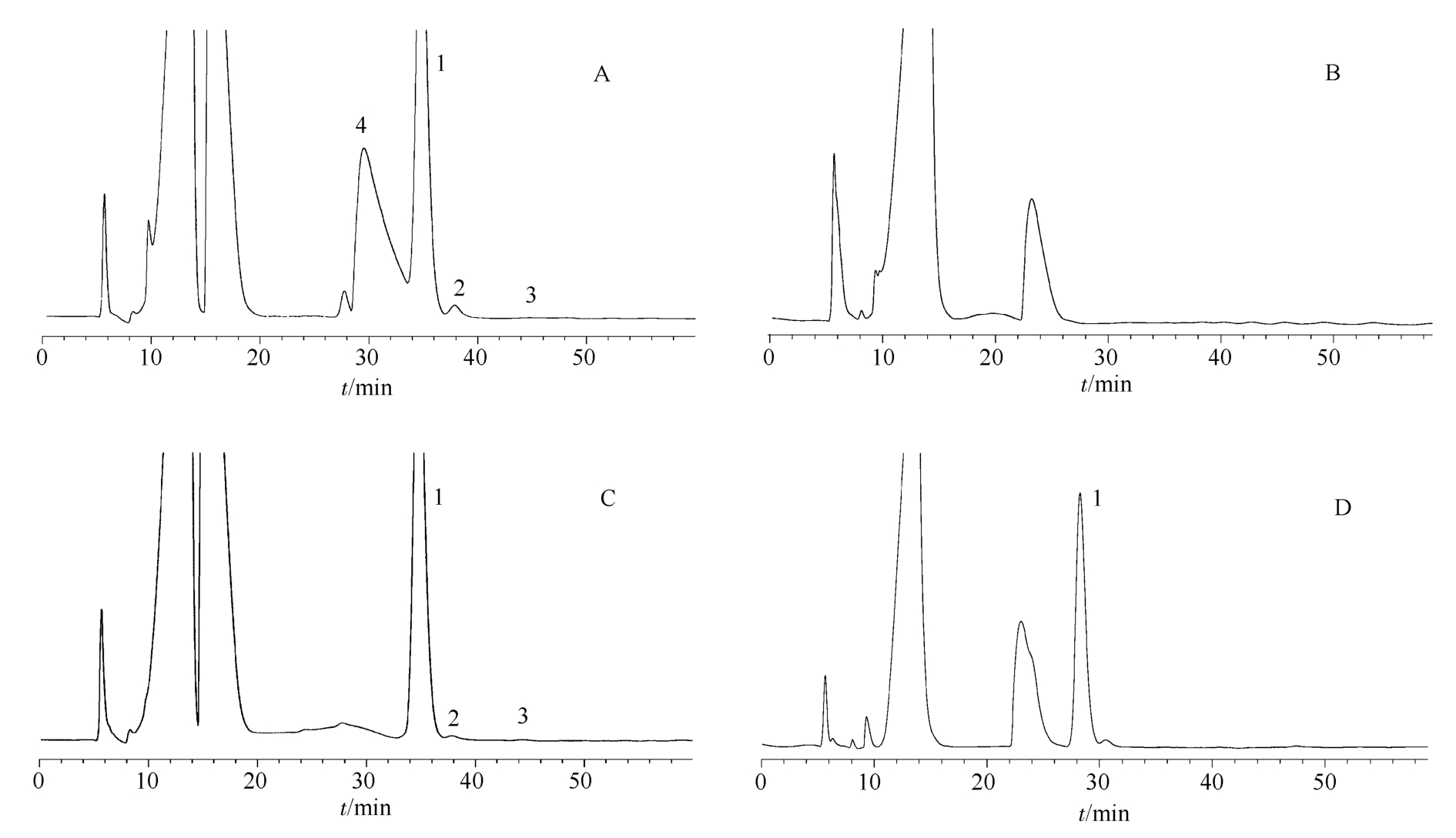
图1 HPLC色谱图
A-系统适用性溶液;B-防腐剂辅料溶液;C-供试品溶液有关物质;D-供试品溶液;1-拉坦前列素;2-5,6-反式-拉坦前列素;3-15S-拉坦前列;4-苯扎氯铵。
Fig. 1 The HPLC chromatogram
A-system suitability test solution; B-antiseptic and accessories solution; C-related substances; D-sample; 1-latanoprost; 2-5,6-trans-latanoprost;3-15S-latanoprost; 4-benzalkonium chloride.
表1 有关物质和含量测定结果
Tab.1 Results of the related substances and assay %

检测成分批号60120503 60131001 60131002 60131003 74131024 130401 130402 130403 Z08325 5,6-反式拉坦前列素 未检出 未检出 未检出 未检出 0.6 未检出 未检出 未检出 2.6 15S-拉坦前列素 未检出 未检出 未检出 未检出 0.3 未检出 未检出 未检出 0.2拉坦前列素含量 94.3 91.9 92.5 92.9 94.3 93.9 94.3 95.4 97.4
2.4.2 线性关系考察 精密称取拉坦前列素、5,6-反式-拉坦前列素和 15S-拉坦前列素对照品各适量,加流动相溶解并稀释,制成一系列浓度的杂质对照品溶液,进样测定,色谱峰面积(A)与浓度(C)呈良好的线性关系,结果见表 2。本品中可能存在的已知杂质为 15S-拉坦前列素和 5,6-反式-拉坦前列素均能与拉坦前列素完全分离,与拉坦前列素的相对响应因子分别为1.0和1.1,因此采用自身对照法测定,同时将 5,6-反式-拉坦前列素峰与主峰的分离度订入系统适用性要求。考虑到15S-拉坦前列素对照品的难获得性,因此以相对保留时间定位。
2.4.3 定量限 通过逐级稀释,进样测定,确定拉坦前列素、5,6-反式拉坦前列素和15S-拉坦前列素的定量限(S/N≈10)分别为 0.1,0.1,0.1 μg·mL-1。本法设计的供试品溶液浓度,可满足有关物质检测的要求。
表2 线性关系
Tab. 2 Linear relationship

成分 线性范围/μg·mL-1回归方程r拉坦前列素 0.1~2.4A=1.73+73.66C0.999 3 5,6-反式-拉坦前列素 0.1~2.5A=1.63+74.23C0.999 5 15S-拉坦前列素 0.1~2.5A=-0.39+81.03C0.999 9
2.4.4 重复性试验 取批号为Z08325的拉坦前列素滴眼液的样品6份,平行测定6次,杂质5,6-反式-拉坦前列素含量 RSD为 2.2%;拉坦前列素的含量RSD为0.9%,表明重复性良好。
2.4.5 溶液的稳定性 取有关物质供试品溶液,分别于0,3,6,12 h进样测定,结果杂质总量分别为0.87%,0.87%,0.87%,0.88%,12 h内杂质总量没有明显增加;拉坦前列素峰面积分别为792.8,789.3,793.1,799.3,796.8,12 h 内拉坦前列素峰面积基本无变化,表明溶液稳定。
2.4.6 回收率试验 取有关物质供试品溶液适量,平均分成9份,分别加入设计的3个不同浓度的 5,6-反式-拉坦前列素和 15S-拉坦前列素对照品溶液,每个浓度3份,9个测定结果,计算回收率,结果见表3,平均回收率为80%~120%,符合有关物质测定准确度的要求。
按处方比例分别精密称取相当于标示量80%,100%,120%的拉坦前列素对照品及相应量的辅料(苯扎氯铵、苯扎溴铵、吐温80、磷酸氢二钠、磷酸二氢钠和氯化钠),加乙腈适量,振摇使拉坦前列素溶解,照确定的实验方法测定。设计3个不同的浓度进行测定,9个测定结果,计算回收率,结果见表4。可见本法的回收率较高,可用于拉坦前列素的含量测定。
表3 加样回收率测定结果
Tab. 3 Analysis results of recoveries (n=9)
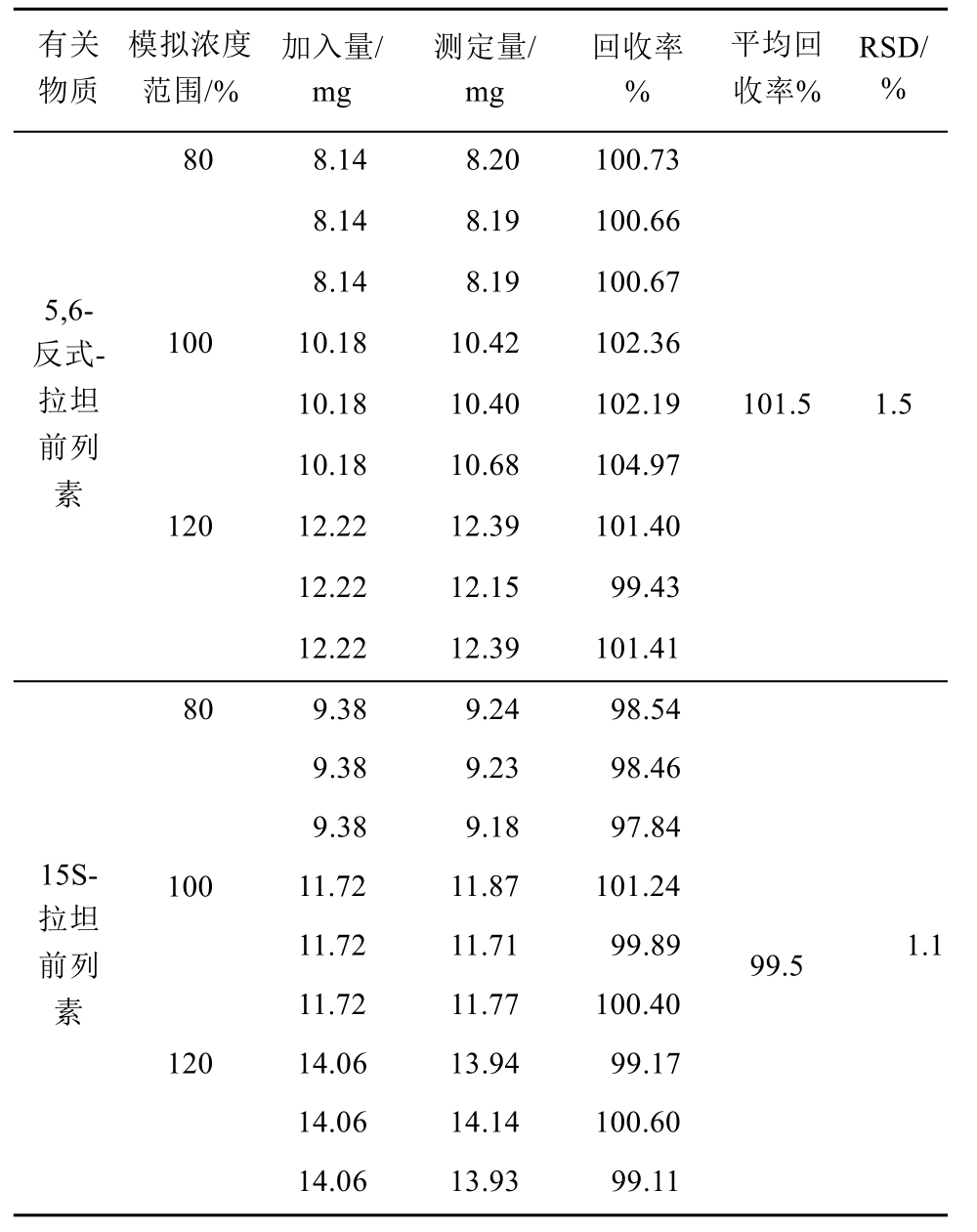
有关物质模拟浓度范围/%加入量/mg测定量/mg回收率%平均回收率%RSD/%80 8.14 8.20 100.73 5,6-反式-拉坦前列素8.14 8.19 100.66 8.14 8.19 100.67 100 10.18 10.42 102.36 10.18 10.40 102.19 10.18 10.68 104.97 120 12.22 12.39 101.40 12.22 12.15 99.43 12.22 12.39 101.41 101.5 1.5 80 9.38 9.24 98.54 15S-拉坦前列素9.38 9.23 98.46 9.38 9.18 97.84 100 11.72 11.87 101.24 11.72 11.71 99.89 11.72 11.77 100.40 120 14.06 13.94 99.17 14.06 14.14 100.60 14.06 13.93 99.11 99.5 1.1
表4 拉坦前列素回收率测定结果(n=9)
Tab.4 Analytical results of latanoprost recoveries (n=9)
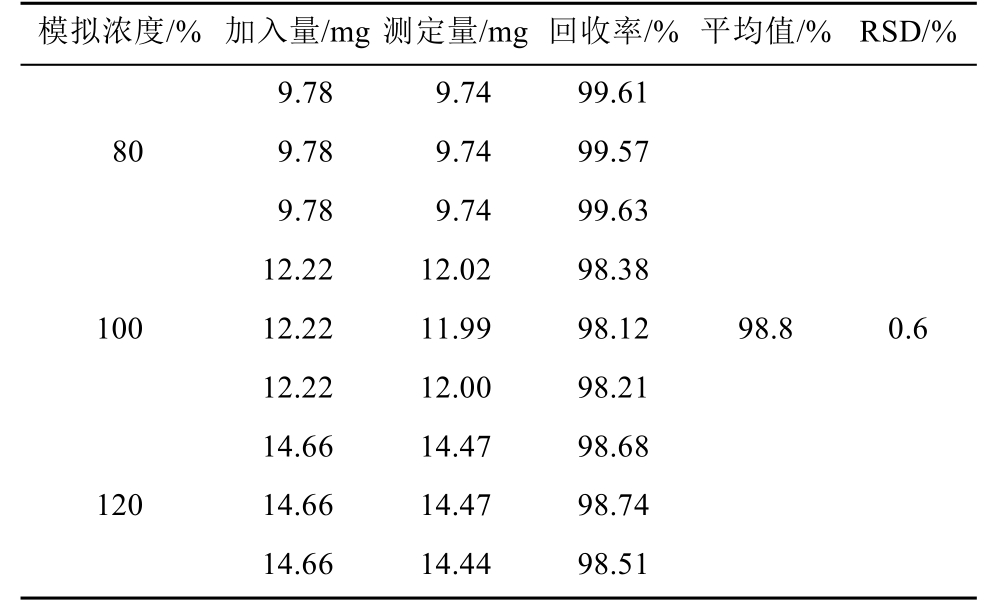
模拟浓度/% 加入量/mg测定量/mg 回收率/% 平均值/% RSD/%9.78 9.74 99.61 809.78 9.74 99.57 9.78 9.74 99.63 100 12.22 12.02 98.38 12.22 11.99 98.12 12.22 12.00 98.21 98.8 0.6 120 14.66 14.47 98.68 14.66 14.47 98.74 14.66 14.44 98.51
3 讨论
本研究综合了各厂家的产品处方,考察了缓冲盐浓度、乙腈比例和柱温对拉坦前列素、苯扎氯铵 C14、吐温 80、5,6-反式-拉坦前列素色谱行为的影响,在拉坦前列素滴眼液原有进口注册标准基础上,改进和优化了色谱条件,使各成分峰间都得到了较好的分离。运用所建立的HPLC,测定了来自国内4个厂家共9批拉坦前列素滴眼液中的有关物质和含量,方法切实可行,结果准确可靠,该方法基本可适用于国内所有厂家生产的拉坦前列素滴眼液的有关物质和含量测定,为该药品质量标准的提高提供了可靠的科学依据和参考。
[1] 赵军梅, 钱军. 拉坦前列素滴眼液治疗青光眼[J]. 中国新药与临床杂志, 2013, 22(1): 38-40.
[2] 张禹华, 于海岩, 宋成君, 等. HPLC 法测定拉坦前列素滴眼液中苯扎氯铵的含量[J]. 中国科技博览, 2010, 22(1):49-50.
[3] 中国药典. 四部[S]. 2015: 通则9101.
[4] WIDOMSKI P, BARAN P, GOŁĘBIEWSKI P, et al.Validated liquid chromatographic method for analysis of the isomers of latanoprost [J]. Acta Chromatogr, 2008, 20(2):157-164.
[5] PAN D J, CHEN Q F, ZHANG J D, et al. Determination of the related substances in Latanoprost Eye drops by NP-HPLC [J].Chin J Pharm(中国医药工业杂志), 2013, 44(9): 932-934.
[6] 郭妍, 殷莉莉, 廉英, 等. 反相高效液相色谱法测定拉坦前列素滴眼液的含量[J]. 中南药学, 2014, 12(5): 475-477
Determination of the Related Substances and Content in the Complex System of Latanoprost Eye Drops by HPLC
CHEN Yue1, WANG Ling2, GAO Fang2, WANG Jian1*(1.Zhejiang Institute for Drug Control, Hangzhou 310052, China;2.Zhejiang Changming Pharmacetical Co., Ltd., Taizhou 317200, China; 3.Zhejiang University of Technology, Hangzhou 310014,China)
ABSTRACT:OBJECTIVE To develop an HPLC method for the determination of the related substances and content in the complex system of Latanoprost Eye drops. METHODS The conditions of detection were Sugar Chiral column C18(250 mm×4.6 mm, 5 µm), related substances measured using the isocratic mobile phase consisted of 0.005 mmol·L-1sodium dihydrogen phosphate (adjust with phosphate to pH 2.7)-acetonitrile(56∶44), and the mobile phase for content determination was 0.005 mol·L-1sodium dihydrogen phosphate solution (adjusted with phosphoric acid to pH 2.7)-acetonitrile(54∶46) with a flow rate of 0.5 mL·min-1, the UV detection wavelength was 200 nm. RESULTS The resolution of 5, 6-trans-Latanoprost and 15S-Latanoprost was good. The method for determination of the related substances of Latanoprost Eye drops had a good linearity.The average recovery of 5,6-trans-Latanoprost and 15S-Latanoprost were 101.5% and 99.5%. The limit of quantitation of Latanoprost, 5,6-trans-Latanoprost and 15S-Latanoprost were 0.12, 0.13 and 0.12 µg·mL-1. The method for determination of Latanoprost Eye drops had a good linearity, the repeatability was good (RSD=0.90%). The average recovery of Latanoprost was 98.8%. CONCLUSION The method is accurate and reliable, which can be used to control the quality of Latanoprost Eye drops.
KEY WORDS:Latanoprost Eye drops; HPLC; related substances; content determination
REFERENCES
中图分类号:R917.101
文献标志码:B
文章编号:1007-7693(2017)12-1743-04
DOI:10.13748/j.cnki.issn1007-7693.2017.12.022
引用本文:陈悦, 王玲, 高芳, 等. HPLC测定拉坦前列素滴眼液复杂系统中的有关物质及含量[J]. 中国现代应用药学,2017, 34(12): 1743-1746.
作者简介:陈悦,男,主任药师 Tel: (0571)86459427 E-mail: 13868057010@163.com*
通信作者:王建,男,主任药师 Tel:(0451)87180358 E-mail: wangjianhw2000@aliyun.com
收稿日期:2017-02-11
(本文责编:曹粤锋)




