钱文慧,王婷,侯忆璠,苏华,白玲玲*
(南京军区南京总医院制剂科,南京 210002)
摘要:目的制定尿素乳膏的质量标准,进一步控制该制剂的产品质量。方法参照中国药典2015年版对尿素乳膏中主要成分尿素进行定性鉴别,同时采用DMAB显色法测定其含量。结果尿素乳膏中尿素鉴别反应呈阳性,尿素含量在0.036 78~0.085 81 mg·ml-1(r=0.999 5)内与吸光度值呈良好的线性关系,平均加样回收率为98.19%,RSD=0.24%(n=9)。结论该法操作简单,准确可靠,能有效控制院内制剂尿素乳膏的质量。
关键词:尿素乳膏;尿素;DMAB显色法;质量标准
尿素乳膏具有滋润皮肤、减少角质增生和增加皮肤角质层的水合作用[1-3],临床主要用于鱼鳞病、手足皲裂及皮肤干燥等症的预防与治疗。传统的尿素乳膏以W/O型基质居多,具有油腻、不易涂布、吸收性差的缺点[4],南京军区南京总医院根据临床需要,按照《中国医院制剂规范》中尿素乳膏的处方及制备方法,配制了O/W型尿素乳膏,该制剂临床疗效较好,被评为南京军区南京总医院的特色外用制剂。为了进一步控制该制剂的产品质量,完善其质量标准,笔者按照全军制剂质量标准提升的要求和中国药典2015年版中含量测定的相关方法[5],摸索并建立了O/W型尿素乳膏的定性和定量方法,以快速全面地控制尿素乳膏的质量。
FA1604S型万分之一电子天平(上海天平仪器厂);AE240型十万分之一电子分析天平(梅特勒-托利多仪器有限公司);UV-1700紫外分光光度计(日本岛津);HH-2型数显恒温水浴锅(国华电器有限公司)。
尿素对照品(中国食品药品检定研究所,批号:100288-200201,纯度:100%,供UV法测定用);尿素乳膏(自制,批号:170105,161226,161101,规格:20 g∶4 g);其余所用试剂均为分析纯,水为纯化水。
本品为白色乳膏。
依据中国药典2015年版二部中尿素“鉴别”项下的方法,建立尿素乳膏中尿素的鉴别方法:取本品2.5 g(约相当于尿素0.5 g),置分液漏斗中,加三氯甲烷50 ml,振摇使分散,加入4%氯化钠溶液,振摇提取,使分层,收集上层水溶液于蒸发皿中,78 ℃蒸去水分。①取适量残渣于试管中缓缓加热,液化并放出臭氨气味,能使湿润的红色石蕊试纸变蓝;继续加热数分钟,冷却,加水10 ml溶解后,加氢氧化钠试液1 ml,混匀,加硫酸铜试液1滴,摇匀,溶液呈蓝紫色。②取适量上述残渣,加水适量,取上清液1 ml,加硝酸1 ml,振摇,生成白色结晶性沉淀。
3批样品均符合乳膏剂项下有关的各项规定(中国药典2015年版四部附录通则0109)。
2.4.1 对照品溶液的制备 精密称取尿素对照品0.25 g,置50 ml量瓶中,加95%乙醇溶解至刻度,摇匀,即得浓度为5.108 mg·ml-1的尿素对照品储备溶液。精密吸取对照品储备液5 ml,置于50 ml量瓶中,加95%乙醇稀释至刻度,摇匀,作为对照品溶液。
2.4.2 供试品溶液的制备 精取本品0.25 g于烧杯中,加95%乙醇20 ml,置80 ℃水浴加热使尿素溶解。移至冰浴中冷却30 min,滤过,滤液置100 ml量瓶中,用95%乙醇洗涤容器及滤器,洗液并入量瓶中,冷却至室温,加95%乙醇稀释至刻度,摇匀,过滤,取续滤液作为供试品溶液。
2.4.3 阴性样品的制备 按处方比例称取硬脂酸1.8 g,十八醇1.8 g,液体石蜡2.7 g,山梨醇酐单硬脂酸酯9.6 g,白凡士林1.8 g,吐温80 1.32 g,甘油3 g,山梨酸0.06 g,按照处方制备工艺制成阴性样品。
2.4.4 显色剂空白对照溶液的制备 精密量取10 ml对二甲氨基苯甲醛溶液置25 ml量瓶中,用95%乙醇稀释至刻度,制备成显色剂空白对照溶液。
2.4.5 测定法 精密量取供试品溶液、对照品溶液及阴性样品溶液各3 ml,分别置25 ml量瓶中;各精密加入对二甲氨基苯甲醛溶液(取对二甲氨基苯甲醛2 g,加乙醇96 ml与盐酸4 ml使溶解即得)10 ml,用95%乙醇稀释至刻度,摇匀,置暗处放置15 min。以显色剂空白对照溶液调零,在420 nm处分别测定吸光度,计算,即得。
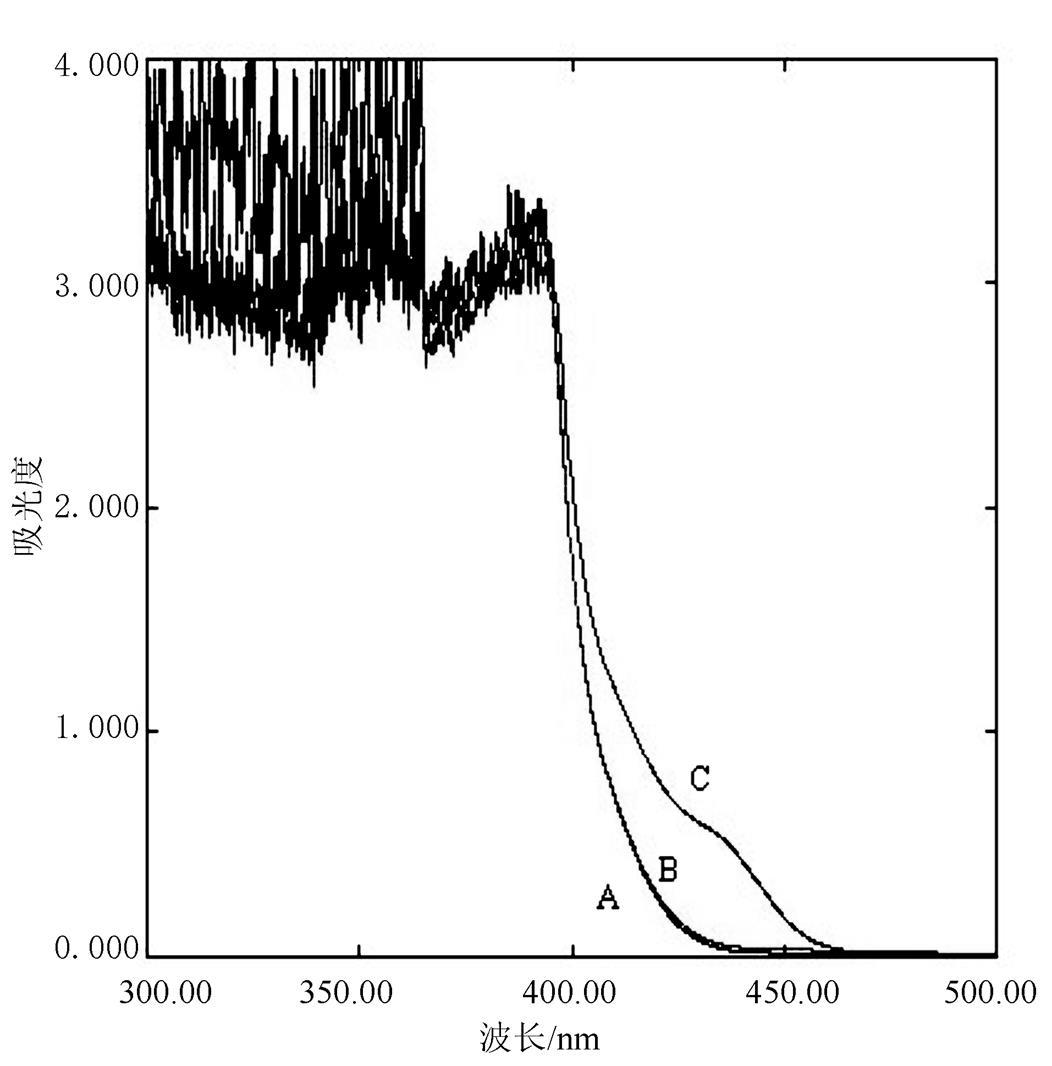
2.4.6 光谱专属性的考察 按处方比例和供试品制备工艺不加尿素制成阴性对照,按“2.4.2”项下供试品溶液的制备方法制成阴性对照溶液。将“2.4.2”项下样品溶液、“2.4.3”项下阴性溶液、“2.4.4”项下显色剂空白对照溶液按照“2.4.5”项下的测定法显色,最后分别以95%乙醇为空白,在300~500 nm内进行波长扫描。结果显示,以95%乙醇溶液为空白,尿素样品溶液在420 nm波长处吸收值范围(0.5~0.8)合适,适合用作紫外定量;显色剂空白对照溶液与阴性对照溶液的紫外吸收图谱几乎一致,虽然两者在420 nm波长处存在略微吸收,但是测定时如果以显色剂空白对照溶液调零做空白则可以消除吸收值的干扰。故中国药典2015年版及相关文献[5-7],选定在420 nm处测定显色衍生物的吸光度,光谱图见图1。

图1 尿素乳膏的紫外吸收图谱
A-显色剂空白对照溶液;B-阴性对照溶液;C-尿素样品溶液。
Fig. 1 Ultraviolet absorption spectrum of Urea cream
A-colour-developer control; B-negative sample; C-test sample.
2.4.7 标准曲线的制备 精密量取“2.4.1”项下尿素对照储备液3.0,4.0,5.0,6.0,7.0 ml,分别置于50 ml的量瓶中,用95%乙醇稀释至刻度,摇匀,按“2.4.5”项下方法稀释浓度进行显色反应,在420 nm波长处测定,以对照品浓度为横坐标(X),紫外吸光度值为纵坐标(Y),进行线性回归,得到回归方程Y=8.288 5X-0.017 5,r=0.999 5(n=5)。结果表明,尿素的浓度在0.036 78~0.085 81 mg·mL-1内与吸光度值呈良好的线性关系。
2.4.8 仪器精密度试验 取“2.4.1”项下的尿素对照品溶液,按“2.4.5”项下衍生化显色方法操作,连续6次测定其吸光度值,尿素含量测得值的RSD为0.44%。结果表明该方法的精密度良好。
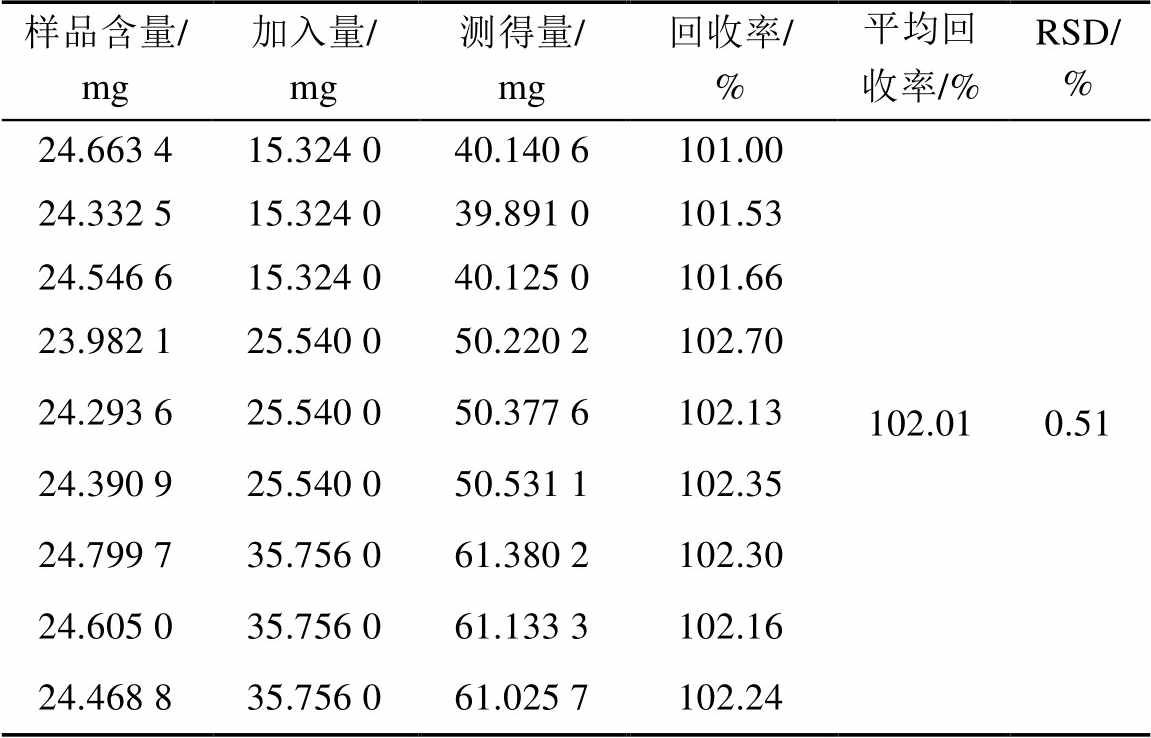
2.4.9 加样回收率试验 精密称取已知含量的样品0.125 g(批号为170105),共 9份,置于烧杯中,加95%乙醇20 ml,置80 ℃水浴加热使尿素溶解。移至冰浴中冷却30 min,滤过,滤液置100 ml 量瓶中,分别精密加入尿素储备液3,5,7 ml,加乙醇稀释至刻度,摇匀,过滤。按“2.4.5”项下样品制备方法衍生化反应,以显色剂空白对照溶液调零,在420 nm处分别测定吸光度,计算回收率。经计算,尿素含量平均回收率为102.01%,RSD为0.51%。结果见表1。
表1 尿素加样回收率试验测定结果(n=9)
Tab. 1 Results of recoveries of urea(n=9)
2.4.10 重复性试验 取同一批号(批号为170105)的样品6份,按“2.4.2”项下方法制备供试品溶液,并进行显色测定,尿素含量测得值的RSD为0.28%。说明方法重复性良好。
2.4.11 样品含量测定 取3批尿素乳膏,按“2.4.2”项下方法制备供试品溶液,依法测定。结果见表2。
表2 尿素含量测定结果(n=3)
Tab. 2 Results of content determination of Urea cream(n=3)

关于尿素的含量测定方法,目前文献报道的有酶解法、对二甲氨基苯甲醛法、HPLC、甲醛法等[8-11],考虑到本制剂为医院制剂,本着快速检验、安全适用的原则,最终选定采用对二甲氨基苯甲醛显色法来测定尿素的含量。尿素为碳酰胺结构,其分子中的酰胺键在酸性条件下与对二甲氨基苯甲醛发生缩合反应,生成黄色的对二甲氨基苯缩脲衍生物,通过测定该衍生物在一定波长下的吸光度值来定量溶液中尿素的含量。该检测方法操作快速、简便,符合中国药典中相关含量测定的要求。因此,笔者参考药典及相关文献[3,5,12-14]制定了其质量标准,并对该含量测定方法进行了优化和验证,以期为临床安全使用提供参考和依据。
该院研制的尿素乳膏为O/W型基质,在冷乙醇液中不易溶解,故需采用加热破乳的方式提取出有效成分。又因尿素易溶于水,水溶液高温受热即可引起尿素的水解,因此提取温度又不宜过高。笔者比较了不同破乳温度(60,80,100 ℃)对尿素含量的影响,发现提取温度为80 ℃时尿素含量最高,提取也较完全;60 ℃时样品中存在少量白色漂浮物,可能油相未完全溶解;100 ℃时测得的样品含量比80 ℃时略微减少,样品可能存在少量水解。因此,制备样品溶液时最适水浴温度为80 ℃,样品提取较完全。
当以95%乙醇为空白,在300~500 nm范围内进行全波长扫描时,从吸收曲线上看,显色剂的空白对照溶液本身在400~440 nm波长处就存在部分吸收,但接近440 nm处其吸收值逐渐减小。单从空白对照溶液的吸光度值考虑的话,波长437 nm最合适[15],该波长处空白对照溶液的吸光度几乎为零,而波长420 nm处空白溶剂的吸光度值则较大;但从样品溶液的吸光度值考虑的话,437 nm波长处时样品溶液的吸光度值也降低了,并且达不到测定紫外吸收值的最佳范围(0.5~0.8)。因此,笔者参考药典及相关文献[5-7],采用420 nm作为最佳检测波长,该波长处样品溶液的吸光度值较合适,本底显色剂的干扰也可通过空白调零来消除。
本实验采用显色法进行定量,因尿素与对二甲氨基苯甲醛缩合反应生成的苯缩脲衍生物不稳定,所以样品的取用量、显色剂加入量、反应时间等因素都会影响含量测定的结果及方法学的精密度。笔者首先研究了不同供试品溶液的取用量对吸光度值的影响,供试品溶液分别取1,3,5 ml时,随着样品溶液体积的增加,衍生物的吸光度值也呈线性增加。当供试品溶液取样体积为3 ml时,衍生物的吸光度值在0.5左右,满足UV检测的灵敏度要求,因此供试品液取样3 ml较合适;同理,笔者研究了不同显色剂加入量(5,10,15 ml)对吸光度值的影响,发现增加显色剂的用量,样品吸光度值也随之增加,本着适量取样与保证检测灵敏度的原则,确定对二甲氨基苯甲醛在25 ml体系内用量为10 ml是最合适的。最后,笔者考察了反应时间对吸光度值的影响,分别在加入对二甲氨基苯甲醛后每隔5 min测定样品溶液的吸光度值,从实验结果看,10 min内显色反应已基本完成,吸光度值已趋于稳定;在10~25 min内溶液的吸光度值虽有略微增加,但是波动不大,比较稳定;在25~40 min内溶液的吸光度值仍在不断上升。因此,参考药典及相关文献[3,5-6],确定该显色反应的最佳检测时间为15 min,必须在25 min内完成测定。另外,本实验采用的对二甲氨基苯甲醛试液必须临用现配、一次用完才能保证每次实验结果的准确性。采用显色法进行含量测定,必须考察显色实验的影响因素,从而来减少实验误差,提高含量测定的准确性和重复性。本方法操作简单快速,能够有效地控制尿素乳膏的质量。
REFERENCES
[1] HUANG J, ZHANG Y. Study on quality specification for Urea ointment [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2014, 31(4): 441-444.
[2] 袁琴芳, 邹静瑶, 庄晓庆. 尿素霜对烧伤康复期患者皮肤护理的疗效观察[J]. 中国误诊学杂志, 2008, 8(29): 7103-7104.
[3] OU J B, SHI Y H, ZHU H, et al. Improvement of quality control of Runfu lotion [J]. Pharm Today(今日药学), 2016, 26(2): 107-109.
[4] 陈燕华, 刁雨辉. 比色法测定尿素乳膏的含量[J]. 江苏药学与临床研究, 2002, 10(3): 17-18.
[5] 中国药典. 二部[S]. 2015: 531, 1202, 附录ⅪⅩA.
[6] Chen F, Chang M q, Wang G, et al. Determination of carbamide contents of Compound Rhizoma Bletillae cream by spectrophotometer [J]. J Pediatric Pharm(儿科药学杂志), 2012, 18(6): 45-46.
[7] 徐凤梅. 紫外分光光度法测定尿素乳膏含量[J]. 天津药学, 2002, 14(2): 61-62.
[8] 刘炜, 孙颖, 曾蔚欣, 等. 紫外分光光度法测定尿素乳膏中尿素的含量[J]. 天津药学, 2011, 23(6): 19-21.
[9] LIU D, LI Z P, WU L M, et al. Determination of urea in compound urea cream by RP-HPLC [J]. Pharmacy Today(今日药学), 2015, 25(4): 266-267.
[10] 王美兰, 贺萍, 许卉, 等. 甲醛法测定尿素总氮含量的若干问题[J]. 大学化学, 2002, 17(6): 35-37.
[11] 余爱霞, 缪佳文. 酶电极法测定医院制剂尿素乳膏中尿素的含量[J]. 中国药事, 2004, 18(9): 565-566.
[12] Long F, Peng X d, Tang Z l, et al. Preparation and quality control of cyproheptadine and Urea Facial cream [J]. China Pharm(中国药业), 2015, 24(4): 19-20.
[13] XU Y, YU J J, LIANG K L, et al. Study on quality standard of Compound Camphor extract [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2017, 34(4): 496-499.
[14] LIAO X, QIAO L Y, WANG Y J, et al. Determination of arietic acid, emodin, chrysophanol and triptolide in Shenyanning tablets by HPLC [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2017, 34(4): 567-570.
[15] 吴红英. 尿素乳膏含量测定方法的改进[J]. 中国药师, 2012, 15(1): 131-132.
(本文责编:曹粤锋)
Study on the Quality Standard for Urea Cream
QIAN Wenhui, Wang Ting, Hou Yifan, SU Hua, Bai Lingling*
(Department of Preparation Division, Nanjing General Hospital, Nanjing 210002, China)
ABSTRACT:OBJECTIVETo establish and improve the quality standard of Urea cream.METHODSThe effective constituent of Urea creamwere qualitative identified according to the methods in Chinese Pharmacopoeia (2015 edition) and its content was determined by DMAB color-test.RESULTSThe qualitative identifications of urea were specific. The liner range of urea was 0.036 78-0.085 81 mg·ml-1(r=0.999 5), its average recovery were 98.19% and RSD was 0.24%(n=9).CONCLUSIONThe method is simple and practical, the result is accurate and reliable and it can be used to control the quality of Urea cream.
KEY WORDS:Urea cream; urea; DMAB; quality standard
中图分类号:R943.3
文献标志码:B
文章编号:1007-7693(2017)11-1564-04
DOI:10.13748/j.cnki.issn1007-7693.2017.11.014
引用本文:钱文慧, 王婷, 侯忆璠, 等. 尿素乳膏的质量标准研究[J]. 中国现代应用药学, 2017, 34(11): 1564-1567.
基金项目:军队医疗机构制剂标准提高科研专项课题重点项目(14ZJZ08)
作者简介:钱文慧,女,硕士,药师 Tel: (025)80863161 E-mail: woshiqwh@163.com
*通信作者:白玲玲,女,药师 Tel: (025)80860163 E-mail: bailingbaobei@126.com
收稿日期:2017-07-12