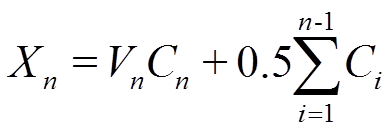 ,式中:Xn为取样点时黄芩甲苷的剩余药量(mg);Vn为取样点时供试液的体积(ml);Cn为取样点时供试液中黄芩甲苷的浓度(mg·L-1)。
,式中:Xn为取样点时黄芩甲苷的剩余药量(mg);Vn为取样点时供试液的体积(ml);Cn为取样点时供试液中黄芩甲苷的浓度(mg·L-1)。陈力1,李静1,蒋斌2*
(1.成都医学院第一附属医院,成都 610500;2.成都倍特药业有限公司,成都 610041)
摘要:目的研究黄芪甲苷配伍冰片前后在大鼠小肠的吸收情况。方法采用大鼠原位肠循环灌注实验法研究黄芪甲苷配伍冰片前后体内吸收动力学的具体变化。结果黄芪甲苷在5~20 mg·kg-1内的吸收动力学参数无显著性差异;2.5 mg·kg-1冰片与黄芪甲苷配伍前后的动力学参数无显著性差异,而5,10 mg·kg-1冰片配伍前后有显著性差异(P<0.01),但5,10 mg·kg-1剂量组之间的动力学参数差异不显著。结论冰片在一定的剂量范围内可促进黄芪甲苷在大鼠小肠内的吸收,可与黄芪甲苷配伍应用以提高生物利用度。
关键词:冰片;黄芪甲苷;体内吸收;肠循环
黄芪为一种常用中药,为豆科植物膜荚黄芪Astragalus membranaceus和蒙古黄芪Astragalusmembranaceus(Fisch.) Bge. var.mongholicus (Beg.) Hsiao的干燥根。黄芪甲苷是黄芪药理活性的主要物质之一[1-2],药理学研究表明黄芪甲苷具有镇静、镇痛、降压消炎、影响肝脏蛋白质合成和促进自然杀伤细胞活性等作用[3-4]。但由于其具有较高的分子量和低水溶性,在体内的膜通透性差,生物利用度低[5],在一定程度上限制了它的临床应用。因此,探求能提高黄芪甲苷生物利用度的有效用药方式有着重要的意义。
冰片为龙脑科植物龙脑香树脂的加工品[6]。据《本草纲目》记载,冰片具有“通诸窍、散郁火”的功效。在临床配伍应用中,主要发挥促进药物透过生物屏障,以提高其他药物的生物利用度的作用[7-11]。
本研究的目的在于采用大鼠原位肠循环灌注实验研究冰片配伍黄芪甲苷前后的肠吸收动力学特性,进一步了解冰片对黄芪甲苷在胃肠道内吸收的促进作用,为黄芪甲苷的临床配伍应用等提供参考。
黄芪甲苷对照品(中国食品药品检定研究院,批号:110781-201605,纯度>99%);黄芪(产地为内蒙古多伦,野生,经成都中医药大学韩丽教授鉴定为豆科植物膜荚黄芪Astragalus membranaceus(Fisch.)的根茎;冰片(国药集团化学试剂有限公司,批号:110749-201602,纯度:99.5%);酚红(国药集团化学试剂有限公司,批号:20160320);Waters e2695高效液相色谱系统(由四元泵,自动进样器,自动脱气装置,紫外可见光检测器等构成,美国Waters公司);BT01-DG2型蠕动泵(天津市协达伟业电子有限公司);乙腈为色谱纯,其余试剂为分析纯,水为注射用水;清洁级SD大鼠购自四川大学华西动物中心,体质量(200±20)g,动物许可证号:SCXH(川)2016-05。
2.1.1 黄芪甲苷制备 取黄芪药材,切细后用粉碎机打成粉,称重。置具塞锥形瓶中,加氨试液,振摇使其充分润湿,再加入正丁醇,密塞,超声处理(功率600 W,33 kHz)15 min,静置分层,倾出上层正丁醇液,下层再加入正丁醇,同法再处理1次,合并2次正丁醇液,滤过,滤液用水洗涤2次,弃去水液,将正丁醇液蒸干,即得。
2.1.2 黄芪甲苷含量测定 采用HPLC检测[12],色谱条件为Zorbax SB C18色谱柱(150 mm×4.6 mm,3.5 μm);流动相:乙腈-水(35∶65);流速:1.0 ml·min-1;柱温:30 ℃;ELSD检测器漂移管温度110 ℃,气流速度2.5 L·min-1。测得自制样品黄芪甲苷(批号:20161201)含量为75.2%。
取实验前禁食12 h(自由饮水)的SD大鼠,于腹腔注射戊巴比妥钠(30 mg·kg-1),麻醉后将其固定。沿大鼠腹中线打开腹腔约2.5 cm,然后结扎胆管,在实验肠管的两端各切一小口,并在上端小口处插入直径为0.3 cm的玻璃管,用线扎紧。用注射器将(37±0.5)℃的生理盐水缓缓注入肠管内,洗去肠管内容物至干净。然后在实验肠管的下端小口处也插入玻璃管,用线扎紧。将肠管两端的玻璃管与蠕动泵的胶管连接,形成回路,开启蠕动泵,以5 mL·min-1的流速循环10 min,随后将流速调至2.5 mL·min-1,立即从装有灌注液的锥形瓶中取样0.5 mL,作为零时间药物浓度和酚红浓度的测定样品,同时向锥形瓶中补加酚红Kreb-Ringer’s试液(K-R试液)0.5 mL。其后亦按同法每隔15 min取样并补加酚红K-R液,循环3 h后中止实验。
2.3.1 K-R试液(pH 7.4) 称取NaCl 7.80 g,HCl 0.35 g ,NaHCO31.37 g,NaH2PO30.32 g,MgCl20.02 g,葡萄糖1.40 g,加纯化水定容成1 000 mL,即得。
2.3.2 黄芪甲苷试液 分别准确称取黄芪甲苷样品(10.00,20.00,40.00 mg)和酚红20.00 mg,用K-R试液定容稀释至1 000 mL。
2.3.3 黄芪甲苷、冰片试液 分别准确称取黄芪甲苷20 mg、冰片(5.00,10.00,20.00 mg)和酚红20.00 mg,用K-R试液定容稀释至1 000 mL。
2.3.4 空白肠循环灌注液 按“2.2”项下方法,用K-R试液进行循环3 h,中止试验,得空白肠循环灌注液。
2.3.5 混合对照品储备液 精密称定黄芪甲苷对照品10.24 mg、酚红对照品10.09 mg,置100 mL量瓶中,用K-R试液稀释定容,于4 ℃冷藏保存,作为混合对照品储备液。
2.3.6 混合对照品标准曲线试液 分别精密量取混合对照品储备液适量,用K-R试液稀释成混合对照品标准曲线试液,使得黄芪甲苷浓度为0.51~10.24 mg·L-1,酚红浓度为0.50~10.09 mg·L-1。
取30只SD大鼠,随机分为6组,按“2.2”项下方法,结扎胆管,然后自十二指肠上部及回肠末端分别插管,用“2.3”项下配制的“黄芪甲苷试液”3个剂量和“黄芪甲苷、冰片试液”3个剂量分别进行原位肠循环灌注实验,每个剂量循环初体积为100 mL,定时取样。
取循环样品供试液,用1 mL甲醇稀释,涡旋1 min,15 000 r·min-1离心5 min,取上清液10 μL进样,记录色谱图,采用线性回归方程计算肠循环液中黄芪甲苷和酚红的浓度。
2.5.1 不同时间供试液体积计算公式Vn=[(Vn-1-0.5)×Cn-1+0.5C0]/Cn,式中:Vn为该次取样时供试液的体积(ml);Vn-1为前一次取样时供试液的体积(ml);Cn为该次取样时供试液中酚红的浓度(mg·L-1);Cn-1为前一次取样时供试液中酚红的浓度(mg·L-1);C0为补液中酚红的浓度(mg·L-1)。
2.5.2 不同时间灌流液中剩余药量计算公式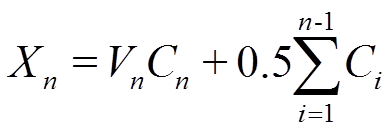 ,式中:Xn为取样点时黄芩甲苷的剩余药量(mg);Vn为取样点时供试液的体积(ml);Cn为取样点时供试液中黄芩甲苷的浓度(mg·L-1)。
,式中:Xn为取样点时黄芩甲苷的剩余药量(mg);Vn为取样点时供试液的体积(ml);Cn为取样点时供试液中黄芩甲苷的浓度(mg·L-1)。
2.5.3 吸收参数计算 根据量瓶中药物初始浓度药量和终末药量之差与循环时间的比值计算每小时的吸收率,即吸收率=(初始浓度×初始体积-终浓度×终体积)/循环时间。根据Fick方程原理计算药物的吸收参数。采用Oneway ANO-VA的S-N-K和LSD检验对数据进行分析,比较甲苷黄芪及配伍冰片后各组的肠吸收参数(吸收半衰期t1/2,吸收速率常数Ka和每小时吸收率A%)是否有统计学差异。
2.6.1 色谱条件 Ultimate C18色谱柱(4.6 mm×250 mm,5 μm),流动相为乙腈-水(35∶65),流速为1.0 mL·min-1,柱温30 ℃,检测波长为203 nm。
2.6.2 专属性考察 分别取空白肠循环灌注液、混合对照品溶液(5.12 mg·L-1黄芪甲苷,5.05 mg·L-1酚红)、肠循环灌注液样品,在“2.6.1”条件下,进样10 μL,记录色谱图,考察空白灌流液对样品的检测是否有干扰。
2.6.3 线性关系考察 取混合对照品系列工作液,在“2.6.1”色谱条件下,进样10 μL,以色谱峰面积(A)为纵坐标,浓度(C)为横坐标,绘制标准曲线。
2.6.4 精密度测定 日内精密度:分别吸取高、中、低3个浓度的混合对照溶液,在“2.5.1”色谱条件下进样10 μL,每个样品重复进样5次,并根据线性回归方程计算各对照品浓度,计算RSD。日间精密度:分别在第1,2和3天吸取高、中、低3个不同浓度的混合对照溶液,在“2.6.1”色谱条件下,重复进样5次,根据线性回归方程计算各样品浓度,计算RSD。
2.6.5 稳定性考察 准确吸取10 mL黄芪甲苷与酚红在K-R试液和肠循环灌注液的样品,置37 ℃恒温水浴锅内,分别于0,1,3,6 h取样检测样品,比较含量的变化情况。另取灌肠循环后的黄芪甲苷与酚红样品,在用甲醇处理后,室温放置0,4,8,12,24 h后取样检测样品的含量变化情况。
2.6.6 回收率测定 分别取混合对照品储备液不同体积,置10 mL量瓶中,用空白K-R试液与甲醇(1∶2)的混合溶液稀释定容,摇匀,得高、中、低3个浓度的对照品工作液,每个浓度各配制3份。在“2.6.1”色谱条件下进样10 μL,记录色谱图与峰面积,根据回归方程计算各样品浓度。以测定的浓度与样品浓度之比计算回收率。
取黄芪甲苷试液和黄芪甲苷+冰片试液,按“2.4”和“2.5”项下方法进行原位肠循环灌注实验,计算黄芪甲苷各组的肠吸收参数:吸收速率常数(Ka),吸收半衰期(t1/2)和每小时吸收率(A/%)。
3.1.1 专属性 黄芪甲苷和酚红HPLC的专属性考察结果见图1。结果表明,酚红、黄芪甲苷的保留时间分别为3.51和6.49 min。肠循环灌注液样品中2种物质的保留时间与混合对照品中的一致,供试液中其他成分在色谱条件下不干扰测定,表明该色谱条件专属性良好。
3.1.2 线性关系 采用“2.6.1”项下色谱条件测定的黄芪甲苷和酚红线性关系良好,其中黄芪甲苷的回归方程:A=26 070C+1 593.9(r=0.998 9),定量浓度范围为0.51~10.24 mg·L-1,酚红的回归方程为A=10 439.15C-218.09(r=0.999 5),定量浓度范围为0.50~10.09 mg·L-1。
3.1.3 精密度 日内精密度结果显示:黄芪甲苷和酚红的高、中、低浓度的RSD分别为0.95%,0.76%,1.03%和0.52%,0.83%,0.94%。日间精密度:黄芪甲苷和酚红的高、中、低浓度含量的RSD分别为0.74%,0.96%,1.07%和1.01%,1.33%,1.04%。日内和日间精密度的结果均表明了该方法重复性良好。
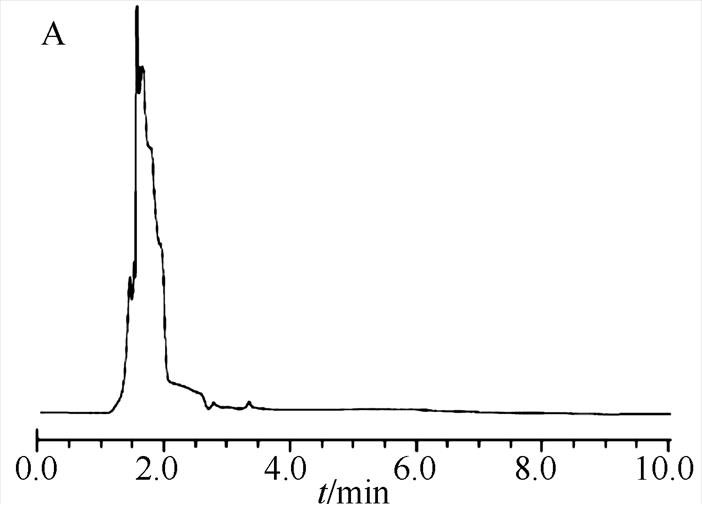
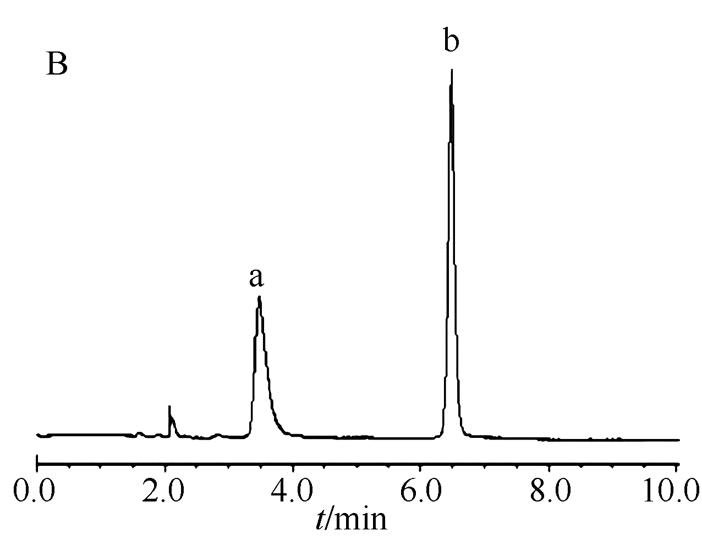
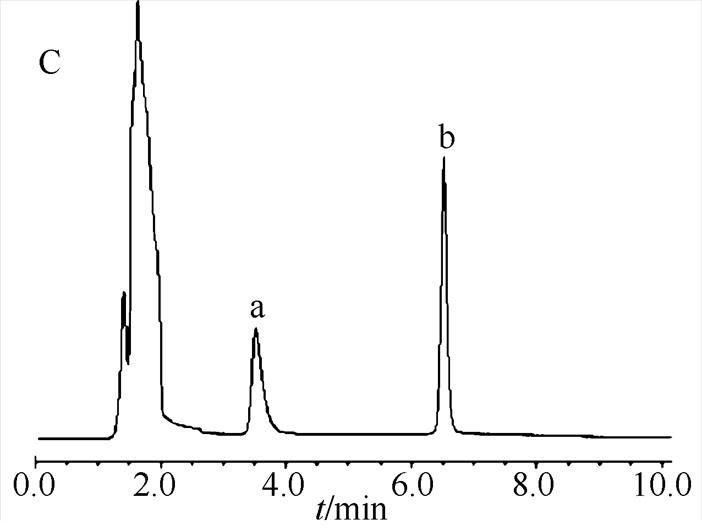
图1 专属性考察色谱图
A-空白肠循环液;B-混合对照溶液;C-肠循环样品溶液;a-酚红;b-黄芪甲苷。
Fig. 1 HPLC chromatograms of exclusive investigation
A-blank intestinal circulation fluid; B-mixed control solution; C-intestinal circulation sample solution; a-phenol red; b-astragaloside Ⅳ.
3.1.4 稳定性 黄芪甲苷与酚红在K-R试液和肠循环灌注液的样品在37 ℃条件下,0~6 h内的样品含量稳定,RSD<0.85%。灌肠循环后的黄芪甲苷与酚红样品在常温条件下24 h内的含量稳定,RSD为1.73%。
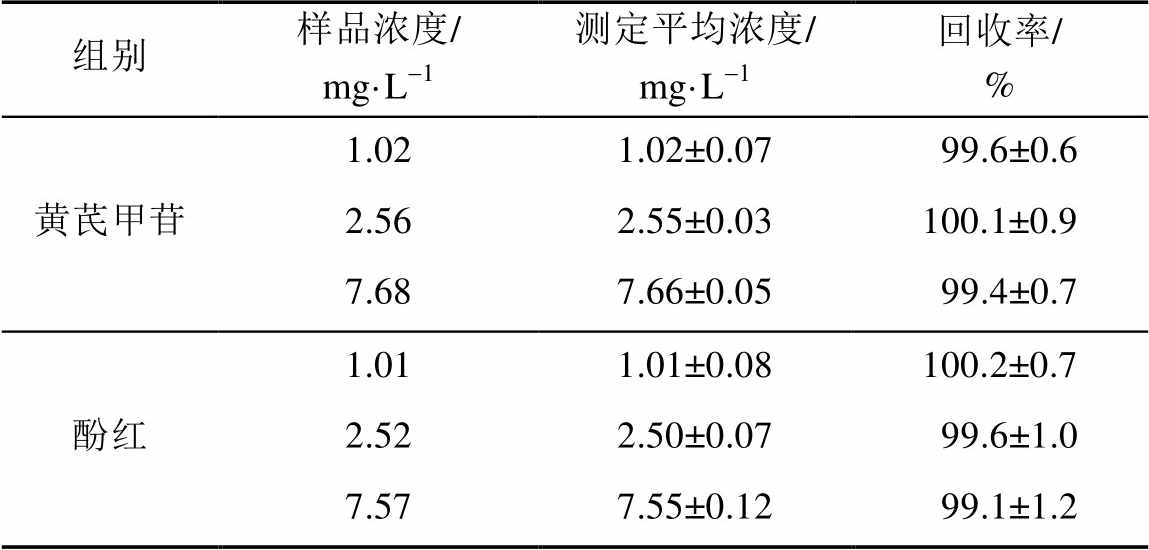
3.1.5 回收率 黄芪甲苷与酚红的混合样品在高、中、低3个浓度条件下的回收率检测结果见表1,各样品的回收率均在99%~101%之间,表明该方法的准确度高。
表1 黄芪甲苷和酚红样品回收率测定结果(n=3,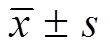 )
)
Tab. 1 Results of recovery experiment of astragaloside IV and borneol(n=3,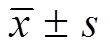 )
)
黄芪甲苷及配伍不同浓度冰片前后在大鼠小肠吸收的实验结果见表2~3。由表2可知,黄芪甲苷在5~20 mg·kg-1内的吸收动力学参数Ka、t1/2和A均无显著性差异;比较冰片与黄芪甲苷配伍前后的肠吸收参数可知,2.5 mg·kg-1冰片组配伍前后并无显著性差异,而5,10 mg·kg-1冰片组配伍前后有显著性差异(P<0.01),但当冰片的浓度增加到10 mg·kg-1时,与5 mg·kg-1冰片浓度相比,肠吸收参数并未进一步显著的增加,表明了冰片对黄芪甲苷在肠道内的吸收能发挥促进作用,其作用大小与浓度有关,呈非线性关系。
表2 黄芪甲苷不同剂量组吸收参数(n=5,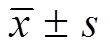 )
)
Tab. 2 Absorption parameters of Astragaloside IV in different dose(n=5,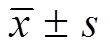 )
)

表3 黄芪甲苷中剂量组与配伍不同剂量冰片组吸收参数(n=5,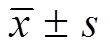 )
)
Tab. 3 Absorption parameters of Astragaloside IV in middle dose treated with different dose of borneol(n=5,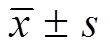 )
)

注:与冰片0 mg·kg-1组比较,1)P<0.01;与冰片2.5 mg·kg-1组比较,2)P<0.01。
Note: Compared with borneol 0 mg·kg-1group,1)P<0.01;compared with borneol 2.5 mg·kg-1group,1)P<0.01.
目前,提高口服药物生物利用度的途径有很多,包括增加药物的水溶性,抑制肠黏膜载体转运和抑制肠道的代谢等,而多种药物之间的配伍应用也是常用的手段之一,特别是对于体内生物利用度低的药物,可通过与促渗透剂等的应用,从而提高药物在体内的吸收。
本实验采用大鼠原位肠循环灌注模型研究了黄芪甲苷配伍冰片前后在肠道内吸收的动力学变化情况。在大鼠原位肠循环灌注实验中,由于肠道水分的吸收可能会导致循环液体积产生变化,故采用在肠道几乎不吸收的酚红来计算循环液的体积,并以此对药物的浓度进行校正,确保检测的数据更准确。
本实验中,在未与冰片配伍的结果中,黄芪甲苷在肠道内的吸收并未随给药浓度的增大而略有增加,浓度在5~20 mg·kg-1内并无显著性差异,表明黄芪甲苷在小肠内的吸收不受自身浓度的影响,可推测黄芪甲苷在大鼠肠道内主要以被动扩散的方式吸收。与不同浓度的冰片配伍后,黄芪甲苷的吸收有不同程度的提高,特别是在5,10 mg·kg-1时能显著提高黄芪甲苷的吸收,表明了冰片在一定的剂量范围内能促进黄芪甲苷在大鼠小肠内的吸收,具有潜在的提高黄芪甲苷生物利用度的作用。本实验即在肠道吸收的层面初步探究了冰片“佐使则有功”的生物学特性,与文献[7-10,15-16]报道的冰片可促进药物各种生物屏障的结果一致,该研究结果提示冰片可考虑作为提高黄芪甲苷生物利用度的配伍药物之一,其具体的促吸收机制有待进一步研究。
REFERENCES
[1] 贾贞超, 陈锦瑶, 张立实. 黄芪甲苷的药理作用与毒理学评价研究进展[C]//中国环境诱变剂学会风险评价专业委员会全国委员会议—低碳生活与健康损害论坛. 2011: 116-120.
[2] SONG Sg, TIAN J, RAO Xl, et al.Anti-hepatic fibrosis effects of astragalosides on carbon tetrachloride-induced hepatic fibrosis in rats [J]. Pharmacy Today(今日药学),2015, 25(3): 176-178, 182.
[3] 林琦, 陆阳, 陈泽乃. 黄芪属植物皂苷类成分研究进展[J]. 国外医药. 植物药分册, 2002, 417(4): 143.
[4] ZHOU Q. Process of the anti-apoptotic mechanism of astragaloside Ⅳ [J] . Chin J Mod Appl Pharm(中国现代应用药学), 2017, 34(5): 783-788.
[5] GU Y C, WANG G J, PAN G Y, et al. Transport and bioavailability studies of astragalosode Ⅳ, an active ingredient in radix astragali [J]. Basic clin Pharmacol Toxicol, 2004, 95(6): 295-298.
[6] 周小雅. 中药冰片的药理研究[J]. 中国现代应用药学, 1998, 15(3): 17-18.
[7] Cheng G, Wu S R, Feng Y. Studies on the effects of borneol on the pharmacokinetics of rifampicin [J]. J Shenyang Pharm Univ, 2001, 18(6): 398-401.
[8] CHEN R L, ZHAO Z G, ZHANG X H, et al. Effect of borneol on sodium valproate passing blood-brain barrier [J]. Chin J Rehabil Theor Pract(中国康复理论与实践), 2007, 13(2): 151-153.
[9] XU B L, WANG H, XU W M, et al. Enhancing effect of synthetic borneol on skin permeation of ligustrazine hydrochloride [J]. Chin Tradit Pat Med(中成药), 2001, 23(12): 864-867.
[10] 樊岚岚, 陆丽珠. 冰片促秦皮甲素透过兔角膜上皮细胞实验研究[J]. 中国中药杂志, 2003, 28(1): 81-82.
[11] Wu S R, Cheng G, Feng Y. Progress in studies on pharmacology of borneol [J] . Chin Tradit Herb Drugs(中草药), 2001, 32(12): 230-233.
[12] CHEN Y G, XIN M T, YANG B, et al. Improved method for determination of astragaloside Ⅳ in radix astragali [J]. Chin J New Drugs(中国新药杂志), 2008, 17(21): 1857-1859.
[13] Ping Q N. Pharmaceutical Experiment and Guidance [M]. Beijing: China Medico-Pharmaceutical Science and Technology Publishing House, 1998: 214-222.
[14] Tamota K, Takaichi A, Kichiro K. Absorption and excretion of drugs: some pharmacokinetic aspects of absorption and excretion from rat small intestine [J]. Chem Pharm Bull, 1964, 12: 421-427.
[15] LI G, FANG C. Review of biological methods of drug intestinal absorption [J]. Chin Pharm J(中国药学杂志), 2002, 37(10): 726-729.
[16] ZENG A G, CHENG X Y, WANG Y C, et al. Influence of penetration enhancer on transdermal permeation of berberine hydrochloridein vitro[J]. J Xi'an Jiaotong Univ (Med Sci)(西安交通大学学报: 医学版), 2004, 25(4): 359-362.
(本文责编:曹粤锋)
Promoting effects of Borneol on the Absorption of Astragaloside Ⅳin vivo
Chen Li1, Li Jing1, Jiang Bin2*
(1.The first affliated hospital of chengdu medical college, Chengdu 610500, China; 2.Brilliant pharmaceutical co., Ltd. of Chengdu, Chengdu 610041, China)
ABSTRACT:OBJECTIVETo study the absorption of astragaloside Ⅳ in the small intestine before and after the combination application of borneol.METHODSThe changes of absorption kinetics of astragaloside Ⅳ inoculated with borneol were studied by in situ intestinal perfusion in rats.RESULTSThere was no significant difference in the absorption kinetics parameters of astragaloside Ⅳ in the concentration range of 5~20 mg·kg-1. There was also no significant difference in the kinetics parameters between astragaloside Ⅳ and astragaloside Ⅳ combined with 2.5 mg·kg-1borneol. While there was significant difference of absorption kinetics before and after being combined with 5 mg·kg-1and 10 mg·kg-1borneol(P<0.01). But there was no significant difference in the kinetic parameters between 5 mg·kg-1and 10 mg·kg-1borneol group.CONCLUSIONBorneol can promote the absorption of astragaloside Ⅳ in the small intestine in a certain dose range. It can be used in combination with astragaloside Ⅳ to improve the bioavailability.
KEY WORDS:borneol; astragaloside Ⅳ;in vivoabsorption; intestinal circulation
中图分类号:285.5
文献标志码:A
文章编号:1007-7693(2017)11-1552-05
DOI:10.13748/j.cnki.issn1007-7693.2017.11.011
引用本文:陈力, 李静, 蒋斌. 冰片对黄芪甲苷体内吸收的促进作用[J]. 中国现代应用药学, 2017, 34(11): 1552-1556.
作者简介:陈力,男,硕士,主管药师 Tel: 13980941287 E-mail: clkk216@163.com
*通信作者:蒋斌,男,工程师 Tel: 13350879489 E-mail: bin.jiang@btyy.com
收稿日期:2017-05-17