 (1)
(1)程开生,丁竞男,陈建斌
(合肥合源药业有限公司,合肥 230088)
摘要:目的对溶出仪自动取样系统进行校准。方法采用经机械校准合格的溶出仪,对D、K 2种自动取样系统的取样体积、取样时间进行校准,对溶出仪采用自动与手动取样时的整机性能进行校准,并比对连续多个取样时间点自动与同时手动取样的水杨酸片的溶出量以计算偏差。结果溶出仪机械性能校准合格,自动与手动取样时溶出仪的整机性能校准合格,D、K 2种自动取样系统体积误差SS≤±2%,精密度SR≤3%,取样值滤过时间均<30 s,表明取样快速,取样体积准确、精密;D自动取样系统与手动取样溶出的比值R的均值在篮法和桨法下均<100%,且有部分点<95%,而K自动取样系统的R均值约为98%~102%,表明D系统存在一定偏差,而K系统无明显偏差。结论应对自动取样系统进行校准,对其偏差进行评估,制定可接受标准,建议体积误差SS≤±5%,精密度SR≤5%,取样值滤过时间均<30 s;溶出量≤50%的点R均值为95%~105%,R的相关标准偏差≤5%;溶出量>50%的点R均值为97%~103%,R的相对标准偏差≤5%。
关键词:溶出;自动取样系统;校准
由于缓控释制剂的开发和仿制药一致性评价的强力推进,对于固体制剂体外溶出的重视,除了对国内外溶出文献的数字化解析外[1],溶出试验获取的数据更具有参考价值。导致工作中溶出试验工作量剧增,为减少劳动强度,个体差异,设备厂商推出了自动取样的新型溶出仪[2]。不同厂家所带自动取样系统型号繁多,主要功能至少包括自动取样和补液。
溶出试验仪器性能指标的优良是溶出结果及溶出曲线能否符合要求的基本前提,是对仪器物理性能验证和校准溶出度测定结果准确的根本保证[3]。国家食品药品监督管理总局组织2016年4月制定并公布了《药物溶出度仪机械验证指导原则》[4],对水平度、垂直度、同轴度、摆动、转速、杯内温度等10项指标进行验证。除机械校验证外,整机性能还应采用化学校正来验证,即采用标准片在规定的溶出条件下,测定标准片的溶出量,并与标准片说明书中规定的溶出范围进行比较,确定溶出仪的整机性能指标是否符合药典要求[5]。即使按上述标准对溶出仪校验,溶出结果仍然存在较大差异。夏佳等[6]采用经校正的溶出仪对水杨酸片不确定度研究分析表明,理论分析不确定度仅为1.14%,215家实验室最大偏差达7%,这可能与不确定来源分析未考虑转速、溶出过程操作等因素有关。
溶出仪校正过程中,可能出现机械校准合格,而整机性能不合格,或者整机性能虽合格,但是最终溶出结果差异大的情况。
溶出仪经校准合格但溶出结果差异大的原因是,现有标准没有考虑到自动取样带来的影响,无法分析是溶出仪本身机械能导致的偏差还是自动取样系统导致的偏差。美国药典(USP)通则1092[7]规定溶出自动化要与药典标准操作进行偏差比对。依照该通则对笔者所在公司2种自动取样系统进行校准。
UV-2550紫外分光光度计及工作站(日本岛津);溶出仪1(D自动取样系统)、溶出仪2(K自动取样系统),均来自甲公司;XS-105型电子分析天平(梅特勒托利多公司);水杨酸(上海润捷化学试剂有限公司,批号:20150601,纯度:100%);水杨酸片(中国国药品生物制品检定所,批号:100103-201512)。磷酸二氢钾、氢氧化钠均购自国药集团化学试剂有限公司,水为纯化水或超纯水。
溶出仪1和2依《药物溶出度仪机械验证指导原则》,对水平度、垂直度、同轴度、摆动、转速、杯内温度等10项指标进行验证。
溶出杯内加入900 mL纯化水,设定桨法转速100 r·min-1及水浴温度37.0 ℃,启动运行至恒定水温(约1 h)。自动取样系统设定5 min后取样,取样量为2 mL,取样前,分别对各空取样瓶标记称重,取样结束收集称重,计算取样体积误差(SS)及取样体积精密度(SR),计算公式分别见式(1)和式(2);设置30 min后取样,取样量为8 mL,同法计算。
 (1)
(1)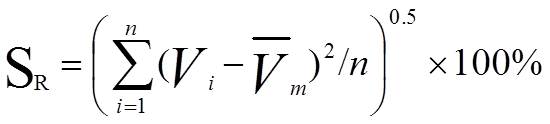 (2)
(2)
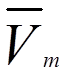 为所有取样点实测取样量的算术平均值(mL);Vs为取样量设定值(mL);Vi为任一样品取样体积(mL);n为同一组测量中取样数量。
为所有取样点实测取样量的算术平均值(mL);Vs为取样量设定值(mL);Vi为任一样品取样体积(mL);n为同一组测量中取样数量。
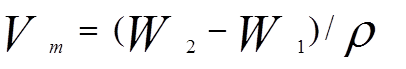 (3)
(3)Vm为实测取样量;W2为取样瓶+纯化水的质量(g);W1为取样瓶的质量(g);ρ为37.0 ℃纯化水的密度(0.993 325 g·mL-1);
以到达设定取样时间时按下秒表开始计时,直到最后一个样品转移至取样瓶中的时间,停止计时,记录时间,取样时长不超过30 s。
取本品,照溶出度与释放度测定法(中国药典2015年版四部通则0931 第一法)[8],以pH 7.4的磷酸盐缓冲液(取磷酸二氢钾6.80 g,加氢氧化钠1.58 g,用水稀释至1 000 mL,即得)为溶出介质,转速为100 r·min-1,选取水杨酸片12片称重后,依法(篮法和桨法)操作,自水杨酸片接触溶出介质时开始计时,经30,60,120 min时同时双人手动和(或)自动取样系统取样,同批次滤膜滤过以避免滤膜引起的差异,同时补充等体积溶出介质,取续滤液为供试品溶液。取供试品溶液及对照品溶液(1),按照紫外-可见分光光度法(中国药典2015年版通则0401)[8],定量稀释后在296 nm处测定吸光度;另精密称取水杨酸对照品20 mg,加水溶解并定量稀释制成每mL约含16 μg的溶液,同法测定。计算即得。该批水杨酸片在篮法和桨法下30 min的溶出限度为21%~26%和20%~27%,RSD应≤5%和≤7%。并计算各时间点自动取样与手动取样溶出的比值(R),计算见式(4)。
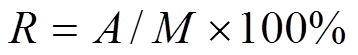 (4)
(4)A为自动取样溶出度;M为手动取样溶出度。
2.4.1 溶出仪机械校正结果 溶出仪1和2机械校正结果符合要求。
2.4.2 取样体积和取样时间校准结果 在5和30 min时分别取样2,8 mL,D、K 2种自动取样系统的取样时间均<30 s。
D、K 2种自动取样系统的取样体积结果见表1。分别取样2 mL和8 mL,D取样系统的取样体积误差为-1.9%和-0.5%,比较准确,而K取样系统的体积误差均为0,非常准确;取样体积精密度,D系统均<3%,而K系统仅约为D系统的1/3。因此2种系统的取样体积是准确和精密的。
2.4.3 水杨酸片校准结果 水杨酸片校准结果见表2~5。溶出仪1和2分别通过手动取样和自动取样,30 min溶出,不论篮法还是桨法,其溶出量和RSD均符合水杨酸片校准要求。
表1 D、K自动取样系统取样体积准确度和精密度
Tab. 1 Accuracy and precision of auto sampling system D and K

表2 水杨酸片用D自动取样与手动取样溶出对比(篮法100 r·min-1)
Tab. 2 Dissolution of salicylic acid tablets sampling by auto D versus manual(basket 100 r·min-1) %
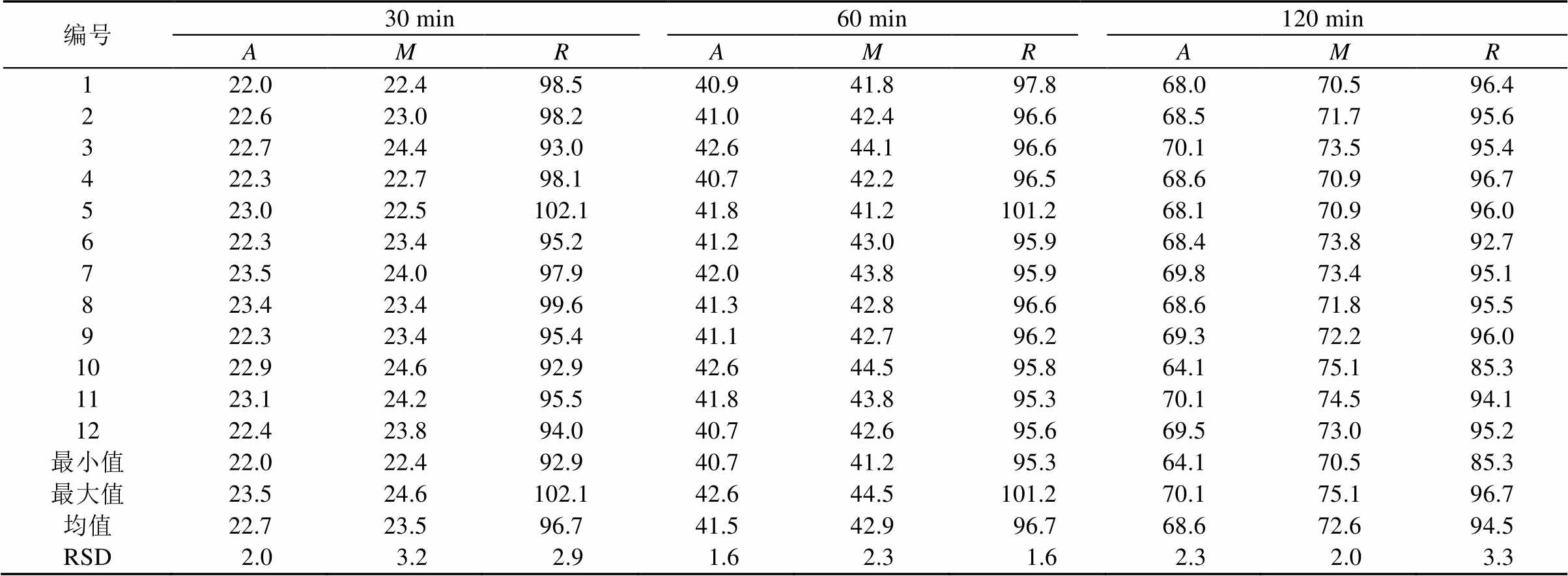
表3 水杨酸片在溶出仪1用D自动取样与手动取样溶出对比(桨法100 r·min-1)
Tab. 3 Dissolution of salicylic acid tablets sampling by auto D versus manual(paddle 100 r·min-1) %

表4 水杨酸片在溶出仪2用K自动取样与手动取样溶出对比(篮法100 r·min-1)
Tab. 4 Dissolution of salicylic acid tablets sampling by auto K versus manual(basket 100 r·min-1) %

表5 水杨酸片在溶出仪2用K自动取样与手动取样溶出对比(桨法100 r·min-1)
Tab. 5 Dissolution of salicylic acid tablets sampling by auto K versus manual(paddle 100 r·min-1) %

2.4.4 自动与手动取样的比较 水杨酸片在溶出仪1采用篮法,在30,60,120 min时,D自动取样和手动取样的溶出12片的精密度RSD均<5%,表明校准片、溶出仪机械性能、手动取样操作、自动取样系统内和分析检测的精密度良好;自动与手动溶出比值R分别为96.7%,96.7%,94.5%,均<100%,且有<95%的点,表明D自动取样与手动取样存在一定偏差;相应时间点12片R值精密度RSD分别为2.9%,1.6%,3.3%,表明自动与手动取样的偏差是精密的。桨法时,D自动取样和手动取样的溶出12片的精密度RSD均<7%,表明校准片、溶出仪机械性能、手动取样操作、自动取样系统内和分析检测的精密度良好;自动与手动溶出比值R分别为93.4%,97.8%,96.7%,均<100%,且有<95%的点,表明D自动取样与手动取样存在一定偏差;相应时间点12片R值精密度RSD分别为4.5%,2.2%,1.7%,表明自动与手动取样的偏差是精密的。
水杨酸片在溶出仪2采用篮法和桨法,在30,60,120 min时,K自动取样和手动取样的溶出12片的精密度RSD均<3%和<5%,比溶出仪1和D自动取样的结合更精密。篮法和桨法下自动与手动溶出比值R分别为99.0%、101.8%、101.2%和97.8%、101.1%、100.8%,范围约为98%~102%均<100%。篮法和桨法相应时间点12片R值精密度RSD均<5%,表明自动与手动取样的偏差是精密的。
采用水杨酸片对2台经机械校正合格的溶出仪进行整机性能校正,篮法和桨法下,自动与手动取样的溶出度均符合校正片要求。
为了评价自动取样系统的性能指标,对取样体积、取样时间和溶出结果与标准的手动取样进行比对偏差。
为此设定了体积误差SS及取样体积精密度SR作为自动取样取样体积评价指标,校准的D、K自动取样系统SS≤±2%,SR≤3%,由于取样体积一般≤10 mL,取样次数≤10次,溶出液体积≥500 mL,总偏差应不大于溶出液体积的1%,即总偏差≤5 mL,换算到每次取样的偏差应≤0.5 mL,SS≤±5%是可以接受的,如果取样体积小和(或)取样次数少,可以根据具体药品适当放宽。取样精密SR≤5%也是可以接受的。
中国药典规定取样至滤过时间为30 s,USP取样时间相对偏差可接受标准为±2%。USP所规定的应该是取样时间而不包括滤过时间,即便如此,手动取样在前期如5 min取样时允许的偏差仅有6 s,取6份样品比较难达到,取12份样品则几乎不能。而自动取样可同时取样,减少了手动序贯取样的偏差。因此采用中国药典的可接受标准,取样滤过时间≤30 s。即便如此,对于同时取样12份,也需要2人同时操作。
自动与手动的偏差,USP可接受标准与溶出中间精密度一致,即溶出量<85%的点为10%,>85%的点为5%。其实是一个非常宽泛的标准,用于相同溶出仪下自动取样系统与手动取样的差异并不合适。按照水杨酸片校准可接受标准,手动与自动取样均符合要求,但是两者比值因自动取样系统的不同而存在差异,因此采用自动与手动溶出的比值R这个指标更能反映自动取样系统的性能,且不受溶出方法差异的影响。比值R的均值反映自动取样系统的偏差,<100%为负偏差,自动取样溶出小于手动溶出;反之,>100%则为正偏差。自动取样系统含多个取样过程,多个取样过程是否精密则采用R值的相对标准偏差来衡量。建议R值的均值和可接受标准为:溶出量≤50%的点R均值为95%~105%,R的相关标准偏差≤5%;溶出量>50%的点R均值为97%~103%,R的相对标准偏差≤5%。
采用上述指标进行溶出仪自动取样系统校准,可以忽略取样系统的系统构造和液体流转过程,整体评价系统的偏差。如果需要分析系统偏差的原因,需根据系统构造与流路分析,可能原因有取样时间过长导致溶出结果偏大,排空和润洗不良导致前次取样残留混杂导致溶出偏低,清洗效果不好导致污染等。
REFERENCES
[1] LUAN N, RUAN H, SHI Y F, et al. Application of graph digitizer software in the consistency evaluation of the dissolution curve of generic drugsin vitro[J]. Chin J Mod Appl Pharm(中国现代应用药学), 2017, 34(1): 78-80.
[2] WANG Z, WANG S, LI S R, et al. Dissolution tester automatic sampling system and its application [J]. Chin J Pharm Anal(药物分析杂志), 2010, 30(6): 1152-1156.
[3] GAO Y C, WANG Z, YU M, et al. Dissolution apparatus and quality consistency evaluation for generics [J]. Chin J New Drugs(中国新药杂志), 2015, 24(3): 317-324.
[4] 国家食品药品监督管理总局. 药物溶出度仪机械验证指导原则的通告[Z]. 2016.
[5] NING B M, HE L, ZHANG Q R, et al. Overview and pplication of reference standard tablets for dissolution tester qualification [J]. Chin J Pharm Anal(药物分析杂志), 2012, 32(8): 1509-1515.
[6] XIA J, FU X, CHEN Z. Study on the uncertainty and the Z score for the determination of dissolution rate of salicylic acid tablets [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2015, 32(12): 1460-1463.
[7] USP 40 [S]. General Chapter <1092>.
[8] 中国药典. 四部[S]. 2015: 通则0931, 0401.
(本文责编:李艳芳)
Verification of Dissolution Apparatus Auto Sampling System
CHENG Kaisheng, DING Jingnan, CHEN Jianbin
(Hefei Cosource Pharmaceuticals Inc, Hefei 230088, China)
ABSTRACT:OBJECTIVETo evaluate and verification the dissolution apparatus auto sampling system.METHODSEmployed mechanical qualified dissolution apparatus, evaluate the auto sampling system D, K based on the accuracy(SS) and precision(SR) of sampling volume and time of sampling to filter. Verificate the overall performance of dissolution apparatus based on the dissolution of salicylic acid tablets. The ratio of auto to manual in three sampling time points was calculated.RESULTSD & K auto sampling system sampling accuracy(SS) were within ±2% and precision(SR) were ≤3%. The sampling time <30 s. It was suggested the D & K auto sampling system were fast, accurate and precisely. The average ratio of auto D to manual were <100%, sometimes were <95%, which the ratio of auto K was in the range of 98%-102%.The results showed that there was a certain deviation in D system, but there was no obvious deviation in K system.CONCLUSIONThe auto sampling system should be verificated. It is suggested the acceptal criteria is: sampling time ≤30 s, SS≤±5%, SR≤5%; Average of R is in the range of 95%-105% and RSD ≤5% at time points with ≤50% dissolved, which is 97%-103% and RSD ≤5% for time points >50%.
KEY WORDS:dissolution; auto sampling system; verification
中图分类号:R917
文献标志码:B
文章编号:1007-7693(2017)11-1589-04
DOI:10.13748/j.cnki.issn1007-7693.2017.11.020
引用本文:程开生, 丁竞男, 陈建斌. 溶出仪自动取样系统的校准[J]. 中国现代应用药学, 2017, 34(11): 1589-1592.
作者简介:程开生,男,硕士,高级工程师 Tel: (0551)65396612 E-mail: chengksn@126.com
收稿日期:2016-12-28